


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、化学反应中既有物质变化又有能量变化 |
| B、即使没有发生化学变化,也可能有能量的变化 |
| C、任何化学反应中的能量变化都表现为热量变化 |
| D、物质的化学能可以通过不同的变化方式转化为热能、电能等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中CCl4为氧化剂 |
| B、金刚石属于金属单质 |
| C、CCl4是一种有机化合物 |
| D、该反应属于置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 需除杂的物质 | 试剂 | 操作 |
| A | NaCl(Na2CO3) | 稀盐酸 | 蒸发结晶 |
| B | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
| C | Cl2(H2O) | 碱石灰 | 洗气 |
| D | CO2(CO) | -- | 点燃 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
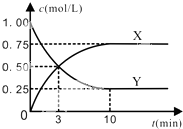 在一恒温、恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:
在一恒温、恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)键线式
(1)键线式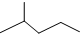 表示的分子式
表示的分子式查看答案和解析>>
科目:高中化学 来源: 题型:
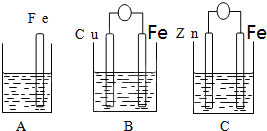
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com