
 2HI(g)
2HI(g) 2HI(g)
2HI(g)| c2(HI) |
| c(H2)?c(I2) |
| 0.022 |
| 0.04×0.04 |
| 0.01 |
| 0.05 |


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B、工业制漂白粉的反应:Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O |
| C、用铜作电极电解饱和食盐水:2Cl-+2H2O=2OH-+Cl2↑+H2↑ |
| D、铜片跟稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,以任意比混合的氢气和一氧化碳气体共8.96L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2NA |
| B、56g铁和足量氯气完全反应,转移的电子数为3NA |
| C、25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
| D、1mol FeCl3完全转化为Fe(OH)3胶体后形成的胶粒数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
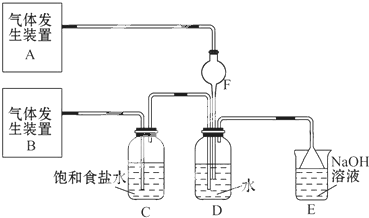
查看答案和解析>>
科目:高中化学 来源: 题型:
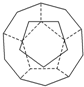 德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图.
德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
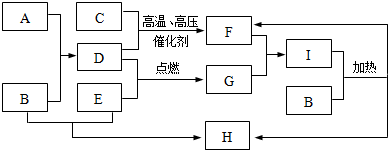
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com