
����Ŀ��ij����ャҺ����Al(OH) 3��MnO2������Na2CrO4�����ǵ��������������ʹNa2CrO4������ȫ��ˮ������ij�о�С������ij�ַ�����ʹ��Һ����ɹ�������ͺ���Ԫ����Һ������������,�ش��й����⡣

������ͼ�еIJ��ַ�������ͷ�Ӧ����δ������
��1����Ӧ�������Լ�NaOH�ĵ���ʽΪ______________��C��Al���Ʊ�������Ϊ_____________��
��2����С��̽����Ӧ�ڷ�����������D��Ũ�����ϣ������ȣ��ޱ仯��������Cl2���ɣ�����Ӧֹͣ������ʣ�࣬��ʱ�μ����ᣬ�ֲ���Cl2 ���ɴ��ж�Ӱ��÷�Ӧ��Ч���е�������(�����)____________��
a���¶� b��Cl����Ũ�� c����Һ�����
 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ������CO��H2�ϳɼ״�����CO��H2��Դ��ú���������ش��������⡣
��I��.��1����֪����H2(g)+1/2O2(g)=H2O(g) ��H1=-241.8kJ/mol
��C(s)+ ![]() O2(g)=CO(g) ��H2=-110.5kJ/mol
O2(g)=CO(g) ��H2=-110.5kJ/mol
��̿��ˮ������Ӧ���Ȼ�ѧ����ʽΪ_____________��
��2����֪��ӦCO(g)+2H2(g)![]() CH3OH(g) ��H=-99kJ/mol�е���ػ�ѧ���������£�
CH3OH(g) ��H=-99kJ/mol�е���ػ�ѧ���������£�

��x=________
��II��(3)��һ�ݻ��ɱ���ܱ������У�lmolCO��2molH2������Ӧ��CO(g)+2H2(g) ![]() CH3OH(g), CO�ڲ�ͬ�¶��µ�ƽ��ת����(a)����ѹǿ�Ĺ�ϵ����ͼ��ʾ��
CH3OH(g), CO�ڲ�ͬ�¶��µ�ƽ��ת����(a)����ѹǿ�Ĺ�ϵ����ͼ��ʾ��

���÷�Ӧ����S_____0��ͼ�е�Tl____T2������>������<������=��)��
���úϳɷ�Ӧ���¶�һ�������240��270����ѡ����¶ȷ�Χ��ԭ���У�________��
��ͼ��a��ʱ��CH3OH�����ʵ�������Ϊ_______���÷�Ӧ��ѹǿƽ�ⳣ��ΪKp=______(KPa)-2����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�����������
��4�����úϳ���(��Ҫ�ɷ�ΪCO��H2)�ϳɼ״���������Ҫ��Ӧ���£�
I: CO(g)+2H2(g) ![]() CH3OH(g) ��H1
CH3OH(g) ��H1
II��CO2(g)+H2(g) ![]() CO(g)+H2O(g) ��H2
CO(g)+H2O(g) ��H2
III��CO2(g)+3H2(g) ![]() CH3OH(g) +H2O(g) ��H31
CH3OH(g) +H2O(g) ��H31
������Ӧ��Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2��K3���������¶ȱ仯��������ͼ��ʾ��

����H1______��H3������>������<������=��)��������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ�۷���ϡ������Һ�У����Ⱥ������Ա仯������������ij���κ�ͭ�����ܽ⣬��������( )
A��NaCl B��KNO3 C��K2SO4 D��Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������仯�����ת������Դ���úͻ�����������Ҫ�о����⡣
��1����֪��ӦI: 2SO2(g)+O2(g)![]() 2SO3(g),��H��-196.6kJ��mol-1
2SO3(g),��H��-196.6kJ��mol-1
��ӦII: 2NO(g)+O2(g)![]() 2NO2(g),��H��-113.0kJ��mol-1
2NO2(g),��H��-113.0kJ��mol-1
��SO2(g)��NO2(g)��Ӧ����SO3(g)��NO(g)���ȷ�Ӧ����ʽΪ________��
��2�������ھ��Ⱥ����ܱ�������ͨ��һ������SO2��O2��һ�������·�����ӦI��һ��ʱ���ڣ�����Ӧ������ʱ��仯��������ͼ��ʾ������a��ʱ����Ӧ______(�����ﵽ������δ�ﵽ��)ƽ��״̬��t1��t3ʱ���ڣ�v����������С����Ҫԭ����___________��

������������ͬ���Ⱥ����ܱ������зֱ����A��2molSO2(g)��1molO2(g)��B:2molSO3(g)������������ͬ��������ӦI���ﵽƽ��ʱ����÷�Ӧ��ƽ�ⳣ����A _____B(����>���������������� �� )��
��3����֪�����£�H2S�ĵ��볣����K1=1.3��10-7, K2=7.1��10-15����0.lmol/LH2S��Һ��pHԼΪ_______(ȡ��������ֵ)����Ũ�Ⱦ�Ϊ0.001mol��l-1��AgNO3��Hg(NO3)2�����Һ��ͨ��H2S���壬��ʼ���ɳ�����c(S2-)Ϊ_______��(��֪��Ksp(Ag2S)=6.3��10��50��Ksp(HgS)=1.6��10��52)
��4��NH3����ԭ�����\����SCR����ĿǰӦ�ù㷺���������������ѳ�����������NO��NO2�Ļ����6L������ͬ��ͬѹ��7L��NH3ǡ��ʹ����ȫת��ΪN2����ԭ���������NO��NO2�����ʵ���֮��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2CO(g)+O2(g)=2CO2(g)��H=-566kJ��mol-1 ��Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g)��H=-226 kJ��mol-1
���������Ȼ�ѧ����ʽ�жϣ�����˵����ȷ���ǣ� ��
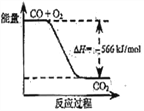
A. CO��ȼ����Ϊ283 kJ
B. ��ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ���̺�������ϵ
C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ��H��-452 kJ��mol-1
D. CO(g)��Na2O2(s)��Ӧ�ų�509 kJ����ʱ������ת����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Simons�ȿ�ѧ�ҷ�����ʹNH3ֱ������ȼ�ϵ�صķ�������װ��Ϊ�ò���Ϊ�缫������������Һ�У�һ���缫ͨ���������һ�缫ͨ�백�������ط�ӦʽΪ 4NH3+3O2�T2N2+6H2O ����Ϊ�������ҺӦ���ԣ�����ԡ������ԡ������ԡ�����д�������ĵ缫��Ӧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʷ�����ᴿ�ķ������������ ��
A. ���ܽ⡢���˷������Ȼ��غͶ������̵Ĺ�������
B. �ýᾧ����������غ��Ȼ��ƵĹ�������
C. �üӾƾ���ȡ�ķ�����ȡ��ˮ�е���
D. ��������ƾ���ˮ�Ļ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ�������ָʾ�������в����п���ʹ����NaOH��Һ��Ũ����ֵƫ�͵���
A. ��ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B. �ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и���
C. ��ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D. ��ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������������������ȷ���ǣ� ��
A���ڱ�״̬�£�1L������ȫȼ�պ������ɵ���̬����ķ�����Ϊ![]() NA
NA
B��1mol̼������CH5+�����ĵ�����Ϊ11NA
C����״̬�£�16g������ȫȼ�������ĵ������ķ�����Ϊ2NA
D��0.5molC3H8�����к�C��H���ۼ�2NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com