
| A、元素原子半径大小呈周期性变化 |
| B、元素相对原子质量依次递增 |
| C、元素原子最外层电子排布呈周期性变化 |
| D、元素的最高正化合价呈周期性变化 |


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
| A、砹化氢(HAt)很稳定 |
| B、单质砹易溶于某些有机溶剂 |
| C、砹的原子半径比碘的原子半径大 |
| D、单质砹是无色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H3BO3的酸性比H2CO3的强 |
| B、Mg(OH)2的碱性比Be(OH)2的强 |
| C、HCl、HBr、HI的热稳定性依次增强 |
| D、若M+和R2-的核外电子层结构相同,则离子半径:M+>R2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第6周期,ⅣA族 |
| B、第7周期,ⅣA族 |
| C、第6周期,ⅢA族 |
| D、第7周期,ⅢA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.9mol/L |
| B、0.45m01/L |
| C、0.25mol/L |
| D、0.225mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如图.
某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如图.| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
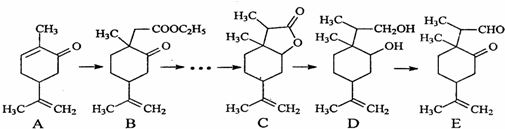
| CH3I |
| 催化剂 |
| LiBH4 |
| THF |
| LiBH4 |
| THF |
| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com