
【题目】把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58 g白色沉淀析出,向所得的浊液中,逐滴加入0.5 mol·L-1的盐酸,加入盐酸的体积和生成沉淀的质量关系如图所示。

(1)混合物中NaOH的质量是______ g。
(2)P点所表示盐酸加入的体积为______ mL。
【答案】 2.6 130
【解析】(1)向所得浊液中,逐滴加入0.5mol/L盐酸,由加入盐酸的体积和生成沉淀的质量关系图分析:①0-10mL,随盐酸的体积增加,生成沉淀的质量不变,说明沉淀是Mg(OH)2,m[Mg(OH)2]=0.58g,NaOH、AlCl3、MgCl2组成的混合物,溶于足量水发生反应是:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;AlCl3+4NaOH=NaAlO2+3NaCl+2H2O,NaOH有剩余,溶液是NaCl、NaAlO2和NaOH的混合液,该阶段发生反应是:NaOH+HCl=NaCl+H2O;②10mL处,加入10mL盐酸刚好中和未反应的NaOH,溶液为NaCl、NaAlO2;③10mL-30mL,随盐酸的体积增加,生成沉淀的质量增加,该阶段发生反应是:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;④30mL处,NaAlO2与盐酸恰好反应,需盐酸体积为:30mL-10mL=20mL,n(HCl)=0.02L×0.5mol/L=0.01mol,沉淀质量达到最大,溶液为NaCl溶液;⑤30mL-P点,随盐酸的体积增加,沉淀的质量减少,发生反应是:Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3 HCl=AlCl3+3H2O;⑥P点,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液。选30mL处,计算NaOH的质量,此时溶液为NaCl溶液,溶液中Cl-来源于原混合物中的AlCl3、MgCl2和加入的30mlHCl,溶液中Na+来源于原混合物中的NaOH,根据NaAlO2 + HCl + H2O=Al(OH)3↓+NaCl可知n(NaAlO2)= n(HCl)=0.01mol,由Al原子守恒得原混合物中n(AlCl3)=n(NaAlO2)=0.01mol,由Mg原子守恒得原混合物中n(MgCl2)=n[Mg(OH)2]= ![]() =0.01mol,由Na+离子和Cl-离子守恒得:n(NaOH)=n(NaCl)=n(Cl-)=2n(MgCl2)+3n(AlCl3)+n(HCl)=0.01mol×2+0.01mol×3 +0.03L×0.5mol/L=0.065mol,所以原混合物中NaOH的质量为:m(NaOH)=0.065mol×40g/mol =2.6g,故答案为:2.6
=0.01mol,由Na+离子和Cl-离子守恒得:n(NaOH)=n(NaCl)=n(Cl-)=2n(MgCl2)+3n(AlCl3)+n(HCl)=0.01mol×2+0.01mol×3 +0.03L×0.5mol/L=0.065mol,所以原混合物中NaOH的质量为:m(NaOH)=0.065mol×40g/mol =2.6g,故答案为:2.6
(2)30mL-P点,随盐酸的体积增加,沉淀的质量减少,发生反应是:Mg(OH)2+2HCl=MgCl2+2H2O、Al(OH)3+3 HCl=AlCl3+3H2O;P点,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液,P点所加盐酸相当于用于中和原混合物中的NaOH,此时所加盐酸物质的量:n(HCl)=n(NaOH)=0.065mol,P点所表示盐酸的体积为:V=![]() =0.13L=130mL,故答案为:130。
=0.13L=130mL,故答案为:130。


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如右图所示。下列结果不正确的是( )
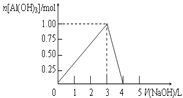
A. 反应过程中,沉淀最多时的质量为78g
B. 反应过程中,Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积可能为3.5L
C. AlCl3溶液的浓度为2.0mol/L
D. 当V(NaOH)=4.0L时,得到的溶液中Na+、Cl-浓度一定不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有两瓶失去标签的溶液,其中一瓶是KHSO4溶液,另一瓶是KOH溶液.鉴别时,下列选用的试纸或试剂不正确的是( )
A.pH试纸
B.紫色石蕊试液
C.K2CO3固体
D.KCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~H等8种物质存在如下转化关系(反应条件及部分产物未标出)。已知:A是正盐,B是能使品红溶液褪色的气体;G是红棕色气体。按要求回答问题:
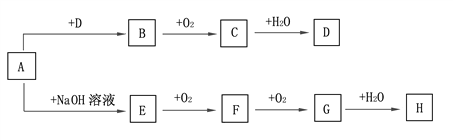
(1)写出下列物质的化学式:A. ___________, B.____________, C.____________。
(2)A→B的离子方程式:________________________________________;
E→F的化学方程式:__________________________________________;
H的浓溶液与铜反应的离子方程式:_______________________________。
(3)检验某溶液中含D中阴离子的方法是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“化学,让城市更美好”,下列叙述不能直接体现这一主题的是( )
A.绿色食品,让人类更健康B.合成光纤,让通讯更快捷
C.火力发电,让能源更清洁D.环保涂料,让环境更宜居
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列结论正确的是( ) 
A.该有机物分子式为C13H16
B.该有机物属于苯的同系物
C.该有机物分子至少有4个碳原子共直线
D.该有机物分子最多有13个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解2L 1molL﹣1的硫酸铜溶液,在电路中通过0.5mol电子后,将电源反接,电路中又通过1mol电子,此时溶液中c(H+)是(设溶液体积不变)( )
A.1.5 molL﹣1
B.0.5 molL﹣1
C.0.75 molL﹣1
D.0.25 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答氯碱工业的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品.理论上k=
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42﹣等杂质,必须精制后才能供电解使用.精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②盐酸 ③BaCl2 , 这三种试剂添加的合理顺序是(填序号)
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能30%以上.在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过. 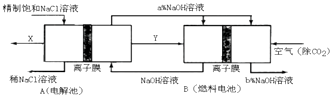
①图中X、Y分别是、(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 .
②分别写出燃料电池B中正极、负极上发生的电极反应:、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的溶液,造成浓度偏高的操作是
A.洗涤后的容量瓶未干燥B.移液后,未洗涤烧杯和玻璃棒
C.定容时,眼睛视线俯视刻度线D.移液时,不慎将液体流到瓶外
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com