
����Ŀ����������Ĵ��ڻ��ƻ�����������һֱ�ڻ���̽�����ƴ�����������Ч��ʩ����֪��N2(g)+O2(g)![]() 2NO(g) ��H=+181.5kJ��mol��1
2NO(g) ��H=+181.5kJ��mol��1
��1�������������γɳ�����ն��⻯ѧ������_______(�о�һ��)�ȴ�����Ⱦ���������֮һ��
��2��ij����С�鳢�����ù����������ս���NO�ķֽ⡣����![]() ��
��![]() ��
��![]() ��
��![]() �ֱ��ʾN2��NO��O2����������ڹ����������ֽ�NO�Ĺ�����ͼ��ʾ���������������Ĺ����У�����״̬��͵���_______(����ĸ���)��
�ֱ��ʾN2��NO��O2����������ڹ����������ֽ�NO�Ĺ�����ͼ��ʾ���������������Ĺ����У�����״̬��͵���_______(����ĸ���)��

��3���¶�ΪT1ʱ�����ݻ�Ϊ1L�ĺ����ܱ������г���0.6molNO2����������Ӧ2NO2(g)![]() 2NO(g)+O2(g) ��H>0����ƽ��ʱc(O2)=0.2mol��L��1������¶��·�Ӧ��ƽ�ⳣ��Ϊ______��ʵ���ã�v��=v(NO2)����=k��c2(NO2)��v��= v (NO2)����=2v(O2)����=k��c2(NO)��c(O2)��k����k��Ϊ���ʳ����������¶�Ӱ�졣���¶ȸı�ΪT2ʱ����k��=k������T1_____T2(����>������<��)��
2NO(g)+O2(g) ��H>0����ƽ��ʱc(O2)=0.2mol��L��1������¶��·�Ӧ��ƽ�ⳣ��Ϊ______��ʵ���ã�v��=v(NO2)����=k��c2(NO2)��v��= v (NO2)����=2v(O2)����=k��c2(NO)��c(O2)��k����k��Ϊ���ʳ����������¶�Ӱ�졣���¶ȸı�ΪT2ʱ����k��=k������T1_____T2(����>������<��)��
��������(NOx)�ǵ糧��Ҫ�ŷŵ���Ⱦ��֮һ����ҵ�ϲ��ð������������ŷţ�ԭ�����£�
��4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) ��H1=��1632.4kJ��mol��1��
4N2(g)+6H2O(g) ��H1=��1632.4kJ��mol��1��
��4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) ��H2=akJ��mol��1��
5N2(g)+6H2O(g) ��H2=akJ��mol��1��
����Ӧ�¶ȹ���ʱ��NH3����������Ӧ��
��4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H3=��902.0kJ��mol��1��
4NO(g)+6H2O(g) ��H3=��902.0kJ��mol��1��
��4����Ӧ���е�a=______��
��5����Ӧ���У����õĴ�����Cr2O3��Fe2O3��Cr2O3�Ĵ�Ч�ʸ���һЩ�����б�ʾ���ִ����ڷ�Ӧ�ڴ������е������仯ʾ��ͼ��������______(��ѡ����ĸ)��

�����õ�ⷨ�������¿�����ϡ����NO(O2Ũ��ԼΪNOŨ�ȵ�10��)��װ��ʾ��ͼ���£��������ʿɴ���O2��
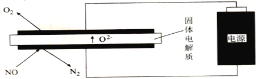
��6�������ĵ缫��ӦʽΪ______��
��7������һ������NO�����ĵĵ���ԶԶ�������ۼ����������ܵ�ԭ����(��������������)______��
��8��ͨ�������缫����Ĵ��������Ը�����һ״�������ô�������______�ԡ�
���𰸡������������꣩ C 0.8 < -1815.0 B 2NO+4e-=N2+2O2- ������������ӦO2+4e-=2O2- ѡ��
��������
��1�������������γɳ�����ն��⻯ѧ����������������ȴ�����Ⱦ���������֮һ��
��2���ƻ���ѧ����Ҫ�����������γɻ�ѧ����Ҫ�ų�����������Խ��Խ���ȶ���Խ��Խ�ȶ���
��3�������¶�ƽ�������ȷ�Ӧ�����ƶ���
��4�����ݸ�˹���ɼ���aֵ��
��5����Ӧ���У�Cr2O3�Ĵ�Ч�ʸ���һЩ������ʹ��Cr2O3��ܸ��ͣ����ݼ��㷴Ӧ�ڵķ�Ӧ������������С�ڷ�Ӧ�
��6������������ԭ��Ӧ��
��7��������������Ӧ��O2+4e-=2O2-��
��8����������ѡ���ԡ�
��1�������������γɳ�����ն��⻯ѧ����������������ȴ�����Ⱦ���������֮һ��
�ʴ�Ϊ�����������ꣻ
��2���ӻ������Կ���������A״̬�У�NO���������������棬B״̬ΪNO��ΪNԭ�Ӻ�Oԭ�ӣ����������Ҫ����������C״̬ΪNԭ�Ӻ�Nԭ�ӽ�ϱ��N2��Oԭ�Ӻ�Oԭ�ӽ�ϱ��O2���������Ϊ�ɼ����̣���Ҫ�ų���������ϵ�������ͣ�
�ʴ�Ϊ��C��
��3����������ݿ�֪���¶�ΪT1ʱ��c(NO2)=(0.6mol/L-0.4mol/L)��c(NO)=0.4mol/L�� c(O2)=0.2mol/L����ѧƽ�ⳣ��K=![]() =0.8��
=0.8��
�ﵽƽ��״̬ʱ���淴Ӧ������ȣ�����k��c2(NO2)=k��c2(NO)��c(O2)����k��=k������֪
c2(NO2)=c2(NO)��c(O2)����ʱK=![]() =1>0.8�����ڸ÷�Ӧ������ӦΪ���ȷ�Ӧ��˵�������¶�ƽ�������ƶ�������T1<T2��
=1>0.8�����ڸ÷�Ӧ������ӦΪ���ȷ�Ӧ��˵�������¶�ƽ�������ƶ�������T1<T2��
�ʴ�Ϊ��0.8 ��<��
��4����֪��4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) ��H1=��1632.4kJ��mol��1��
4N2(g)+6H2O(g) ��H1=��1632.4kJ��mol��1��
��4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H3=��902.0kJ��mol��1��
4NO(g)+6H2O(g) ��H3=��902.0kJ��mol��1��
���ݸ�˹���ɣ�[��![]() 5-��]
5-��]![]() 4�â�4NH3(g)+6NO(g)
4�â�4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) ��H2=[(��1632.4kJ��mol��1��
5N2(g)+6H2O(g) ��H2=[(��1632.4kJ��mol��1��![]() 5��(��902.0kJ��mol��1��]
5��(��902.0kJ��mol��1��]![]() 4=akJ��mol��1����a=-1815.0
4=akJ��mol��1����a=-1815.0
�ʴ�Ϊ��-1815.0��
��5����Ӧ���У�Cr2O3�Ĵ�Ч�ʸ���һЩ������ʹ��Cr2O3��ܸ��ͣ����ݼ��㷴Ӧ��Ϊ���ȷ�Ӧ�����������������С�ڷ�Ӧ��ģ�Bͼ�������⣬ѡB��
�ʴ�Ϊ��B��
��6������װ��ʾ��ͼ��֪��������ӦΪ��2NO+4e-=N2+2O2-��
�ʴ�Ϊ��2NO+4e-=N2+2O2-��
��7������һ������һ�����������ĵĵ���ԶԶ�������ۼ�������������������������Ӧ��O2+4e-=2O2-��
�ʴ�Ϊ��������������Ӧ��O2+4e-=2O2-��
��8��ͨ�������缫����Ĵ��������Ը�����һ״�������ô�������ѡ���ԡ�
�ʴ�Ϊ��ѡ��


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ�Ĺ���Ԫ�ء�
(1)��λ��Ԫ�����ڱ��������ڢ��壬���̬ԭ����δ�ɶԵ��Ӹ���Ϊ___________��
(2)��̬Fe3+�ĺ�������Ų�ʽ___________
(3)��������һ�ִ��Բ��ϣ���ҵ���Ʊ�ʱ������ˮ�ⷨ���Ʊ�ʱ����������(CO(NH2)2)�������Ƶȼ������ʡ����ط����������ǽ���Ԫ�صĵ縺���ɴ�С��˳����___________����������������������Ŀ֮��Ϊ___________����������̼ԭ�ӵ��ӻ�����___________��
(4)������Ҳ��ʹ�ó��������Ʊ�ʱ�����백(NH3)������(N2H4)�������֪��(NH3�۵㣺��77.8%�桢�е㣺��33.5%��)������(N2H4�۵㣺2�桢�е㣺113.5��C)�������۷е�ߵ͵���Ҫԭ��______________________��
(5)Co(NH3)5BrSO4���γ������ܵ�������֪Co3+����λ��Ϊ6��Ϊȷ����������Ľṹ���ֶ�����������������ʵ�飺�ڵ�һ���������Һ�м�����������Һ������ɫ���������һ������������Ϊ___________���ڵڶ����������Һ�м�����������Һ��������ɫ��������ڶ�������������Ϊ___________��

(6)��������̼�ܽ���r-Fe���γɵ�һ�ּ�϶�����壬���ԣ��侧��Ϊ���������ṹ������ͼ��ʾ��������ʵĻ�ѧʽΪ___________����Ʒ���ܶ�Ϊdg��cm��3���������������̼ԭ�ӵľ���Ϊ___________pm(�����ӵ�������ֵ��NA��ʾ��д����ļ���ʽ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������(K2FeO4)��һ�ָ�Ч��ˮ��.��֪:K2FeO4 ������ˮ,����Һ����ɫ������ŨKOH ��Һ,��0����5����ǿ������Һ�н��ȶ�.ijС��ͬѧ����ͼװ���Ʊ���̽��
K2FeO4 ������.�Ʊ�ԭ��:
3Cl2��2Fe(OH)3��10KOH��2K2FeO4��6KCl��8H2O,װ����ͼ��ʾ(�г�װ����)

(1)ʢ�Ŷ������̵���������___________________,װ��C��������____________________��
(2)װ��A �з�Ӧ�Ļ�ѧ����ʽ��________________________________________��
(3)ʵ��ʱ���ñ�ˮԡ��ԭ����____________________,��װ�ô���һ������ȱ��,��ָ��____________��
(4)K2FeO4 �ֲ�Ʒ����Fe(OH)3��KCl������,һ����75���Ҵ�����ϴ��,��Ŀ����_____________________��
(5)��������֪,K2FeO4 �ܽ� Mn2�������� MnO4��.��С���������ʵ�������֤:

�ر�K,���ձ���Һ���ɫ,���ձ���Һ����ɫ.��������ձ���Һ�ʻ�ɫ��ԭ��,��Ҫ���Լ���__________��д��K2FeO4 ����Mn2�� �����ӷ���ʽ: ___________________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в�����������������ǣ� ��
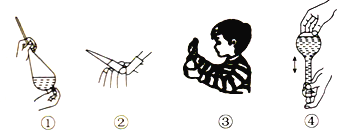
A. ��Ϊ��ȡʱ��������������Ӧ��������
B. ��Ϊ��ʽ�ζ��������������������¼��ʼ����
C. ��Ϊ��������ζ�IJ����������ж��������ܽ��ǿ״ս�ƿ��
D. ��Ϊ������Һ������ҡ�ȵIJ�����ҡ�Ⱥ��������Һ����ڿ̶���Ҳ�����ټ�ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һЩ�����ı�ȼ�������±���

����˵����ȷ���ǣ� ��
A. ���ȶ��ԣ������飾�춡��
B. ������ı�ȼ���ȴ�ԼΪ����H���C3540 kJ��mol-1
C. ����ȼ�յ��Ȼ�ѧ����ʽΪ2C2H6��g��+7O2��g��= 4CO2��g��+6H2O��g�� ��H���C1560.8 kJ��mol-1
D. ��101kPa�£��������ֵ��891.0kJ��g-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��װ����ͼ��ʾ�ĵ绯ѧװ�ã��缫��ΪZn�������缫��ΪCu������˵��������ǣ�
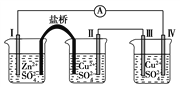
A. �缫������������Ӧ
B. ��ͬʱ���ڣ��缫����缫���������仯ֵ��ͬ
C. �缫���ĵ缫��Ӧ��4OH����4e��===O2����2H2O
D. �������缫�������������缫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��mA(g)+nB(g) ![]() pC(g)+qQ(g)��m��n��p��qΪ��������ʱ���ﵽƽ��ı�־�ǣ��� ��
pC(g)+qQ(g)��m��n��p��qΪ��������ʱ���ﵽƽ��ı�־�ǣ��� ��
����ϵ��ѹǿ���ٸı� ����ϵ���¶Ȳ��ٸı� �۸���ֵ�Ũ�Ȳ��ٸı� �ܸ���ֵ������������ٸı�ݷ�Ӧ����VA:VB:VC:VD=m:n:p:q ��λʱ����m mol A�ϼ���Ӧ��ͬʱp mol CҲ�ϼ���Ӧ
A. �ۢܢݢ� B. �ڢۢܢ� C. �٢ۢܢ� D. �٢ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H��(aq)��OH��(aq)===H2O(l)����H����57.3 kJ��mol��1���ش��й��кͷ�Ӧ�����⡣
(1)��0.1 mol Ba(OH)2���ϡ��Һ������ϡ���ᷴӦ���ܷų�________________kJ������

(2)��ͼװ��������A��������____________��������__________________________��
����ĭ���ϵ�������_____________________________��
Ҫ�ظ���������ʵ���Ŀ���� ____________________��
(3)��ͨ��ʵ��ⶨ�к��ȵĦ�H�������������ڣ�57.3 kJ��mol��1����ԭ������� ____________��
(4)����ͬŨ�Ⱥ�����İ�ˮ(NH3��H2O)����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��__________(�ƫ����ƫС��������Ӱ�족)��
(5)��V1 mL 1.00 mol/L HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ��ʾ(ʵ����ʼ�ձ���V1��V2��50 mL)������������ȷ������____��

A������ʵ��ʱ�����¶�Ϊ22 ��
B����ʵ�������ѧ�ܿ���ת��Ϊ����
C��NaOH��Һ��Ũ��ԼΪ1.00 mol��L��1
D����ʵ�������ˮ���ɵķ�Ӧ���Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����Ϳ����صĹ���ԭ������ͼ��ʾ���ŵ�ʱ�ܷ�ӦΪ:Al+3Cn(AlCl4)+4AlCl4-![]() 4Al2Cl7-+3Cn(Cn��ʾʯī)��
4Al2Cl7-+3Cn(Cn��ʾʯī)��

����˵����ȷ����
A. �ŵ�ʱ������ӦΪ:2Al-6e-+7Cl-= Al2Cl7-
B. �ŵ�ʱAlCl4-��������
C. ���ʱ������ӦΪ: AlCl4-e-+Cn=Cn(AlCl4)
D. ��·��ÿת��3mol���ӣ������1molCn(AlCl4)����ԭ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com