
【题目】甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是

A. 金属性:甲>乙>丁
B. 乙的单质在空气中燃烧生成只含离子键的化合物
C. 原子半径:辛>己>戊
D. 丙与庚的原子核外电子数相差3
【答案】C
【解析】戊的一种单质(金刚石)是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲的原子序数为6-3=3,即甲为Li,由元素在周期表中的相对位置图可知,乙为Na,丙为K,丁为Ca;丁与辛属同周期元素,由第ⅣA族元素可知,己为Si,庚为Ge,辛为Ga;A.同主族,从上到下金属性增强;同周期,从左向右金属性减弱,则金属性甲<乙<丁,故A错误;B.乙的单质在空气中燃烧生成Na2O2,为含离子键和非极性共价键的化合物,故B错误;C.电子层越多,半价越大;同主族从上到下原子半径增大,则原子半径为辛>己>戊,故C正确;D.原子序数等于核外电子数,丙(原子序数为19)与庚(原子序数为32)的原子核外电子数相差32-19=13,故D错误;故选C。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】如图,在盛有稀 H2SO4 的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
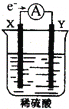
A. 外电路的电流方向为:X→外电路→Y
B. 若两电极分别为Fe和碳棒,则X为碳棒,Y为Fe
C. X极上发生的是还原反应,Y极上发生的是氧化反应
D. 若两电极都是金属,则它们的活动性顺序为X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,反应C(s)+H2O(g)CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.增加C的量
B.将容器的体积减小一半
C.保持体积不变,充入氢气使体系的压强增大
D.保持压强不变,充入氮气使体系的体积增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【贵州省贵阳市2017届高三2月适应性考试(一)】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,是浅绿色晶体,可溶于水,在100℃~110℃时分解,常用作定量分析中的标准试剂。某化学小组以废铁屑为原料在实验室中进行实验探究——制备硫酸亚铁铵并检验其纯度,过程如下:
I.制备硫酸亚铁铵
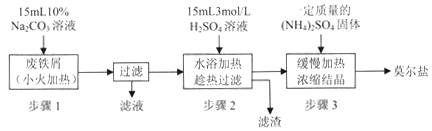
请回答下列问题:
(1)步骤l的作用是_________。(用离子方程式及必要的文字说明);
(2)步骤2中所加硫酸需过量,且不宜等到铁屑完全反应后才过滤,其中蕴含的道理是_______________;
II.测定硫酸亚铁铵的纯度
称取mg实验室制备的硫酸亚铁铵样品,配成500ml溶液,取25. 00mL硫酸亚铁按溶液,用0 . 1mol/L的酸性KMnO4溶液进行滴定,再重复滴定两次。
(3)配制(NH4)2SO4·FeSO4溶液所用的蒸馏水,通常需加热煮沸一段时间后,冷却至室温再使用,这样操作的好处是___________________;
(4)滴定时发生反应的离子方程式为___________________;
(5)滴定终点时的现象为 ___________________;
(6)三次滴定测得酸性KMnO4溶液的用量平均值为VmL,则硫酸亚铁铵样品的纯度为__________;
(7)化学小组分析发现这种检测纯度的方法不够准确,目前处理氮氧化物污染的方法有多种,请你帮助他们设计一种检测方案________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是 ( )
A.向水中通入二氧化碳气体 B.将水加热煮沸
C.向水中投入一小块金属钠 D.向水中加食盐晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | R |
利用表中元素回答下列问题:
(1)X元素在周期表中的位置为__________。
(2)气态氢化物水溶液呈碱性的元素是_____________,此氢化物的电子式__________。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是__________。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)![]() 和
和![]() 是元素R的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为w g,则
是元素R的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为w g,则![]() 的相对原子质量的表达式为___________,元素R的相对原子质量的表达式为______________________。
的相对原子质量的表达式为___________,元素R的相对原子质量的表达式为______________________。
(5)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/L NaOH溶液和1mol O2,则两种气体中相对分子质量较大的气体的分子式及物质的量为__________、_____________,生成硫酸铜的物质的量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各图的叙述,正确的是

A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6Kj·mol-1
B.乙表示恒温恒容条件下发生的可逆反应2NO2![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁是一种性质活泼的金属,请回答下列问题:
(1)甲组同学通过实验探究Mg能否在CO2气体中燃烧,将镁条在空气中点燃后迅速插入盛有CO2气体的集气瓶中,观察到镁条剧烈燃烧,瓶内壁出现黑色固体颗粒等现象。写出Mg在CO2中燃烧的化学方程式:__________
(2)乙组同学根据甲组实验,推测Mg也能在NO2中燃烧,可能产物为MgO 、Mg3N2、和N2。请通过下图所给装置及药品来验证反应产物(夹持装置省略,部分仪器可重复使用)。
已知:a. Mg3N2遇水强烈水解。
b. NO2气体能被NaOH吸收。
c.25℃时,电离常数:CH3COOH的Ka=1.8×10-5 NH3·H2O的Ka=1.8×10-5

回答下列问题:
①乙组同学实验装置连接的正确顺序为A→__________(填装置字母);装置C中盛放的试剂是________。
②当实验过程中出现_________现象时,才能开始加热,确定产物中有N2生成的实验现象为_________。
③装置D中生成两种物质的量相等的钠盐,其离子方程式为___________。
(3)设计实验证明:
①产物中存在Mg3N2:__________________。
②Mg(OH)2与NH4+直接反应而溶解:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com