
����Ŀ��������ʡ������2017�����2����Ӧ�Կ��ԣ�һ������������泥�(NH4)2SO4��FeSO4��6H2O���׳�Ī���Σ���dz��ɫ���壬������ˮ����100����110��ʱ�ֽ⣬���������������еı��Լ���ij��ѧС���Է���мΪԭ����ʵ�����н���ʵ��̽�������Ʊ���������鱗������䴿�ȣ���������:
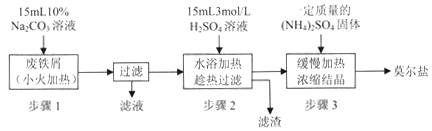
I.�Ʊ����������
��ش��������⣺
(1)����l��������_________���������ӷ���ʽ����Ҫ������˵������
(2)����2������������������Ҳ��˵ȵ���м��ȫ��Ӧ��Ź��ˣ������̺��ĵ�����_______________��
II.�ⶨ��������淋Ĵ���
��ȡmgʵ�����Ʊ��������������Ʒ�����500ml��Һ��ȡ25. 00mL������������Һ����0 . 1mol/L������KMnO4��Һ���еζ������ظ��ζ����Ρ�
(3)����(NH4)2SO4��FeSO4��Һ���õ�����ˮ��ͨ����������һ��ʱ�����ȴ��������ʹ�ã����������ĺô���___________________��
(4)�ζ�ʱ������Ӧ�����ӷ���ʽΪ___________________��
(5)�ζ��յ�ʱ������Ϊ ___________________��
(6)���εζ��������KMnO4��Һ������ƽ��ֵΪVmL���������������Ʒ�Ĵ���Ϊ__________��
(7)��ѧС������������ּ�ⴿ�ȵķ�������ȷ��Ŀǰ��������������Ⱦ�ķ����ж���,��������������һ�ּ�ⷽ��________________��
���𰸡���1��Na2CO3��Һˮ���Լ��Ա��ڳ�ȥ��м��������ۣ�CO32-+H2OHCO3-+OH-
��2���������������Fe2+ˮ�⣬��Ӧδ����ʱ������м�ɷ�ֹFe2+����
��3����ȥˮ�е���������ֹFe2+������
��4��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
��5���������һ��KMnO4��Һʱ����ƿ����Һ��Ϊ��ɫ����30s�ڲ���ȥ
��6��![]() ��100%
��100%
��7��ͨ���ⶨSO42-�����ʵ�����NH4+�����ʵ�����������������淋���
������������м��̼������Һ��ϴ�ӳ�ȥ��������ۣ�С�����������������ϴ����м������ϡ������Һˮԡ���ȡ����ȹ��ˣ��õ���Һ�м���һ��������粒��壬��Һ������־�Ĥʱ��ֹͣ���ȣ�����ʱ��Һ�е��������ӻᱻ���뾧���У��¶ȹ��߾���ֽⱻ������������������ȡ����Ũ������ȴ�ᾧ������ͨ����ѹ����(�����)�ȵõ���Ϊ����ľ��塣
(1)Na2CO3��Һ��CO32-ˮ��CO32-+H2OHCO3-+OH-��ʹNa2CO3��Һ�ʼ��ԣ�Na2CO3����Ҫ�����dz�ȥ��м��������ۣ��ʴ�Ϊ��Na2CO3��Һˮ���Լ��Ա��ڳ�ȥ��м��������ۣ�CO32-+H2OHCO3-+OH-��(2)��������ˮ��ķ���ʽ�ǣ�Fe2++2H2OFe(OH)2+2H+������������Һ�е������ӻ�����Fe2+��ˮ�⣬Fe2+�ױ�����ΪFe3+��������Fe3+��Fe������ӦFe+2Fe3+=3Fe2+����Ӧδ����ʱ������м�ɷ�ֹFe2+������ΪFe3+���ʴ�Ϊ���������������Fe2+ˮ�⣬��Ӧδ����ʱ������м�ɷ�ֹFe2+������(3)ˮ������һ�����������������������ԣ�(NH4)2Fe(SO4)2��Һ�к����������ӣ�Fe2+�ױ�����������(NH4)2Fe(SO4)2��Һ���õ�����ˮ��ͨ����������һ��ʱ�����ȴ��������ʹ�ã����������ɳ�ȥˮ�е���������ֹFe2+���������ʴ�Ϊ����ȥˮ�е���������ֹFe2+��������(4)���������Fe2+�ķ�Ӧ��MnO4-��Mn2+��5e-��Fe2+��Fe3+��e-�����ݵ����غ㣬�����Ӻ���������ǰ��5������ԭ���غ�͵���غ�õ���Ӧ�����ӷ���ʽΪ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O���ʴ�Ϊ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��(5)MnO4-Ϊ��ɫ���ζ��յ�ʱ���������һ�����Ը��������Һ����ɫ����ȥ����Һ����ɫ����ɫ��30s���ޱ仯��˵���ζ����յ㣬�ʴ�Ϊ���������һ��KMnO4��Һʱ����ƿ����Һ��Ϊ��ɫ����30s�ڲ���ȥ��(6)���εζ��������KMnO4��Һ������ƽ��ֵΪVmL������KMnO4�����ʵ���ΪV��10-3L��0.1000molL-1=V��10-4mol��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��n(Fe2+)=5V��10-4mol����(NH4)2SO4FeSO46H2O������Ϊ5V��10-4mol��392g/moL�������������Ʒ�Ĵ���Ϊ![]() ��100%=
��100%=![]() ��100%���ʴ�Ϊ��
��100%���ʴ�Ϊ��![]() ��100%��(7)���������ױ�������ͨ�������������IJⶨ������(NH4)2SO4FeSO46H2O�����ʵ�����ȷ������������Ӳ���������笠���������Һ��Ҳ���ױ�����������ͨ���ⶨ��������ӵ����ʵ�����笠����ӵ����ʵ�����������������淋������ʴ�Ϊ��ͨ���ⶨ��������ӵ����ʵ�����笠����ӵ����ʵ�����������������淋�����
��100%��(7)���������ױ�������ͨ�������������IJⶨ������(NH4)2SO4FeSO46H2O�����ʵ�����ȷ������������Ӳ���������笠���������Һ��Ҳ���ױ�����������ͨ���ⶨ��������ӵ����ʵ�����笠����ӵ����ʵ�����������������淋������ʴ�Ϊ��ͨ���ⶨ��������ӵ����ʵ�����笠����ӵ����ʵ�����������������淋�����
����ʦ��������������Ī���ε��Ʊ�Ϊ���壬��������ˮ�⡢������ԭ��Ӧ��������ԭ��Ӧ�ζ�Ӧ�á����ʷ����ᴿ���й�ʵ������Լ������龳���ۺ�����֪ʶ�������������������Ĺؼ�����˳�������ջ�ѧʵ��Ļ����������״�����(6)�ļ��㡣


 ����ν����Ž̲��㽭���̴�ѧ������ϵ�д�
����ν����Ž̲��㽭���̴�ѧ������ϵ�д� �����Ļ������������������ϵ�д�
�����Ļ������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֡�

��֪A��B��C��D��E��X��Y���ɱ��и���Ԫ����ɵij������ʻ����������ͼ��ʾ��ת����ϵ(����������ͷ�Ӧ��������ȥ)��
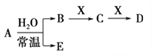
��1��Ԫ�آ������������Ӧˮ����Ļ�ѧʽ��_________________________��
��2��Ԫ�آ���As����Ԫ���У�����̬�⻯����ȶ�����___________���ѧʽ����
��3��Ԫ�آڢޢߵļ����Ӱ뾶�ɴ�С��˳����___________���û�ѧ���ű�ʾ����
��4��Ԫ�آ۵ĵ�����Ԫ�آڵ�����������Ӧ��ˮ���ﷴӦ�����ӷ���ʽ��________________��
��5����AΪ����ɫ���壬��X��D�Ļ�ѧʽ�ֱ�Ϊ___________��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ�Ľ���������������(��Ҫ�ɷ���Al2O3��������SiO2��Fe2O3����)�ǹ�ҵ����ȡ����ԭ�ϡ�ʵ����ģ�ҵ����������Ϊԭ����ȡAl2(SO4)3�����������[NH4Al(SO4)2��12H2O]�Ĺ���������ͼ��ʾ��
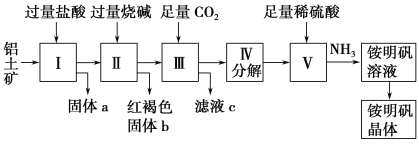
��ش��������⣺
(1)����a�Ļ�ѧʽΪ ������ͨ������CO2���巢����Ӧ�����ӷ���ʽΪ ��
(2)������ȡ�������Һ�Ļ�ѧ����ʽΪ �����������Һ�л������������ʵ���������Ϊ(���������) ����ȴ�ᾧ������ϴ�ӡ�
(3)��1 000 kg��������36%��������Ϊԭ����ȡAl2(SO4)3����������������98%������(�ܶ�1.84 g��cm��1 L(����һλС��)��
(4)��ͬʱ��ȡ���������������ͨ����������������������ֲ�Ʒ�IJ���������ʹ�Ƶõ�������������������ʵ���֮��Ϊ1��1����Ͷ��ʱ�������е�Al2O3��H2SO4�����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2017�챱����������������ѧ����ĩ���ԡ�25��ʱ����10 mL 0.1 mol��L-1 NH4HSO4��Һ����ε���0.1 mol��L-1 NaOH��Һ����Һ��pH��NaOH��Һ�����ϵ����ͼ��ʾ��
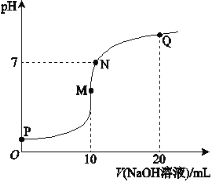
(1)�����뷽��ʽ��ʾP��pH��7��ԭ����________��
(2)M��Q�����У�ˮ�ĵ���̶Ƚϴ����________�㡣
(3)���й�ϵ�У���ȷ����________��
a.M��c(Na+)��c(NH4+)
b.N��c(NH4+)+c(Na+)=2c(SO42-)
c.Q��c(NH4+)+c(NH3��H2O)=c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ���о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죬����������ʵ�飺
��ʵ��ԭ����2KMnO4 + 5H2C2O4 + 3H2SO4 == K2SO4 + 2MnSO4 + 10CO2�� + 8H2O
��ʵ�����ݼ���¼��
ʵ���� | �����£��Թ��������Լ��������� / mL | ��������Һ��ɫ������ɫ����ʱ�� / min | |||
0.6 mol/L H2C2O4��Һ | H2O | 0.2 mol/L KMnO4��Һ | 3 mol/L ϡ���� | ||
1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
��ش�
��1�������ϱ��е�ʵ�����ݣ����Եõ��Ľ����� ��
��2������ʵ��1���ݼ��㣬��KMnO4��Ũ�ȱ仯��ʾ��Ӧ���� v(KMnO4)= ��
��3����С��ͬѧ���ݾ��������n(Mn2+) ��ʱ��仯���Ƶ�ʾ��ͼ����ͼ����ʾ������ͬѧ�������е�ʵ�����Ϸ��֣���ʵ�������n(Mn2+) ��ʱ��仯������Ӧ��ͼ����ʾ�� ��С��ͬѧ����ͼ����ʾ��Ϣ������µļ��裬����������ʵ��̽����
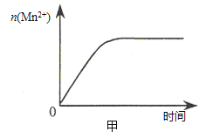
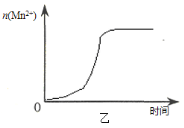
�ٸ�С��ͬѧ����ļ����� ��
�����������С��ͬѧ���ʵ�鷽������ѡ���пհ״�Ӧ��������ʡ�
ʵ���� | �����£��Թ��������Լ��������� / mL | �����Թ��м����������� | ��������Һ��ɫ������ɫ����ʱ�� / min | |||
0.6 mol/L H2C2O4��Һ | H2O | 0.2 mol/L KMnO4��Һ | 3 mol/L ϡ���� | |||
4 | 3.0 | 2.0 | 3.0 | 2.0 |
| |
A��KMnO4 B��H2C2O4 C��K2SO4 D��MnSO4
������С��ͬѧ����ļ��������Ӧ�۲쵽�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס�����Ԫ�������ڱ��е����λ�����±����������ԭ���������3�����һ�ֵ�������Ȼ��Ӳ���������ʣ���������ͬ����Ԫ�أ������ж���ȷ����

A. �����ԣ���>��>��
B. �ҵĵ����ڿ�����ȼ������ֻ�����Ӽ��Ļ�����
C. ԭ�Ӱ뾶����>��>��
D. �������ԭ�Ӻ�����������3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������к�����2017�������ѧ����ĩ���ԡ�һ���¶��£�������Һ������Ũ�ȹ�ϵʽ��ȷ���ǣ� ��
A. pH=5��H2S��Һ�У�c(H+)= c(HS��)=1��10��5 mol��L��1
B. pH=a�İ�ˮ��Һ��ϡ��10������pH=b����a=b+1
C. pH=2��H2C2O4��Һ��pH=12��NaOH��Һ���������ϣ�c(Na��)+ c(H��)= c(OH��)+c( HC2O4��)
D. pH��ͬ����CH3COO Na��NaHCO3��NaClO������Һ��c(Na��)������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���Һ�����Ӵ��ں�ת���ı����������
A����0.lmol/L��pH=l��NaHA ��Һ�м��� NaOH ��Һ��HA-+OH-=A2-+H2O
B����״��������1.12LCO2����ͨ��lL0.lmol/L��NaA1O2��Һ����
CO2+2H2O+A1O2-=A1(OH)3��+HCO3-
C����ˮ�������c(H+)=1��1012mol/L����Һ�п��ܴ�������K+��I-��Mg2+��NO3-
D����NH4A1(SO4)2��Һ�еμ� Ba(OH)2��Һʹ SO42-��ȫ����:
NH4++Al3++2SO42-+2Ba2++4OH-=NH3��H2O+Al(OH)3��+2BaSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50 mL��ʽ�ζ�����ʢ��������Һ��ǡ����a mL�̶ȴ����ѹ���Һ��ȫ��������Ͳ��������Һ������һ�� (����)
A. ����a mL B. ����(50-a)mL C. ����(50-a)mL D. ����a mL
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com