
【题目】碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以纯铜屑为原料制取的流程如下:
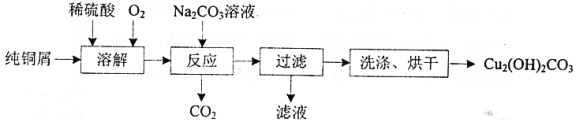
(1)“溶解”步骤反应的离子方程式为_______.温度宜控制在50℃左右,若高于50℃,溶液中O2溶解量减少、Cu的转化率降低,若低于50℃ ,_____
(2)“反应”步骤生成Cu2(OH)2CO3的化学方程式为_________。反应后溶液中铜元素残留量受pH和反应时间的影响如图所示:
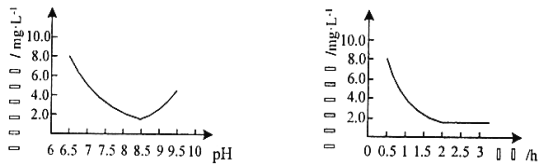
判断反应的最佳条件: pH为___、反应时间为____h。
(3)检验Cu2(OH)2CO3洗涤是否完全的方法是____________________
(4) Cu2(OH)2CO3也可以表示为CuCO3·Cu(OH)2。 查阅文献,上述反应条件下还可能生成少量CuCO3·Cu(OH)2。为测定产品的纯度[产品中Cu2(OH)2CO3的质量分数],取10.97g干燥样品,400℃左右加热,测得固体质量随时间变化关系如图所示。
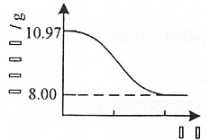
已知: 8.00g固体为黑色纯净物。
有关物质的摩尔质量如表:
物质 | CuCO3·Cu(OH)2 | CuCO3·2Cu(OH)2 | CuO |
摩尔质量/g·mol-1 | 222 | 320 | 80 |
请计算产品的纯度(写出计算过程,结果保留3位有效数字)。______
【答案】2Cu+O2+4H+![]() 2Cu2+ +2H2O 反应(或溶解)速率慢 2CuSO4+2Na2CO3+H2O = Cu2(OH)2CO3↓+2Na2SO4+CO2↑ 8.5 2 取最后一次洗涤的滤液少许于试管中,滴加盐酸酸化的BaCl2溶液[或先加稀盐酸再加BaCl2或Ba(NO3)2溶液],若出现浑浊,则说明Cu2(OH)2CO3未洗涤干净,反之则反 设CuCO3·Cu(OH)2的物质的量为x,杂质CuCO3·2Cu(OH)2的物质的量为y,
2Cu2+ +2H2O 反应(或溶解)速率慢 2CuSO4+2Na2CO3+H2O = Cu2(OH)2CO3↓+2Na2SO4+CO2↑ 8.5 2 取最后一次洗涤的滤液少许于试管中,滴加盐酸酸化的BaCl2溶液[或先加稀盐酸再加BaCl2或Ba(NO3)2溶液],若出现浑浊,则说明Cu2(OH)2CO3未洗涤干净,反之则反 设CuCO3·Cu(OH)2的物质的量为x,杂质CuCO3·2Cu(OH)2的物质的量为y,
依据原样品的质量10.97g,下列等式222 g·mol-1x+320 g·mol-1 y=10.97g①由图像分析出样品最终分解得到CuO8g,![]() ,根据铜元素守恒2x+3y=0.1mol②,联合解等式①②可得:x=0.035mol,y=0.01mol;故
,根据铜元素守恒2x+3y=0.1mol②,联合解等式①②可得:x=0.035mol,y=0.01mol;故![]() ,
,![]()
【解析】
纯铜屑中加入稀硫酸再通入氧气,反应生成了硫酸铜和水,在上述溶液中加入Na2CO3后,通过调节pH值可以让铜离子析出沉淀碱式碳酸铜,同时放出CO2气体,最后经过洗涤,干燥即可得到纯净的碱式碳酸铜,据此进行解题。
(1)据分析可知:“溶解”步骤发生的反应为2Cu+O2+2H2SO4![]() 2CuSO4+2H2O,故其离子方程式为2Cu+O2+4H+
2CuSO4+2H2O,故其离子方程式为2Cu+O2+4H+![]() 2Cu2++2H2O,温度宜控制在50℃左右,若高于50℃,溶液中O2溶解量减少、Cu的转化率降低,若低于50℃,温度太低,当然是反应速率减慢,影响实验的效率,故答案为:2Cu+O2+4H+
2Cu2++2H2O,温度宜控制在50℃左右,若高于50℃,溶液中O2溶解量减少、Cu的转化率降低,若低于50℃,温度太低,当然是反应速率减慢,影响实验的效率,故答案为:2Cu+O2+4H+![]() 2Cu2++2H2O;反应(或溶解)速率慢;
2Cu2++2H2O;反应(或溶解)速率慢;
(2)根据流程图中可知:“反应”步骤是由CuSO4溶液和Na2CO3反应生成Cu2(OH)2CO3同时放出CO2,故化学方程式为2CuSO4+2Na2CO3+H2O = Cu2(OH)2CO3↓+2Na2SO4+CO2↑,据左图可知pH等于8.5时铜的残留量最小,说明铜离子沉淀得最完全,据右图可知,当时间进行到2小时左右时,铜得残留量达到最低,再往后虽然略有下降,但很不明显,且浪费时间,故答案为:2CuSO4+2Na2CO3+H2O = Cu2(OH)2CO3↓+2Na2SO4+CO2↑;8.5;2;
(3)检验Cu2(OH)2CO3洗涤主要除去表面得杂质Na2SO4等,但是碱式硫酸铜也会极少数溶解,故要想检验是否完全洗涤干净,需检验最后一次洗涤液中是否有![]() ,由于有
,由于有![]() 的影响,故最后得检验方法为取最后一次洗涤的滤液少许于试管中,滴加盐酸酸化的BaCl2溶液[或先加稀盐酸再加BaCl2或Ba(NO3)2溶液],若出现浑浊,则说明Cu2(OH)2CO3未洗涤干净,反之则反;
的影响,故最后得检验方法为取最后一次洗涤的滤液少许于试管中,滴加盐酸酸化的BaCl2溶液[或先加稀盐酸再加BaCl2或Ba(NO3)2溶液],若出现浑浊,则说明Cu2(OH)2CO3未洗涤干净,反之则反;
(4) 设CuCO3·Cu(OH)2的物质的量为x,杂质CuCO3·2Cu(OH)2的物质的量为y,
依据原样品的质量10.97g,下列等式222 g·mol-1x+320 g·mol-1y=10.97g①由图像分析出样品最终分解得到CuO8g,![]()
![]() ,
,![]() ,故答案为:设CuCO3·Cu(OH)2的物质的量为x,杂质CuCO3·2Cu(OH)2的物质的量为y,
,故答案为:设CuCO3·Cu(OH)2的物质的量为x,杂质CuCO3·2Cu(OH)2的物质的量为y,
依据原样品的质量10.97g,下列等式222 g·mol-1x+320 g·mol-1y=10.97g①由图像分析出样品最终分解得到CuO8g,![]() ,根据铜元素守恒2x+3y=0.1mol②,联合解等式①②可得:x=0.035mol,y=0.01mol;故
,根据铜元素守恒2x+3y=0.1mol②,联合解等式①②可得:x=0.035mol,y=0.01mol;故![]() ,
,![]()


科目:高中化学 来源: 题型:
【题目】下列实验现象与实验操作不相匹配的是( )
A.将镁条点燃后迅速伸入集满![]() 的集气瓶,集气瓶中产生浓烟并有黑色颗粒产生
的集气瓶,集气瓶中产生浓烟并有黑色颗粒产生
B.向盛有![]() 溶液的试管中加过量铁粉,充分振荡后加1滴
溶液的试管中加过量铁粉,充分振荡后加1滴![]() 溶液,黄色逐渐消失,再加
溶液,黄色逐渐消失,再加![]() 后溶液颜色不变
后溶液颜色不变
C.将![]() 溶液加入
溶液加入![]() 溶液中,有白色沉淀生成,
溶液中,有白色沉淀生成,![]() 结合
结合![]() 的能力强于
的能力强于![]()
D.制取较高浓度的次氯酸溶液,将![]() 通入碳酸钠溶液中
通入碳酸钠溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇及其化合物可制成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的烯丙醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
①基态镍原子的价电子排布图为________。
②1 mol CH2=CH-CH2OH含有σ键的数目为________,烯丙醇分子中碳原子的杂化类型为___。
③Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2- 和[Ni(SCN)2]- 等,与CN-互为等电子体的阴离子为_____。
(2)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
①CaC2中C22-中碳与碳之间存在碳碳三键,C22-与O22+互为等电子体,O22+的电子式可表示为_______。
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中σ键和π键数目比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可燃冰主要含有甲烷水合物(CH4·nH2O),还含少量CO2等物质。
(1)可燃冰中,CH4分子的空间构型为_______,CO2的电子式为________
(2)工业利用甲烷制氢气,化学方程式为CH4(g) + H2O(g)CO(g) + 3H2(g)
①下列措施能加快反应速率的是_______
a.降低温度 b.增加CH4浓度 c.使用催化剂
②若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是______
a.c(H2) = 3c(H2O) b.混合气体的质量不再变化 c.单位时间内生成1 mol CO,同时消耗3 mol H2
(3)某种甲烷燃料电池工作原理如图所示:
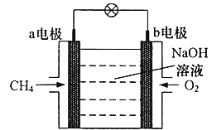
①电子移动方向为________,(填“a→b"或“b→a")
②b电极的电极反应式为____________。
(4)甲烷可催化还原NO,反应历程如图所示:

①该历程中,反应i为CH4+ 12Fe2O3=8Fe3O4+CO2+2H2O,
则反应ii的化学方程式为____________
②工业上催化还原2molNO,理论上需要______LCH4 (标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.工业以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:
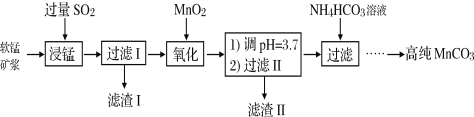
(1)浸锰过程中Fe2O3与SO2反应的离子方程式为Fe2O3+SO2+2H+=2Fe2++SO42-+H2O,该反应是经历以下两步反应实现的。
ⅰ:Fe2O3+6H+ =2Fe3++3H2O
ⅱ:____________________________________________(离子方程式)。
(2)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为____________(填离子符号)。
(3)氧化过程中被MnO2氧化的物质有(写化学式):____________________。
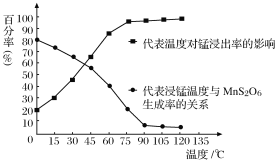
(4) “浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是_________;向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度不宜太高的原因是______________________。
(5).加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:_______________________________________________________。
Ⅱ.重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
酸性条件下,六价铬主要以Cr2O72-形式存在,工业上常用电解法处理含Cr2O72-的废水。实验室用如图装置模拟处理含Cr2O72-废水,阳极反应式Fe-2e-=Fe2+,阴极反应式2H++2e-=H2↑随着电解进行,阴极附近pH升高。
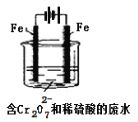
(1)电解时能否用Cu电极来代替Fe电极?____(填“能”或“不能”),理由是______________________。
(2)电解时阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式为______________________________。
(3)上述反应得到的金属阳离子在阴极区可沉淀完全,从其对水的电离平衡影响角度解释其原因__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在体积可变的容器中发生反应:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(l),改变起始时加入各物质的量,在不同压强下达平衡时CH3OCH3(g)的物质的量如表所示,下列说法错误的是( )
CH3OCH3(g)+3H2O(l),改变起始时加入各物质的量,在不同压强下达平衡时CH3OCH3(g)的物质的量如表所示,下列说法错误的是( )
压强 | P1 | P2 | P3 | |
n/mol | ①2.0molCO2 6.0molH2 | 0.10mol | 0.04mol | 0.02mol |
②1.0molCO2 3.0molH2 | x 1 | y 1 | z 1 | |
③1.0molCH3OCH3 3.0molH2O | x 2 | y 2 | z 2 | |
A.P1>P2B.x 1=0.05
C.P2条件下,③中CH3OCH3平衡转化率为96%D.若该反应可自发进行,则高温更有利
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家研制的一种新型“微生物电池”可以将污水中的有机物转化为H2O和CO2,同时产生电能,其原理示意如图。下列有关该电池的说法正确的是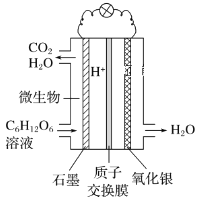
A.氧化银电极上的反应为Ag2O+2e-=2Ag+O2-
B.石墨电极上的反应为C6H12O6+6H2O-24e-=6CO2↑+24H+
C.每转移4 mol电子,石墨电极产生22.4 L CO2气体
D.每30 g C6H12O6参与反应,有4 mol H+经质子交换膜进入负极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体[CH3CH(OH)COO]2Fe·3H2O,相对分子质量为288;易溶于水,是一种很好的补铁剂,可由乳酸[CH3 CH(OH)COOH]与FeCO3反应制得。
I.碳酸亚铁的制备(装置如图所示)
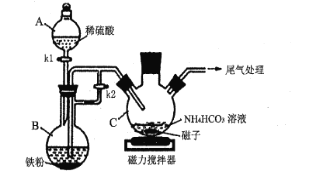
(1)仪器C的名称是____;实验操作如下:打开kl、k2,加入适量稀硫酸,关闭kl,使反应进行一段时间,其目的是____。
(2)接下来关闭k2使仪器C中的制备反应发生,其反应的离子方程式为__。
Ⅱ.乳酸亚铁的制备及铁元素含量测定
(3) 仪器C中混合物经过滤、洗涤得到FeCO3沉淀,检验其是否洗净的方法是____。
向纯净FeCO3固体中加入足量乳酸溶液,在75℃下搅拌使之充分反应,经过滤,在隔绝空气的条件下,经低温蒸发等操作后,获得乳酸亚铁晶体。
(4)两位同学分别用不同的方案进行铁元素含量测定:
①甲同学通过KMnO4滴定法测定样品中Fe2+的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于l00%,其原因可能是 ___。
②乙同学经查阅资料后改用碘量法测定铁元素的含量计算样品纯度。称取3.000g样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成l00mL溶液。吸取25.00 rnL该溶液加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0. 100 mol.L-1硫代硫酸钠溶液滴定(已知:I2+2S2O32-=S4O62-+2I-),当溶液____,即为滴定终点;平行滴定3次,硫代硫酸钠溶液的平均用量为23. 80 mL,则样品纯度为____%(保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知阴离子交换膜只允许阴离子通过。某化学课外活动小组采用如下方案对印刷电路废液(溶质主要是FeCl2、CuCl2和 FeCl3)进行再生,先向废液中加入过量铁粉,充分反应后过滤,再将滤液转入下图所示的装置中进行电解。下列说法中不正确的是
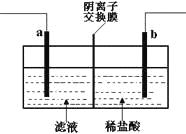
A.电解时,电极a应与外电源的正极相连
B.电解时,电极b周围产生无色无味的气体
C.电解时,电极a发生的反应是:2Cl--2e-=Cl2↑
D.电解时,可以用氯化钠溶液替代稀盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com