
【题目】将3.64 g Fe2O3和Al2O3的混合物溶于200 mL 0.1 mol/L盐酸中(盐酸过量),再向该溶液中加入NaOH溶液使Fe3+和Al3+恰好完全沉淀,用去NaOH溶液100 mL。则NaOH溶液的物质的量浓度是( )
A. 0.1 mol/L B. 0.2 mol/L C. 0.4 mol/L D. 0.8 mol/L
【答案】B
【解析】
反应生成硫酸铝、硫酸铁,盐酸有剩余,向反应后的混合溶液中加入10 mL NaOH溶液,恰好使Fe3+、Al3+完全沉淀,此时溶液中溶质为NaCl,根据钠离子守恒有n(NaOH)=n(NaCl),根据氯离子守恒有n(NaCl)=n(HCl),据此计算n(NaOH),再根据c=![]() 来分析计算。
来分析计算。
盐酸的浓度为0.1 mol/L,体积为0.2L,则其中氯离子的物质的量为0.02mol.
Fe2O3、Al2O3与硫酸反应生成硫酸铝、硫酸铁,硫酸有剩余,向反应后的混合溶液中加入10 mL NaOH溶液,恰好使Fe3+、Al3+完全沉淀,此时溶液中溶质为NaCl,
根据氯离子守恒有n(NaCl) = n(HCl) = 0.2 L×0.1 mol/L = 0.02 mol,
根据钠离子守恒可得:n(NaOH) = n(NaCl) = 0.02 mol,则该c(NaOH) = ![]() = 0.2 mol/L,
= 0.2 mol/L,
答案选B。


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】资源化利用CO2,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
(1)CO2的捕集:
①写出CO2的电子式__________。
②用饱和Na2CO3溶液做吸收剂可“捕集”CO2。若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式___________。
③聚合离子液体是目前广泛研究的CO2 吸附剂。结合下图分析聚合离子液体吸附CO2的有利条件是__________。

(2)生产尿素:
工业上以CO2、NH3为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步:2NH3(g)+CO2(g)![]() H2NCOONH4(s) △H =-159.5 kJ/mol
H2NCOONH4(s) △H =-159.5 kJ/mol
第二步:H2NCOONH4(s)![]() CO(NH2)2(s)+ H2O(g) △H =+116.5 kJ/mol
CO(NH2)2(s)+ H2O(g) △H =+116.5 kJ/mol
①写出上述合成尿素的热化学方程式_________。
②某实验小组模拟工业上合成尿素,在一定体积的密闭容器中投入4mol NH3和1mol CO2,实验测得反应中各组分物质的量随时间的变化如图所示:

已知总反应的快慢由慢的一步反应决定,则合成尿素总反应的快慢由第______步反应决定,总反应进行到________min时到达平衡。
(3)合成乙酸:
①中国科学家首次以CH3OH、CO2和H2为原料高效合成乙酸,其反应路径如图所示:

原料中的CH3OH可通过电解法由CO2制取,用稀硫酸作电解质溶液,写出生成CH3OH的电极反应式___。
②根据图示,写出总反应的化学方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
元素 | A | B | C | D |
性质结构信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(1)写出B原子的电子排布式__________
(2)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为__________,简要描述该配合物中化学键的成键情况:__________
(3)“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。

则在以上分子中,中心原子采用sp3杂化形成化学键的是__________(填序号);在②的分子中有__________个σ键和__________个π键
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:
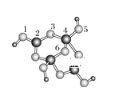
在Xm-中,硼原子轨道的杂化类型有__________;配位键存在于__________原子之间(填原子的数字标号);m=__________(填数字)
(5)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的化学式为__________,第二种配合物的化学式为_________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时,将n mol·L-1氨水滴入10 mL 1.0 mol·L-1 盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是

A. a点KW=1.0×10-14
B. b点:c(NH)>c(Cl-)>c(H+)>c(OH-)
C. 25 ℃时,NH4Cl水解常数为(n-1)×10-7(用n表示)
D. d点水的电离程度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
A. 0.1mol![]() 和0.1mol
和0.1mol![]() 于密闭容器中充分反应,反应后分子总数为0.2
于密闭容器中充分反应,反应后分子总数为0.2![]()
B. 向过氧化钠中通入足量的二氧化碳,当固体增重28g,转移电子数为l![]()
C. 在标准状况下,22.4LHF与![]() 个
个![]() 中含有的电子数相同
中含有的电子数相同
D. 含有![]() 个
个![]() 胶粒的氢氧化铁胶体中,铁元素的质量大于56g
胶粒的氢氧化铁胶体中,铁元素的质量大于56g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,有①6.72LCH4,②3.01×1023个HCl,③13.6gH2S ,④0.2molNH3,则下列四种气体的关系表示正确的是()
A. 体积:④<①<②<③ B. 密度:①<③<④<②
C. 质量:④<①<③<② D. 氢原子数:②<③<④<①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是( )
A.NaOH电离方程式:NaOH=Na++H++O2-
B.硫酸铝的电离方程式:Al2(SO4)3=Al23++(SO4)32-
C.NaCl的电离方程式:NaCl![]() Na++Cl-
Na++Cl-
D.硫酸氢铵电离方程式:NH4HSO4 =NH4++H++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是研究铁钉腐蚀的装置图,下列说法不正确的是
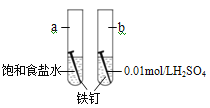
A. 铁钉在两处的腐蚀速率:a < b
B. a、b两处铁钉中碳均正极
C. a、b两处铁钉中的铁均失电子被氧化
D. a、b两处的正极反应式均为O2+4e-+4H+===2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaCN溶液中CN-水解常数![]() 是NaCN溶液的起始浓度]。25℃时,向c0的NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lgc0与2pOH[pOH-=-lg c(OH-)]的关系如图。
是NaCN溶液的起始浓度]。25℃时,向c0的NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lgc0与2pOH[pOH-=-lg c(OH-)]的关系如图。

下列说法不正确的是
A. 其它条件不变,降低温度,可使b点变到a点
B. 相同温度时,c点对应溶液中的pH大于a点
C. 由图可知,25 ℃时,Kh(CN-)≈10-4.7
D. 向1 L lgc0=0的NaCN溶液中通入0.5 mol HCl气体,所得溶液中c(CN-)<c(HCN)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com