
【题目】已知可逆反应X(g)+2Y(g)![]() Z(g) ΔH <0,一定温度下,在体积为2 L的密闭容器中加入4 mol Y和一定量的X后,X的浓度随时间的变化情况如图所示,则下列说法正确的是( )
Z(g) ΔH <0,一定温度下,在体积为2 L的密闭容器中加入4 mol Y和一定量的X后,X的浓度随时间的变化情况如图所示,则下列说法正确的是( )

A. 若向该容器中加入1molX、2molY,达平衡时,X的平衡浓度小于0.125mol/L
B. a点正反应速率大于逆反应速率
C. 反应达平衡时,降低温度可以实现c到d的转化
D. 该条件下,反应达平衡时,平衡常数K=3
【答案】B
【解析】
试题A.根据图像可知,在反应开始时加入2molX 、4molY,二者的物质的量的比是1:2,若向该容器中加入1molX、2molY,二者的物质的量的比也是1:2,该反应是反应前后气体体积相等的反应,所以改变压强,化学平衡不发生移动,则当达到平衡时X的浓度是原来的1/2,c(X)=0.125mol/L,错误;B.根据题意可知反应从正反应方向开始,到c点时达到化学化学平衡,此时正反应速率与逆反应速率相等,所以在达到平衡前的a点,正反应速率大于逆反应速率,正确;C.反应达平衡时,降低温度化学平衡向放热的正反应方向移动,反应物的浓度会降低,所以不可能实现c到d的转化,错误;D.该条件下,反应达平衡时,平衡常数,各种物质的浓度分别是c(X)=0.25mol/L,c(Y)=0.5mol/L,c(Z)=0.75mol/L,所以该反应的化学平衡常数K= c(Z)÷[c(X)×c2(Y)]= 0.75÷[0.25×0.52]=12,错误。


 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】下列有关组成细胞化学元素的叙述,正确的是( )
A. 组成细胞最基本的元素是氮
B. 活细胞内含量最高的元素是氧
C. Mg、Zn、Ca等大量元素是生物体必不可少的
D. 微量元素对于生物体来说可有可无
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处于另一周期。C、B可按原子个数比2∶1和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。D的周期序数等于D原子最外层电子数。E原子半径是同周期中最小的(除稀有气体外)。根据以上信息回答下列问题:
(1)A、B、C、D、E五种元素的原子半径由小到大的顺序是__________________ (用元素符号填写),其中D的最高价氧化物是________氧化物(填“酸性”“碱性”或“两性”)。
(2)乙物质中存在的化学键类型是________。
(3)化合物乙的电子式为________。
(4)写出C与D分别对应的最高价氧化物的水化物反应的离子方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述能说明反应2A(g)+B(g)![]() 2C(g)已达平衡状态的有( )
2C(g)已达平衡状态的有( )
①A、B、C的百分含量相等;
②单位时间,消耗a mol B,同时生成2a mol C;
③单位时间,消耗a mol A,同时生成0.5a mol B;
④外界条件不变时,物质总质量不随时间改变;
⑤外界条件不变时,气体总分子数不再变化;
⑥A、B、C分子数之比为2:1:2.
A.除④外 B.除②⑥外 C.②④⑤ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡。六种元素的原子半径与原子序数的关系如图所示。下列推断正确的是

A. 最简单氢化物的沸点排序:Y>T>R
B. 原子半径和离子半径均满足:Y<Z
C. 最高价氧化物对应的水化物的酸性:T<R
D. 单质氧化性:Y>R>T
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示转化关系,且ΔH=ΔH1+ΔH2,则X、Y可能是
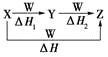
①C、CO ②S、SO2③AlCl3、Al(OH)3④Na2CO3、NaHCO3⑤Fe、FeCl2
A. ①②③④⑤B. ②④⑤
C. ①③④D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com