
【题目】菠萝酯是一种带有浓郁的菠萝香气和香味的食用香料,其合成路线如下(部分反应条件及产物已略去):

请回答下列问题:
(1) A可用于制备顺丁橡胶(顺式聚1,3-丁二烯),顺丁橡胶的结构简式为_________,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为__________。
(2) F的结构简式为__________,反应④的条件是________________。
(3) ①一⑥反应中属于取代反应的是__________。
(4) 下列有关B的说法正确的是__________(填字母序号)。
a. 元素分析仪可确定B的实验式为C6H10
b. 质谱仪可检测B的最大质荷比的数值为82
c. 红外光谱仪可测定B中六个碳原子一定在同一平面上
d. 核磁共振仪可测定B有两种类型氢原子吸收峰
(5) 写出反应③的化学方程式_________________。
(6) 同时满足下列条件的E的同分异构体的数目为__________种。
①遇氯化铁溶液显紫色 ②苯环上只有2个取代基且处于对位
(7) 参照上述合成路线,现仅以A为有机原料,无机试剂任选,设计制备![]() 的合成路线。
的合成路线。
已知:①反应物分子的环外双键比环内双键更容易被氧化;
②![]() (R,R’代表烃基或氢)
(R,R’代表烃基或氢)
___________________________________________ 。
【答案】![]() 10002CH2=CH-CH2-OHCu/O2 加热③⑥b
10002CH2=CH-CH2-OHCu/O2 加热③⑥b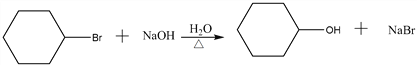 12
12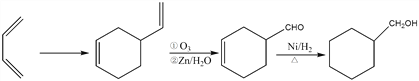
【解析】
试题分析:A可用于制备顺丁橡胶(顺式聚1,3-丁二烯),所以A为1,3-丁二烯,1,3-丁二烯与乙烯发生加成反应生成环己烯,环己烯与HBr发生加成反应生成C为![]() ,C发生水解反应生成D为
,C发生水解反应生成D为![]() ,环己醇发生氧化反应生成
,环己醇发生氧化反应生成![]() ,
,![]() 与CH2=CH-CN发生加成反应生成E,比较菠萝酯和
与CH2=CH-CN发生加成反应生成E,比较菠萝酯和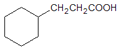 的结构简式可知,
的结构简式可知, 与F为CH2=CHCH2OH发生酯化反应得到菠萝酯,据此答题。
与F为CH2=CHCH2OH发生酯化反应得到菠萝酯,据此答题。
解析:A可用于制备顺丁橡胶(顺式聚1,3-丁二烯),所以A为1,3-丁二烯,1,3-丁二烯与乙烯发生加成反应生成环己烯,环己烯与HBr发生加成反应生成C为![]() ,C发生水解反应生成D为
,C发生水解反应生成D为![]() ,环己醇发生氧化反应生成
,环己醇发生氧化反应生成![]() ,
,![]() 与CH2=CH-CN发生加成反应生成E,比较菠萝酯和
与CH2=CH-CN发生加成反应生成E,比较菠萝酯和 的结构简式可知,
的结构简式可知, 与F为CH2=CHCH2OH发生酯化反应得到菠萝酯,则
与F为CH2=CHCH2OH发生酯化反应得到菠萝酯,则
(1)顺丁橡胶的链节为![]() ,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为 540108÷54=10002;
,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为 540108÷54=10002;
(2)根据上面的分析可知,F的结构简式为 CH2=CH-CH2-OH,反应④为环己醇发生氧化反应,反应的条件是Cu/O2 加热 ;
(3)根据上面的分析可知,①一⑥反应中属于取代反应的是③⑥;
(4)B为![]() ,a.元素分析仪测定元素种类,不能进行定量分析,B的实验式为C3H5,a错误;b.B的相对分子质量为82,故B的最大质荷比的数值为82,b正确;c.红外光谱仪可测定原子团或官能团,不能测定空间构型,c错误;d.分子中含有3种化学环境不同的H原子,核磁共振仪可测定B有3种类型氢原子吸收峰,d错误,答案选b;
,a.元素分析仪测定元素种类,不能进行定量分析,B的实验式为C3H5,a错误;b.B的相对分子质量为82,故B的最大质荷比的数值为82,b正确;c.红外光谱仪可测定原子团或官能团,不能测定空间构型,c错误;d.分子中含有3种化学环境不同的H原子,核磁共振仪可测定B有3种类型氢原子吸收峰,d错误,答案选b;
(5)反应③为![]() 的碱性水解,反应的化学方程式为
的碱性水解,反应的化学方程式为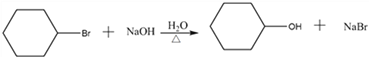 ;
;
(6)根据条件①遇氯化铁溶液显紫色,说明有酚羟基,②苯环上只有2个取代基且处于对位,结合E的结构简式可知,符合条件的结构为苯环上连有-OH、-CH2CH2CH2NH2,或-OH、-CH2CH(NH2)CH3,或-OH、-CH(NH2)CH2CH3,或-OH、-CH(CH3)CH2NH2,或-OH、-CNH2(CH3)2,或-OH、-CH2CH2NHCH3 ,或-OH、-CH2NHCH2CH3 ,或-OH、-NHCH2CH2CH3 ,或-OH、-CH2N(CH3)2,或-OH、-CH(CH3)NHCH3,或-OH、-NHCH(CH3)2,或-OH、-N(CH3)CH2CH3,共12种;
(7)A为1,3-丁二烯,以1,3-丁二烯为有机原料制备![]() ,可以用两分子A发生加成反应生成
,可以用两分子A发生加成反应生成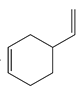 ,
, 发生信息②中反应生成
发生信息②中反应生成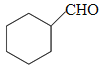 ,
, 与氢气发生全加成反应生成
与氢气发生全加成反应生成![]() ,因此反应的合成路线为
,因此反应的合成路线为 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 钠与水反应:Na+H2O= Na++OH-+H2↑
B. 铁与硫酸铁溶液反应:Fe+Fe3+ = 2Fe2+
C. 氢氧化镁与稀盐酸反应:Mg(OH)2+2 H+ = Mg2++2H2O
D. 碳酸氢钠溶液中滴入氢氧化钠溶液:OH —+HCO3-= H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;④KNO3,铜粉可溶解的是
A. ①② B. ②④ C. ②③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将MnO2与FeSO4溶液、硫酸充分反应后过滤,将滤液加热至60℃后,再加入Na2CO3溶液,最终可制得碱式碳酸锰[aMnCO3·bMn(OH)2·cH2O]。
(1)用废铁屑与硫酸反应制备FeSO4溶液时,所用铁屑需比理论值略高,原因是 ,反应前需将废铁屑用热Na2CO3溶液浸泡,其目的是 。
(2)为测定碱式碳酸锰组成,取7.390 g样品溶于硫酸,生成CO2 224.0 mL(标准状况),并配成500 mL溶液。准确量取10.00 mL该溶液,用0.0500 mol·L-1 EDTA(化学式Na2H2Y)标准溶液滴定其中的Mn2+(原理为Mn2+ +H2Y2-=MnY2-+2H+),至终点时消耗EDTA标准溶液28.00 mL。通过计算确定该样品的化学式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下将1molCO和1molH2O (g)通入一个密闭容器中反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),达到平衡后CO2的物质的量为0.67mol,再通入4molH2O (g)达到平衡后CO2的物质的量可能是( )
CO2(g)+H2(g),达到平衡后CO2的物质的量为0.67mol,再通入4molH2O (g)达到平衡后CO2的物质的量可能是( )
A. 等于0.6mol B. 等于lmol C. 大于lmol D. 等于0.94mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某充电电池如图所示,已知a、b为惰性电极,溶液呈酸性,充电时左槽溶液颜色由蓝色变为黄色。下列叙述正确的是( )

A. 放电时,a极是电池的负极 B. 充电时,a极的电极反应式为:VO2++2H++e-=VO2++H2O
C. 氧化性VO2+>V3+ D. 放电时,H+从左槽迁移进右槽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的s电子数比p电子数多3个,Y、Z均位于第二周期且两元素最外层电子数之和为11, Z、R同主族,M核外电子有26种运动状态,请回答下列问题:
(1)化合物XCl3中心原子的杂化轨道类型为_______;RC12的立体构型为________。
(2)H2Z、H2R的沸点分别为100℃、-60.4℃,试解释其原因:______________。
(3)R、M形成的一种化合物晶胞如图所示。

① 该化合物的化学式为________;
② 若晶胞参数为a pm。列式计算该晶胞的密度ρ=_______g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:4Na+3CO2 = 2Na2CO3+C。下列说法错误的是

A. 电池工作温度可能在200℃以上
B. 该装置可以将化学能转化为电能
C. 放电时,Na+向正极移动
D. 放电时,正极的电极反应为:4Na++3CO2+4e-=2Na2CO3+C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com