
【题目】二氧化氯(ClO2)是一种高效消毒剂,易溶于水,沸点为11.0℃,极易爆炸分解,若用空气、二氧化碳、氮气等惰性气体稀释时,爆炸性则降低。用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如图:

(1)仪器a的名称为___________,装置A中反应的离子方程式为____________________。
(2)试剂X的作用是_____________________________。
(3)装置D中通入干燥空气的作用是______________________________。
(4)该实验装置的缺陷是_____________________________。
【答案】圆底烧瓶 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 吸收HCl 稀释降低二氧化氯的浓度,减少其爆炸的可能性 装置E没有采取防倒吸措施;装置D和E之间缺少干燥装置
Mn2++Cl2↑+2H2O 吸收HCl 稀释降低二氧化氯的浓度,减少其爆炸的可能性 装置E没有采取防倒吸措施;装置D和E之间缺少干燥装置
【解析】
由实验装置图可知,装置A中中二氧化锰和浓盐酸共热制备氯气,氯气中混有挥发出的氯化氢气体,装置B中盛有的饱和食盐水能除去氯气中混有的氯化氢,装置C中盛有浓硫酸的目的是干燥氯气,装置D中氯气与固体亚氯酸钠在冰水浴条件下制备二氧化氯,装置E中氢氧化钠溶液用于吸收过量的氯气和挥发出的二氧化氯,防止污染环境。
(1)仪器a的名称为圆底烧瓶;装置A中二氧化锰和浓盐酸共热反应生成氯化锰、氯气和水,反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,故答案为:圆底烧瓶;MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:圆底烧瓶;MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)浓盐酸具有挥发性,装置A中制取的氯气中混有氯化氢气体,装置B中盛有的试剂X饱和食盐水,目的是吸收除去氯气中混有的氯化氢气体,故答案为:吸收HCl;
(3)由题意可知,二氧化氯极易爆炸分解,若用空气、二氧化碳、氮气等惰性气体稀释时,爆炸性则降低,则向装置D中通入干燥空气能稀释降低二氧化氯的浓度,减少其爆炸的可能性,故答案为:稀释降低二氧化氯的浓度,减少其爆炸的可能性;
(4)由题意可知,二氧化氯气体易溶于水,可能溶于氢氧化钠溶液中挥发出的水蒸气,应在装置D和E之间添加干燥装置,防止二氧化氯溶于水;氯气和二氧化氯能与氢氧化钠溶液反应,若直接通入氢氧化钠溶液会产生倒吸,为防止倒吸,应在装置E中采取防倒吸措施,故答案为:装置E没有采取防倒吸措施;装置D和E之间缺少干燥装置。


科目:高中化学 来源: 题型:
【题目】某温度下,在2 L恒容密闭容器中投入一定量的A、B,发生反应:3A(g)+bB(g)![]() cC(g)+2D(s),12 s时生成C的物质的量为0.8 mol(反应进程如图所示)。下列说法中正确的是
cC(g)+2D(s),12 s时生成C的物质的量为0.8 mol(反应进程如图所示)。下列说法中正确的是

A.图中两曲线相交时,A的消耗速率等于A的生成速率
B.0-2 s,D的平均反应速率为0.1 mol·L-1·s-1
C.化学计量系数之比b:c=1:4
D.12 s时,A的转化率为75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色透明的溶液中: Fe3+、Mg2+、SCN 、Cl
B.![]() =1×10-12的溶液中:K+、Na+、CO32、NO3
=1×10-12的溶液中:K+、Na+、CO32、NO3
C.![]() 的溶液中: K+、NH4+、MnO4、SO42-
的溶液中: K+、NH4+、MnO4、SO42-
D.能使甲基橙变红的溶液中: Na+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期主族元素原子半径与原子序数的关系图。下列说法正确的是( )
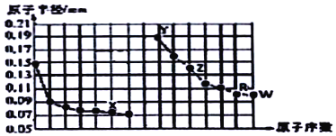
A.X所在主族中,X的简单氢化物分子间存在氢键,所以其氢化物稳定性最强
B.R简单氢化物的酸性弱于W简单氢化物,故元素非金属性R小于W
C.在同周期中,W的含氧酸酸性最强
D.Y的氢化物可以与水反应,产生一种单质气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措施之一。
(1)将硫酸锰、硝酸钇与氢氧化钠溶液按一定比例混合,搅拌使其充分反应,可获得一种砷的高效吸附剂X,吸附剂X中含有CO32-,其原因是____。
(2)H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1和图2所示。


①以酚酞为指示剂(变色范围pH8.0~10.0),将NaOH溶液逐滴加入H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为____。
②H3AsO4第一步电离方程式H3AsO4![]() H2AsO4-+H+的电离常数为Ka1,则pKa1=___(pKa1=-lgKa1)。
H2AsO4-+H+的电离常数为Ka1,则pKa1=___(pKa1=-lgKa1)。
(3)溶液的pH对吸附剂X表面所带电荷有影响。pH=7.1时,吸附剂X表面不带电荷;pH>7.1时带负电荷,pH越高,表面所带负电荷越多;pH<7.1时带正电荷,pH越低,表面所带正电荷越多。pH不同时吸附剂X对三价砷和五价砷的平衡吸附量(吸附达平衡时单位质量吸附剂X吸附砷的质量)如图3所示。

①在pH7~9之间,吸附剂X对五价砷的平衡吸附量随pH升高而迅速下降,其原因是___。
②吸附剂X对水中三价砷的去除能力远比五价砷的弱,这是因为___,提高吸附剂X对三价砷去除效果可采取的措施是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。
⑴甲醇脱氢法可制备甲醛,反应方程式为CH3OH![]() HCHO+H2。
HCHO+H2。
①发生反应时的过程如图所示,从热效应角度判断,可知该反应为______反应。

②下列方法中能减慢反应速率的是______(填字母)。
a.使用催化剂 b.升高温度 c.降低反应物浓度
③使用催化剂________(填“能”或“不能”)使反应物的转化率达到100%。
⑵甲醛超标会危害人体健康,需对甲醛含量检测及处理。
①某甲醛气体探测仪利用燃料电池工作原理,其结构如图所示。电极a为______(填“正”或“负”)极,在电极b上发生的反应类型为______反应。(填“氧化”或“还原”)

②探测仪工作时,电子从______极流出(填“a”或“b”),总反应方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为短周期元素,X的一种核素的质子数为8;Y和Ne原子的核外电子数相差1;Z的单质是一种常见的半导体材料;W的非金属性在同周期元素中最强。其原子半径随原子序数变化如图所示。
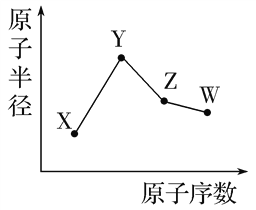
下列说法正确的是
A.对应简单离子半径:W>Y>X
B.对应气态氢化物的稳定性:Z>W
C.化合物YWX中既含离子键,又含共价键
D.Z的氧化物能与W的气态氢化物、Y的最高价氧化物对应水化物的溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与应叙述相符的是
A.图1表示向![]() 氯水中逐滴加入
氯水中逐滴加入![]() 醋酸,溶液导电性随加入酸体积的变化
醋酸,溶液导电性随加入酸体积的变化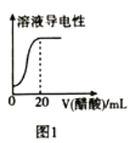
B.图2表示酸性介质![]() 原电池反应过程中的电流强度的变化,T时可能加入了
原电池反应过程中的电流强度的变化,T时可能加入了![]()
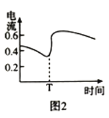
C.图3表示SO2与![]() 反应过程中的能量变化,其中
反应过程中的能量变化,其中![]()

D.图4表示在饱和![]() 溶液中逐步加
溶液中逐步加![]() 固体后,溶液中
固体后,溶液中![]()
![]() 的浓度变化
的浓度变化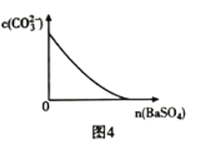
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置的叙述,正确的是( )
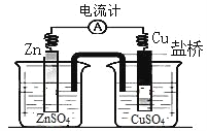
A.铜做正极,铜片上有气泡产生
B.盐桥中的阴离子会移向 CuSO4 溶液
C.正极附近的 SO![]() 浓度逐渐增大
浓度逐渐增大
D.锌片表面被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com