
【题目】六苯乙烷为无色晶体,其结构如图所示。下列有关说法中正确的是( )
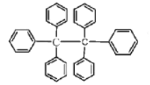
A. 它是一种苯的同系物,易溶于有机溶剂中
B. 它的分子式为C38H30,只含有非极性键
C. 核磁共振氢谱有3组峰
D. 它的分子中所有原子共平面
【答案】C
【解析】
A.根据苯的同系物的结构特点判断;
B.由结构简式可确定有机物分子式,根据形成共价键的原子是否为同种元素判断共价键的极性;
C.六个苯环的位置是等效的,苯环上有3种不同的位置;
D.由甲烷的结构可知,C最多与2个H共面,苯环为平面结构,据此分析。
A. 分子中含有6个苯环,而苯的同系物只含有1个苯环,与苯的结构不同,不是同系物,A项错误;
B. 它的分子中含有38个碳原子和30个氢原子,分子式为C38H30,分子中含有碳碳单键,为非极性键,含有碳氢单键,为极性键,B项错误;
C. 六个苯环的位置是等效的,但每个苯环上的氢不全等效,出现邻、间、对三种不同位置的取代产物,C项正确;
D. 中心两个C原子形成4个单键,采用sp3杂化,为四面体结构,它的分子中所有原子不可能共平面,D项错误;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氮氧化物(NOx)是大气污染物之一。工业上在一定的温度和催化剂条件下,可用NH3来消除NOx的污染,生成两种对环境无害的物质。
(1)请写出NH3与NO2反应的化学方程式____。
(2)①写出实验室中由固体物质制取氨气的化学方程式__;
②欲收集一瓶干燥的氨气,选择下图中的装置,其连接顺序为:发生装置→____(按气流方向,用小写字母表示)
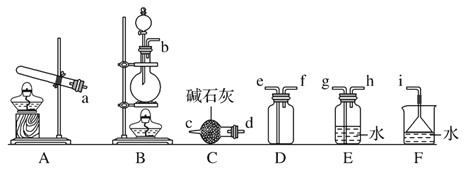
(3)电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。若用NO2气体进行模拟电解法吸收实验。
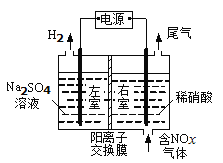
①写出电解时NO2发生反应的电极反应式:___。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Fe3+氧化性强于Cu2+,向含有![]() 、
、 ![]() 的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断错误的是( )
的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断错误的是( )
A.加入KSCN溶液不显红色
B.溶液中一定含Fe2+
C.溶液中一定含 ![]()
D.剩余固体中一定含铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的SO2。某同学设计下列实验以确定混合气体中含有乙烯和SO2。
(1)(I)、(Ⅱ)、(Ⅲ)、(Ⅳ)中盛放的试剂分别是________(可重复使用,填字母)。
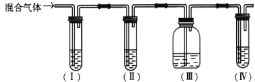
A.品红溶液 B. NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是_________________。
(3)使用装置Ⅱ的目的是_________________。
(4)使用装置Ⅲ的目的是_________________。
(5)确定含有乙烯的现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下图1所示是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
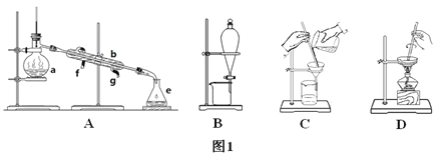
(1)从氯化钾溶液中得到氯化钾固体选择装置________(填代表装置图的字母,下同);除去自来水中的氯离子等杂质选择装置________。
(2)从碘水中分离出I2选择装置________,该分离方法的名称为________。
Ⅱ.海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如图2流程的实验:
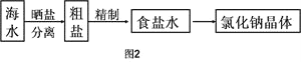
(3)粗盐中含![]() 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有: ①加入过量的Na2CO3溶液②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④加入盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是(填写序号字母)_________________。
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有: ①加入过量的Na2CO3溶液②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④加入盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是(填写序号字母)_________________。
A.⑤②③①④⑥⑦ B.⑤①②③⑥④⑦ C.⑤②①③④⑥⑦ D.⑤③②①⑥④⑦
(4)写出上述实验步骤中加入过量的Na2CO3溶液时发生反应的离子方程式:______________________,_______________________。
(5)由海水到氯化钠晶体的实验过程中要用到的主要装置是(从图1中给定的四种装置中选择)______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的类别和核心元素的化合价是研究物质性质的两个基本视角。
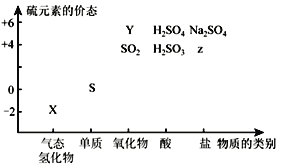

(1)图中Y物质的化学式为______。
(2)治理含CO、SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体.则治理烟道气反应的化学方程式为____________________________。
(3)实验室中X气体由不溶性的硫化亚铁(FeS)固体和稀硫酸混合反应制得,该反应的离子方程式为:_____________________________________________。
(4)Na2S2O3(硫代硫酸钠)是一种用途广泛的钠盐。
①下列物质用于Na2S2O3的制备,从氧化还原反应的角度,理论上有可能的是___。
a.Na2S+S b.Z+S c.Na2SO3+Y d.NaHS+NaHSO3
②Na2S2O3具有较强还原性,能作为织锦物漂白后的脱氯剂,脱氯后S2O32-转变为SO42-。 现需处理含标准状况下Cl2 2.24L的织锦物,理论上需要0.00100mol/L Na2S2O3溶液的体积为_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是石油裂解气的重要成分,由M制备环酯P的合成路线(部分反应条件略去)如图所示:
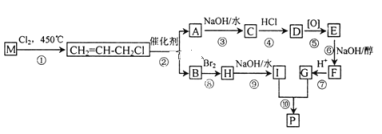
已知在特殊催化剂的作用下,能够发生碳碳双键两边基团互换的反应,如:
2CH2=CHR![]() CH2=CH2+RCH=CHR
CH2=CH2+RCH=CHR
回答下列问题:
(1)M的名称是____________。
(2)⑥的反应类型是________________。
(3)C的结构简式为____________。由C→G的过程中步骤④、⑥的目的是___________。
(4)符合下列条件D的同分异构体有______种。
①氯原子连在碳链的端点碳上 ②羟基连在不同的碳原子上
(5)由I和G在一定条件下制取环酯P的化学方程式为_________________。
(6)已知: 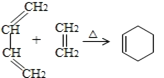 根据题中信息,设计以2-氯丙烷制备环己烯的合成路线(无机试剂和溶剂任选)___________。
根据题中信息,设计以2-氯丙烷制备环己烯的合成路线(无机试剂和溶剂任选)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为元素周期表的一部分、表中阿拉伯数字(1、2……)是元素周期表中行或列的序号,请参照元素A~I在表中的位置,回答下列问题。
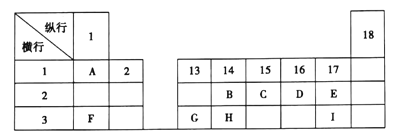
(1)B、C、H三元素中非金属性最强的是__________(写出元素符号)。
(2)表中某元素能形成两性氧化物,写出该氧化物的化学式___________。
(3)D与F构成原子个数比为1:1和1:2的两种离子化合物Z和M,写出Z与H2O反应的化学方程式_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是

A. 按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B. 图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C. 铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑
D. 图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com