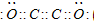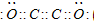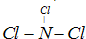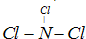����A��B��C��D��E���ֶ�����Ԫ�أ���֪���ǵ�ԭ��������������Ԫ��A��ԭ��ֻ��һ�����Ӳ㣬��֪Ԫ��A�ֱܷ���Ԫ��B��C��D�γɵ���������ȵĻ��������X��Y��Z��Y�д̼�����ζ����AΪ��Ԫ�أ�Ԫ��E�ĵ��ʵ�ˮ��Һ��Ư���ԣ���EΪ��Ԫ�أ�ZΪ�⻯�Z������ΪҺ̬��ZΪˮ������DΪ��Ԫ�أ�X��Y��Z����������ȣ�Y�д̼�����ζ��ZΪˮ�����Ӻ���10�����ӣ���YΪNH
3����CΪ��Ԫ�أ�����XΪCH
4����BΪ̼Ԫ�أ�
��AΪ��Ԫ�أ�BΪ̼Ԫ�أ�CΪ��Ԫ�أ�DΪ��Ԫ�أ�EΪ��Ԫ�أ�XΪCH
4��YΪNH
3��ZΪˮ��
��1��Ԫ��E�ĵ���ΪCl
2������ˮ�д�������ƽ��Cl
2+H
2O
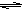
HCl+HClO��CaCO
3����ˮ�е�HCl��Ӧ��ʹ c��H
+����С��ƽ�������ƶ���HClOŨ������Ư������ǿ��
�ʴ�Ϊ��Ԫ��E�ĵ���ΪCl
2������ˮ�д�������ƽ��Cl
2+H
2O
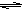
HCl+HClO��CaCO
3����ˮ�е�HCl��Ӧ��ʹ c��H
+����С��ƽ�������ƶ���HClOŨ������Ư������ǿ��
��2��C
2A
4ΪN
2H
4���ڹ�¯ˮ�м���N
2H
4�����ѹ�¯�������������ԭΪ�ṹ���ܵ����������������㣬N
2H
4 ���������ҷ�Ӧ������Ⱦ�����ɣ�N
2H
4������Ϊ������ͬʱ����ˮ����Ӧ�Ļ�ѧ����ʽΪ6Fe
2O
3+N
2H
4=4Fe
3O
4+N
2��+2H
2O������������N
2����Ԫ�ػ��ϼ���-2������Ϊ0�ۣ�1mol N
2H
4 �μӷ�Ӧת�Ƶ��ӵ���ĿΪ1mol��4��N
Amol
-1=4N
A��
�ʴ�Ϊ��6Fe
2O
3+N
2H
4=4Fe
3O
4+N
2��+2H
2O��4N
A��N
2��
��3��YΪNH
3����Ԫ��C����������������ˮ����ΪHNO
3�����߰����ʵ�����Ϊ2��1��ȫ��Ӧ��������ʣ�࣬��ҺΪ��ˮ�������1��1�����Һ��һˮ�ϰ��ĵ���̶ȴ���笠�����ˮ��̶ȣ���Һ�ʼ��ԣ�����c ��NH
4+����c ��NO
3-����c ��OH
-����c ��H
+����һˮ�ϰ�����̶Ȳ���������Һ������Ũ���ɴ�С��˳��Ϊc ��NH
4+����c ��NO
3-����c ��OH
-����c ��H
+�����ʴ�Ϊ���c ��NH
4+����c ��NO
3-����c ��OH
-����c ��H
+����
��4����CH
4��O
2���ܴ���O
2-�Ĺ���������ɵ�ԭ����У���������������Ӧ�������ڸ����ŵ磬��O
2-���������ɶ�����̼��ˮ�������ĵ缫��ӦʽΪ CH
4+4O
2--8e
-=CO
2+2H
2O��
�ʴ�Ϊ��CH
4+4O
2--8e
-=CO
2+2H
2O��
��5��A��B��D����Ԫ�ؿ����γ����ʽΪB
2A
4D������ζ���л�����л��������������¿���ˮ�⣬���ɺ�̼ԭ������ͬ�����ֳ����л���������л����������ʳƷ��ζ������������ζ���л���B
2A
4DΪCH
3COOCH
2CH
3��CH
3COOCH
2CH
3��һ��������ˮ��Ļ�ѧ����ʽ��CH
3COOCH
2CH
3+H
2O
CH
3COOH+CH
3CH
2OH��
�ʴ�Ϊ��CH
3COOCH
2CH
3+H
2O
CH
3COOH+CH
3CH
2OH��

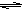
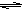



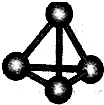 ����A��B��C��D��E��F���ֶ�����Ԫ�أ����ǵ�ԭ��������������D��E���⻯����ӹ��Ͷ���V�ͣ�A��B������������֮����C��������������ȣ�A�ֱܷ���B��C��D�γɵ���������ȵķ��ӣ���A��D���γɵĻ���������¾�ΪҺ̬��
����A��B��C��D��E��F���ֶ�����Ԫ�أ����ǵ�ԭ��������������D��E���⻯����ӹ��Ͷ���V�ͣ�A��B������������֮����C��������������ȣ�A�ֱܷ���B��C��D�γɵ���������ȵķ��ӣ���A��D���γɵĻ���������¾�ΪҺ̬��