
【题目】1934年约里奥–居里夫妇在核反应中用α粒子(即氦核![]() )轰击金属原子
)轰击金属原子![]() ,得到核素
,得到核素![]() ,开创了人造放射性核素的先河:
,开创了人造放射性核素的先河:![]() +
+![]() →
→![]() +
+![]() 。其中元素X、Y的最外层电子数之和为8。下列叙述正确的是
。其中元素X、Y的最外层电子数之和为8。下列叙述正确的是
A.![]() 的相对原子质量为26
的相对原子质量为26
B.X、Y均可形成三氯化物
C.X的原子半径小于Y的
D.Y仅有一种含氧酸
【答案】B
【解析】
原子轰击实验中,满足质子和质量数守恒,因此W+4=30+1,则W=27,X与Y原子之间质子数相差2,因X元素为金属元素,Y的质子数比X大,则Y与X位于同一周期,且Y位于X右侧,且元素X、Y的最外层电子数之和为8,设X最外层电子数为a,则Y的最外层电子为a+2,解得a=3,因此X为Al,Y为P,以此解答。
A.![]() 的质量数为27,则该原子相对原子质量为27,故A错误;
的质量数为27,则该原子相对原子质量为27,故A错误;
B.Al元素均可形成AlCl3,P元素均可形成PCl3,故B正确;
C.Al原子与P原子位于同一周期,且Al原子序数大于P原子序数,故原子半径Al>P,故C错误;
D.P的含氧酸有H3PO4、H3PO3、H3PO2等,故D错误;
故答案为:B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某学生欲配制6.0mol/L的H2SO4 1000 mL,实验室有三种不同浓度的硫酸:
①480mL 0.5mol/L 的硫酸;②150mL 25%的硫酸(ρ=1.18g/mL);③足量的18mol/L的硫酸。有三种规格的容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为______mol/L(保留1位小数)。
(2)配制该硫酸溶液应选用容量瓶的规格为______mL。
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol/L的浓硫酸____mL,沿玻璃棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D._________________________________________________________________________________________________________________________________
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(4)如果省略操作D,对所配溶液浓度有何影响?________(填“偏大”、“偏小”或“无影响”)。
(5)进行操作C前还需注意____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在指定条件下,下列各组离子一定能大量共存的是( )
A.滴加甲基橙试剂显红色的溶液中:Na、Fe2、Cl-、NO3-
B.滴入KSCN显血红色的溶液中:NH4、Al3、NO3-、SO42-
C.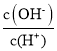 =1012的溶液中:NH4+、K+、Cl-、HCO3-
=1012的溶液中:NH4+、K+、Cl-、HCO3-
D.由水电离的c(H+)=1.0×l0-13mol/L溶液中:K、Al3、SO42-、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常利用SiO2 和碳反应来制取硅,写出反应的化学方程式___________________。
工业上还可以利用镁制取硅,反应为2Mg+SiO2 = 2MgO+Si,同时会发生副反应:2Mg + Si = Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 ___________________________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃.用化学方程式表示这两个反应①________________________②___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按以下步骤可从![]() 合成
合成![]() (部分试剂和反应条件已略去)。
(部分试剂和反应条件已略去)。
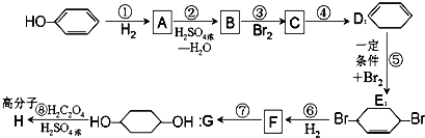
请回答下列问题:
(1)B,F的结构简式为:B___,F_______;
(2)反应①~⑦中属于消去反应的是(填代号)_______;
(3)根据反应![]() +Br2
+Br2![]()
![]() ,写出在同样条件下CH2=CHCH=CH2与等物质的量Br2发生加成反应的化学方程式:__;
,写出在同样条件下CH2=CHCH=CH2与等物质的量Br2发生加成反应的化学方程式:__;
(4)写出第④步C→![]() 的化学方程式(有机物写结构简式,注明反应条件)__;
的化学方程式(有机物写结构简式,注明反应条件)__;
(5)与4个不同的原子或原子团相连的碳原子称为手性碳原子;A﹣G这七种有机物分子中含有手性碳原子的是(填序号)__;
(6)核磁共振谱是测定有机物分子结构最有用的工具之一,在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目,例如:乙醛的结构式为:![]() ,其PMR谱中有2个信号峰,其强度之比为3:1,则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是__。
,其PMR谱中有2个信号峰,其强度之比为3:1,则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是__。
A ![]() B
B ![]() C
C ![]() D
D ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+I2(g)![]() 2HI(g)ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI0.2mol,在相同温度下分别达到平衡。现欲使甲中HI平衡时的百分含量大于乙中HI平衡时的百分含量,则应采取的措施是
2HI(g)ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI0.2mol,在相同温度下分别达到平衡。现欲使甲中HI平衡时的百分含量大于乙中HI平衡时的百分含量,则应采取的措施是
A. 甲、乙提高相同温度 B. 甲中加入0.1molHe,乙中不变
C. 甲降低温度,乙增大压强 D. 甲增加0.1molH2,乙增加0.1molI2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A.漂白粉可以用于生活用水的消毒
B.石蕊溶液滴入氯水中,溶液变红,随后迅速褪色
C.氯气通入水中杀菌消毒,发生了化学变化
D.漂白粉在空气中久置变质,原因是原白粉中的CaCl2与空气中的CO2反应生成CaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如右图所示。下列结论不正确的是( )

A. 反应开始4 min内温度对反应速率的影响比浓度大
B. 一段时间后,反应速率减小的原因是c(H+)减小
C. 反应在2~4 min内平均反应速率最大
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.06 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
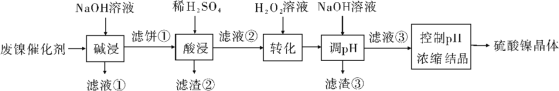
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
开始沉淀时(c=0.01 mol·L1)的pH 沉淀完全时(c=1.0×105 mol·L1)的pH | 7.2 8.7 | 3.7 4.7 | 2.2 3.2 | 7.5 9.0 |
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______________。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式______________。
(2)“滤液②”中含有的金属离子是______________。
(3)“转化”中可替代H2O2的物质是______________。若工艺流程改为先“调pH”后“转化”,即
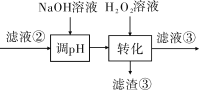
“滤液③”中可能含有的杂质离子为______________。
(4)利用上述表格数据,计算Ni(OH)2的Ksp=______________(列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L1,则“调pH”应控制的pH范围是______________。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式______________。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com