
三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。根据下列工艺流程示意图回答问题。
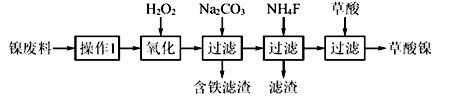
(1)操作1为 。
(2)生产过程中多次进行过滤,实验室进行过滤操作中需用到玻璃棒,下列实验操作中哪些操作中玻璃棒的作用完全相同的是 (填选项字母)。
①配制0.1mol/L的H2SO4溶液
②测定Na2CO3溶液的pH
③用KI淀粉试纸检验溶液中的氧化性离子
④加热食盐溶液制备NaCl晶体
⑤配制20%的KNO3溶液
A.①⑤ B.②③ C.④⑤ D.①④
(3)加入H2O2发生的主要反应的离子方程式为 ;
加入Na2CO3溶液调pH至4.0~4.5,其目的为 ;
加入NH4F后除掉的杂质是 。
(4)草酸镍(NiC2O4·2H2O)在热空气中干燥脱水后在高温下煅烧三小时,制得Ni2O3,同时获得混合气体。草酸镍受热分解的化学方程式为 。
(5)工业上还可用电解法制取Ni2O3。用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2SO4后采用惰性电极电解。电解过程中产生的Cl2有80%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍。ClO-氧化Ni(OH)2生成Ni2O3的离子方程式为 。amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为 。
(6)电解法制取Ni2O3的实际过程中,有时获得一种结晶水合物,已知含1molNi的该物质中含有0.5mol结晶水。取该化合物20.2g进行充分加热,获得Ni2O3固体和0.2mol水,则该结晶水合物的化学式为 。
【知识点】电解原理、配制一定浓度溶液计算
【答案解析】(15分,除注明外其余每空2分)
(1)加酸溶解,过滤(1分) (2)BC
(3)2Fe2++H2O2+2H+===2Fe3++2H2O; 促进Fe3+水解沉淀完全(1分); Ca2+、Mg2+
(4)2NiC2O4 Ni2O3+3CO↑+CO2↑
Ni2O3+3CO↑+CO2↑
(5)ClO-+2Ni(OH)2===Cl-+Ni2O3+2H2O 1.25a mol
(6)NiOOH·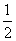 H2O或2NiOOH·H2O
H2O或2NiOOH·H2O
解析:(1)分析框图:含镍废料(镍、铁、钙、镁合金为主),要使之变成离子,应该加酸溶解,溶解金属,再除去不溶物过滤;
(2)①配制O.1mol/L的H2SO4溶液,搅拌引流作用;
②测定Na2CO3溶液的pH,玻璃棒蘸取溶液滴在pH试纸上测定;
③用KI淀粉试纸检验 溶液中氧化性离子,玻璃棒蘸取溶液滴在KI淀粉试纸上测定;
④加热食盐溶液制备NaCl晶体,玻璃棒搅拌避免局部受热固体飞溅;
⑤配制20%的KNO3溶液,玻璃棒搅拌加速溶解;
所以②③和④⑤符合;故答案为:BC.
(3)加双氧水的目的是氧化生成Fe3+,反应的离子方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O,加入碳酸钠溶液的作用是调节pH,促进铁离子水解沉淀完全,再加入NH4F的目的是除去钙离子、镁离子,故最后加草酸时生成草酸镍沉淀;
故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O,促进铁离子水解沉淀完全,Ca2+、Mg2+;
(4)草酸镍(NiC2O4•2H2O)在热空气中干燥脱水后生成NiC2O4,NiC2O4再发生氧化还原反应(Ni由+2价升高到+3价,则C由+3价降低到+2价,题中要求生成混合气体,则另一气体为CO2)生成Ni2O3、CO、CO2,再利用化合价升降相等,Ni:升高2×(3-2),C:升高1×(4-3),C:降低:3×(3-2),配平方程式为:2NiC2O4 Ni2O3+3CO↑+CO2↑;
Ni2O3+3CO↑+CO2↑;
(5)Cl由+1价降低到-1价,Ni由+2价升高到+3价,利用化合价升降相等可配平ClO-、Ni(OH)2、Cl-、Ni2O3的计量数,再利用H原子守恒配平水的计量数,最后可利用O原子检查配平是否正确,得到离子方程式为:ClO-+2Ni(OH)2═Cl-+Ni2O3+2H2O;
ClO-+2Ni(OH)2═Cl-+Ni2O3+2H2O
1 2
n(ClO-) a mol
则n(ClO-)=0.5 a mol
Cl2+2OH-═ClO-+Cl-+H2O
0.8n(Cl2) 0.5 a mol
则n(Cl2)=0.625 a mol
进行电解时:2Cl--2e-═Cl2↑
2 1
n(e-) 0.625 a mol
则n(e-)=1.25a mol;
(6)0.2 mol水的质量为3.6g,则m(Ni2O3)=20.2 g-3.6g=16.6g,n(Ni2O3)=0.1mol,即:n(Ni2O3):n(H2O)=0.1mol:0.2 mol=1:2,再利用原子守恒写成结晶水合物的形式,“1mol该物质中含有0.5 mol结晶水”,即NiOOH·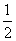 H2O或整合成:2NiOOH•H2O;
H2O或整合成:2NiOOH•H2O;
【思路点拨】本题考查了流程分析推断,实验操作步骤的分析判断,化学方程式计算和电解原理分析应用,题目综合性较大,难度较大。


科目:高中化学 来源: 题型:
实验室配制500mL 0.2mol/L的FeSO4溶液,实验操作步骤有:
①在天平上称出27.8g绿矾,把它放在烧杯里,用适量的蒸馏水使它完全溶解
②把制得的溶液小心地注入500mL容量瓶中
③继续向容量瓶中加蒸馏水至液面距刻度1~2cm处.改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞塞紧,充分摇匀
请填写下列空白:
(1)操作步骤的正确顺序为(填序号) ①②④③⑤ .
(2)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是
500mL容量瓶 、 胶头滴管 .
(3)某同学观察液面的情况如图所示,对所配溶液浓度有何影响?会 偏高 (填“偏高”、“偏低”或“无影响”).
(4)若出现如下情况,所配溶液浓度将偏高还是偏低:没有进行操作步骤④,会 偏低 ;加蒸馏水时不慎超过了刻度,会 偏低 .向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面,会 偏低 .
(5)若实验过程中出现如下情况应如何处理?加蒸馏水时不慎超过了刻度,应 重新配制 .

查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,体积为1 L的密闭容器中发生如下反应:
SiF4(g)+2H2O(g)  SiO2(s)+4HF(g) ΔH=+148.9 kJ·mol-1
SiO2(s)+4HF(g) ΔH=+148.9 kJ·mol-1
(1)下列各项中能说明该反应已达化学平衡状态的是________(填字母序号)。
a.v消耗(SiF4)=4v生成(HF) b.容器内气体压强不再变化
c.容器内气体的总质量不再变化 d.HF的体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中t2>t1)所示。
| 反应时间/min | n(SiF4)/mol | n(H2O)/mol |
| 0 | 1.20 | 2.40 |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
通过a或b的值及化学平衡原理说明t1时反应是否达到化学平衡状态:_________________________________________________________________________。
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应________(填序号)。
a.一定向正反应方向移动 b.一定向逆反应方向移动
c.一定是减小压强造成的 d.一定是升高温度造成的 e.SiF4的平衡转化率一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W四种元素原子序数依次增大且均小于36。 Z基态原子最外层电子数是其内层电子总数的3倍,Y基态原子是同周期元素中未成对电子数最多的原子,X分别与Y、Z元素组合均可形成10电子微粒, W基态原子有10个价电子。回答下列问题(以下问题均以推知元素符号作答):
(1)若 YX3与X2Z﹑YX2-与ZX-﹑Y3-与Z2-性质相似,请写出Mg(YX2)2在一定条件下分解的化学反应方程式
⑵已知0℃时X2Z的密度为a g/cm3,其晶胞中X2Z分子的空间排列方式与金刚石晶胞类似,相似的原因是 。两个X2Z分子间的最近距离为 pm(用a和NA表示)。已知X2Y的升华热是51 kJ/mol,除氢键外,X2Z分子间还存在范德华力(11 kJ/mol),则X2Z晶体中氢键的“键能”是 kJ/mol。
⑶ WZ是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面。工业上常以W(YZ3)2·6X2Z和尿素[CO(NH2)2]为原料制备。
①W2+的基态核外电子排布式为 ,其核外电子有 种运动状态。
②尿素分子中碳原子的杂化方式为 ,1 mol尿素分子中含有的σ键数为 。
 ③YZ3-的空间构型 。
③YZ3-的空间构型 。
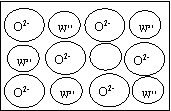
④WZ晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种WZ晶体中就存在如右图所示的缺陷:一个W2+空缺,另有两个W2+被两个W3+所取代。其结果晶体仍呈电中性,但化合物中W和Z的比值却发生了变化。经测定某样品中W3+与W2+的离子数之比为6∶91。若该晶体的化学式为WxZ,则x= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的化学方程式或离子方程式正确的是
A. 以MnO2为原料制得的MnCl2溶液中常含有Cu2+等金属离子,通常添加难溶电解质MnS使这些离子形成硫化物沉淀而除去:Cu2+ + S2-=CuS↓
B. 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2 + 2OH- = SiO32- + H2O
C. 金属钠在空气中放置表面会很快失去金属光泽:2Na + O2 = Na2O2
D. 向硫酸亚铁铵[(NH4)2Fe(SO4) 2·6H2O]的稀溶液中加入足量Ba(OH) 2稀溶液:
NH4+ + Fe2+ + SO42-+ Ba2+ +3OH- = BaSO4↓+ Fe(OH) 2↓+ NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是( )
A.野火烧不尽,春风吹又生 B.春蚕到死丝方尽,蜡炬成灰泪始干
C.粉身碎骨浑不怕,要留青白在人间 D.爆竹声中一岁除,春风送暖入屠苏
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组在溶液中反应,不管反应物的量是多少,都能用同一离子方程式表示的是( )
A.FeBr2与Cl2 B.Ba(OH)2与H2SO4
C.HCl与Na2CO3 D.NaHCO3与Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
用图中所示的装置进行实验,实验现象与预测不一致的是

| ①中的物质 | ②中的物质 | 预测现象 | |
| A | 浓氨水 | FeCl3溶液 | ②中有红褐色沉淀 |
| B | 浓氨水 | 浓盐酸 | ③中有白烟 |
| C | 浓硝酸 | 淀粉KI溶液 | ②中溶液为蓝色 |
| D | 饱和亚硫酸溶液 | 蓝色石蕊试液 | ②中溶液先变红又褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
咖啡酸可用作化学原料的中间体,其结构如图。下列关
于咖啡酸的说法中正确的是
A.分子中所有官能团均能与NaOH反应,且反应原因相同
B.一定条件下,咖啡酸能够发生取代反应、加聚反应、缩
聚反应,但不能与NaHCO3溶液反应
C.分子中的所有碳原子可能共平面,但氧原子不可能与所有碳原子处于同一平面上
D.咖啡酸与浓溴水反应,一个咖啡酸分子中最多能引入5个溴原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com