
【题目】实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4 ℃、118 ℃、77.1 ℃)。

乙酸乙酯的制取装置
请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是_______________。
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是__________。
(3)若用1 mol乙醇和1 mol 乙酸在浓硫酸作用下加热,充分反应,能否________(填“能或不能”)生成1mol乙酸乙酯,其原因是___________。
(4)反应开始时用酒精灯对圆底烧瓶小火加热的原因是___________________________。
(5)分离锥形瓶中所得乙酸乙酯和碳酸钠溶液的操作为(只填名称)__________。
【答案】防止烧瓶中液体暴沸 先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡 不能 该反应是可逆反应,反应不能进行到底 加快反应速率,防止反应物乙醇和乙酸大量挥发而损失 分液
【解析】
(1)乙醇、浓硫酸、乙酸为液体,反应需要加热,因此加入碎瓷片的作用是防止烧瓶中的液体暴沸;
(2)浓硫酸的密度大于乙醇的密度,乙醇和浓硫酸混合相当于稀释浓硫酸,因此混合乙醇和浓硫酸的操作是现在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶中,边加边振荡;
(3)乙醇和乙酸发生酯化反应CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O,该反应为可逆反应,不能进行到底,因此1mol乙醇与1mol乙酸发生酯化反应,不能生成1mol乙酸乙酯,产生的乙酸乙酯物质的量小于1mol;
CH3COOCH2CH3+H2O,该反应为可逆反应,不能进行到底,因此1mol乙醇与1mol乙酸发生酯化反应,不能生成1mol乙酸乙酯,产生的乙酸乙酯物质的量小于1mol;
(4)乙醇、乙酸易挥发,如果加强热,容易造成乙醇和乙酸大量挥发,因此为了减少乙醇和乙酸的挥发,以及加快反应速率,采用小火加热的方式进行;
(5)乙酸乙酯不溶于碳酸钠溶液,且出现分层,因此采用分液的方法进行分离。


科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:

回答下列问题:.
(1)固体1含有的物质是_________、CaCO3、Ca(OH)2;捕获剂所捕获的气体主要是_______________。
(2)若X是空气,则上述反应中NO和O2的物质的量之比最好为___________,若空气过量,导致的结果会是____________________________。
(3)流程中处理含NH4+废水时发生反应的离子方程式为____________________________。气体1也可通过催化剂直接转化成无污染气体,反应的化学方程式为_____________________________________。
(4)若工业废气中主要含N2、SO2,不考虑其他成分,则可用下列工艺生产NaHSO3过饱和溶液[NaHSO3过饱和溶液是生产焦亚硫酸钠(Na2S2O5)的原料]。
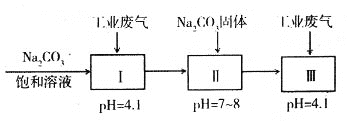
pH=4.1时,I中反应的化学方程式为_________________________;工艺中加入Na2CO3
固体、并再次通入废气的目的是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒容容器中加入amol A使 A(g) ![]() B(?)+C(?)达到平衡状态(△H>0),升高温度,气体平均相对分子质量有变小趋势,则下列判断中正确的是( )
B(?)+C(?)达到平衡状态(△H>0),升高温度,气体平均相对分子质量有变小趋势,则下列判断中正确的是( )
A. B和C可能都是固体 B. B和C一定都是气体
C. 若C为固体,则B不一定是气体 D. B和C可能都是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中一定能大量共存的是( )
A. 含有大量 Ba2+的溶液中:Cl- K+ ![]()
![]()
B. 含有大量H+的溶液中:Mg2+ Na+ ![]()
![]()
C. 含有大量OH-的溶液中:Mg2+ ![]()
![]()
![]()
D. 含有大量Na+的溶液中:H+ K+ ![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.灼烧至红热的细铁丝与氯气反应生成FeCl2
B.常温常压下,22.4L SO2中含有的分子数为6.02×1023
C.纯碱溶液呈碱性,热的纯碱溶液可以去除物品表面的油污
D.Na2O2能与水或CO2反应生成O2,可用作呼吸面具中的供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯和聚乙烯的叙述不正确的是( )
A. 乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物
B. 乙烯的化学性质比聚乙烯活泼
C. 取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等
D. 乙烯和聚乙烯都能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为________________________________________________________________________。
(2)W与Y 可形成化合物W2Y,该化合物的电子式为________________________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为____________________。
(4)比较Y、Z气态氢化物的稳定性________>________(用分子式表示)。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是________>________>________>________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:X>W>Z
C. 最简单气态氢化物的热稳定性:Y>X>W>Z
D. 元素X、Z、W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种工业制备SrCl2·6H2O的生产流程如下图所示:

已知:①M(SrCl2·6H2O)=267 g/mol;
②Ksp(SrSO4)=3.3×10-7、Ksp(BaSO4)=1.1×10-10;
③经盐酸浸取后,溶液中有Sr2+和Cl-及少量Ba2+。
(1)隔绝空气高温焙烧,若2 mol SrSO4中只有S被还原,转移了16 mol电子。写出该反应的化学方程式:______________________________ 。
(2)过滤2后还需进行的两步操作是_____、_____。
(3)加入硫酸溶液的目的是_____;为了提高原料的利用率,滤液中Sr2+的浓度应不高于_____ mol/L(注:此时滤液中Ba2+浓度为1×10-5 mol/L)。
(4)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2 mol的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_____。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com