
【题目】下列说法正确的是( )
A.灼烧至红热的细铁丝与氯气反应生成FeCl2
B.常温常压下,22.4L SO2中含有的分子数为6.02×1023
C.纯碱溶液呈碱性,热的纯碱溶液可以去除物品表面的油污
D.Na2O2能与水或CO2反应生成O2,可用作呼吸面具中的供氧剂
科目:高中化学 来源: 题型:
【题目】为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是
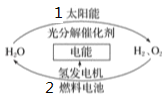
A. 过程1是放热反应
B. 过程2可将化学能转化为电能
C. 氢能源可从自然界直接获取,是一次能源
D. 氢气不易贮存和运输,无开发利用价值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容时,N2O4 ![]() 2NO2已达平衡状态。现做如下改变:①加入一定量的NO2;②加入一定量的N2O4,二者均再达平衡状态后, NO2和N2O4的物质的量之比值,应( )
2NO2已达平衡状态。现做如下改变:①加入一定量的NO2;②加入一定量的N2O4,二者均再达平衡状态后, NO2和N2O4的物质的量之比值,应( )
A. ①中增大②中减小 B. ①中减小②中增大 C. 均增大 D. 均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两个密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入1molN2和3mol H2的混合气体,并使A和B容积相等(如下图所示)。在保持400℃的条件下使之发生如下反应:N2(g)+ 3H2(g) ![]() 2NH3(g) 。
2NH3(g) 。
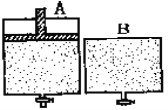
(1)达到平衡时所需的时间:A___ B,N2的转化率:A___B(填“大于”、“小于”或“等于”,下同)
(2)都达平衡后,两容器中分别通入1mol氩气,再达平衡后,N2的转化率:A中_____ B中 _____ (填“增大”、“减小”或“不变”)
(3)都达平衡后,向两容器中再通入1molN2和3mol H2 ,再达到平衡后:混合气体的密度:A中____ B中_____(填“增大”、“减小”或“不变”,下同);混合气体的平均相对分子质量:A中___B中 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某固定容积的密闭容器中,存在下列化学平衡aA(g) ![]() bB(g)+cC(g),在温度不变的条件下,向容器中再充入一定量的A物质,重新达到平衡时,判断在下列情况下有关物质量的变化趋势(在下列空白中填写“增大”“减小”或“不变”)
bB(g)+cC(g),在温度不变的条件下,向容器中再充入一定量的A物质,重新达到平衡时,判断在下列情况下有关物质量的变化趋势(在下列空白中填写“增大”“减小”或“不变”)
(1)当a=b+c时,B的物质的量分数___________。
(2)当a>b+c时,A的物质的量分数_______。
(3)当a<b+c时,A的转化率___________。
(4)当a<b+c时,混合气体的平均相对分子质量 ___,混合气体的密度 _____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4 ℃、118 ℃、77.1 ℃)。

乙酸乙酯的制取装置
请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是_______________。
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是__________。
(3)若用1 mol乙醇和1 mol 乙酸在浓硫酸作用下加热,充分反应,能否________(填“能或不能”)生成1mol乙酸乙酯,其原因是___________。
(4)反应开始时用酒精灯对圆底烧瓶小火加热的原因是___________________________。
(5)分离锥形瓶中所得乙酸乙酯和碳酸钠溶液的操作为(只填名称)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的碘元素(以I形式存在)。实验室中提取碘的流程如下:

(1)实验操作③的名称是________,所用主要仪器名称为________。
(2)提取碘的过程中,可供选择的有机试剂是________(填序号)。
A.酒精(沸点78 ℃) B.四氯化碳(沸点77 ℃)
C.甘油(沸点290 ℃) D.苯(沸点80 ℃)
(3)在操作②中,溶液中生成少量ICl(ICl的性质类似于氯气),为消除此杂质,使碘全部游离出来,应加入适量________(填序号)溶液,反应的离子方程式___________________。
A.KIO3 B.HClO C.KI D.Br2
(4)利用碘的有机溶液得到单质I2的方法是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列短周期元素性质的数据判断,下列说法正确的是
|
|
|
|
|
|
|
| |
原子半径 |
|
|
|
|
|
|
|
|
最高价或最低价 |
|
|
|
|
|
|
|
|
A. 元素![]() 形成的氢化物稳定
形成的氢化物稳定
B. 元素![]() 的非金属强,所以氢化物的沸点高
的非金属强,所以氢化物的沸点高
C. 元素![]() 形成的化合物是共价化合物
形成的化合物是共价化合物
D. 元素![]() 的最高价氧化物对应水化物的碱性最强
的最高价氧化物对应水化物的碱性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列物质中原子数最多的是
A. 64 g SO2 B. 3.01×1023个N2
C. 0.75 mol H2S D. 36 mL H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com