
下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O2(g)═CO2(g) ;△H1 C(s) +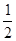 O2(g)═CO(g) ; △H2
O2(g)═CO(g) ; △H2
②S(s)+O2(g)═SO2(g) ;△H3 S(g) +O2(g)═SO2(g) ;△H4
③H2(g) +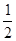 O2(g)═H2O(g);△H5 2H2(g)+O2(g)═2H2O(l);△H6
O2(g)═H2O(g);△H5 2H2(g)+O2(g)═2H2O(l);△H6
④CaCO3(s)═CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)═Ca(OH)2(s);△H8
| A.① | B.④ | C.①②③ | D.②③④ |
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:单选题
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是N2和H2反应生成2 mol NH3过程中能量变
化示意图,写出生成NH3的热化学方程式:
_____________________________________________
___________________________。
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能。从化学键的角度分析,化
学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过
程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应N2(g)+3H2(g)??2NH3(g) ΔH=a kJ·mol-1。
试根据表中所列键能数据估算a的数值:________。
| 化学键 | H—H | N—H | N≡N |
| 键能kJ·mol-1 | 436 | 391 | 945 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学反应中通常伴随着能量变化,下列说法中错误的是
| A.煤燃烧时将部分化学能转化为热能 |
| B.电解熔融Al2O3时将部分化学能转化为电能 |
| C.TNT爆炸时将部分化学能转化为动能 |
| D.镁条燃烧时将部分化学能转化为光能 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据以下三个热化学方程式:
(1)2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH= -Q1kJ·mol-1
(2)2H2S(g)+O2(g)=2S(g)+2H2O(g) ΔH= -Q2kJ·mol-1
(3)2H2S(g)+O2(g)=2S(g)+2H2O(l) ΔH= -Q3kJ·mol-1
判断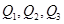 三者关系正确的是
三者关系正确的是
| A.Q1>Q2>Q3 | B.Q1>Q3>Q2 | C.Q3>Q2>Q1 | D.Q2>Q1>Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应既属于氧化还原反应,又是吸热反应的是
| A.铝片与稀盐酸的反应 | B.Ba(OH)2?8H2O与NH4Cl的反应 |
| C.灼热的炭与CO2的反应 | D.甲烷在氧气中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| B.由C(石墨)= C(金刚石) △H=+1.90 kJ/mol可知,金刚石比石墨稳定 |
| C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为: 2H2(g)+O2(g)=2H2O(l) △H=-285.8kJ/mol |
| D.在稀溶液中,H+(aq)+ OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知下列四个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) △H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g) △H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l) △H4;
则△H四者的关系中正确的是
| A.△H1>△H2>△H3>△H4 | B.△H4>△H2>△H3>△H1 |
| C.△H3>△H4>△H1>△H2 | D.△H4>△H3>△H2>△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
半导体工业用石英砂做原料通过三个重要反应生产单质硅
SiO2(s)+2C(s)=Si(s)+2CO(g) △H1=+682.44kJ·mol-1
(石英砂) (粗硅)
Si(s)+2C12(g)=SiCl4(l) △H2=一657.01kJ·mol-1
(粗硅)
SiCl4(l)+2Mg(s)=2MgCl2(s)+Si(s) △H3=一625.63kJ·mol-1
(纯硅)
若生产1.00kg纯硅放出的热量为
| A.21.44kJ | B.600.20kJ | C.21435.71kJ | D.1965.10kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com