
【题目】人们对苯的认识有一个不断深化的过程。已知分子式为![]() 的甲、乙两种物质的结构简式如图所示。
的甲、乙两种物质的结构简式如图所示。
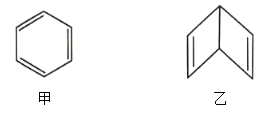
(1)甲、乙的化学性质的区别为甲能___________________(填字母,下同),而乙能___________________。
A.被酸性![]() 溶液氧化
溶液氧化
B.与溴水发生加成反应
C.与氢气发生加成反应
(2)![]() 甲和
甲和![]() 乙分别与
乙分别与![]() 发生完全加成反应,甲消耗___________
发生完全加成反应,甲消耗___________![]()
![]() ,而乙消耗__________
,而乙消耗__________![]()
![]()
(3)![]() 还可能有另一种结构丙(如图所示),其二氯代物有___________________种。
还可能有另一种结构丙(如图所示),其二氯代物有___________________种。

【答案】C ABC 3 2 3
【解析】
(1)根据结构简式图可知,甲为苯,分子中不存在碳碳双键,不具有烯烃的性质,因而不能被酸性高锰酸钾溶液氧化,与溴水也不能发生加成反应,但可以和H2发生加成反应,而乙为烯烃,分子中含有碳碳双键,能被酸性高锰酸钾溶液氧化,与溴水也能发生加成反应,也可以和H2发生加成反应,故答案为:C;ABC;
(2)1mol苯可以与3molH2发生加成反应得到环己烷,1个乙分子中有2个碳碳双键,1mol碳碳双键可与1molH2发生加成反应,则1mol乙可与2molH2发生加成反应,故答案为:3;2;
(3)因为六个碳原子共连接6个氢原子,所以其二氯代物可能有![]() 3种,故答案为:3。
3种,故答案为:3。


科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.向水中通入NO2:2NO2+H2O=2H++NO![]() +NO
+NO
B.向NH4HCO3溶液中加入过量NaOH溶液:HCO![]() +OH-=CO
+OH-=CO![]() +H2O
+H2O
C.向稀硝酸中加入FeO:3FeO+NO![]() +10H+=3Fe3++NO↑+5H2O
+10H+=3Fe3++NO↑+5H2O
D.向Na2SO3溶液中加入酸性K2Cr2O7溶液:3SO![]() +Cr2O
+Cr2O![]() +2H2O=3SO
+2H2O=3SO![]() +2Cr3++6OH-
+2Cr3++6OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用煤化工所得的苯可合成甲苯、乙苯、环己烷,其反应如下:
①![]()
![]()
![]() (甲苯)
(甲苯)![]()
②![]()
![]()
![]()
 (乙苯)
(乙苯)
③![]()
![]()
![]()
![]() (环己烷)
(环己烷)
下列说法正确的是( )
A.反应①、②、③均属于加成反应
B.溴水中加入苯,二者可发生取代反应
C.甲苯中所有原子一定在同一平面上
D.能用溴的四氯化碳溶液判断反应②所得的乙苯中是否混有乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对分子性质的解释中,不正确的是( )
A. 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B. 由于乳酸(![]() )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
)中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
C. HF的稳定性很强,是因为其分子间能形成氢键
D. 由右图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子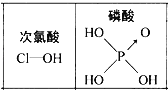
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1 ℃和T2 ℃时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )
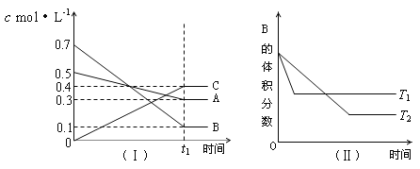
A.该平衡体系的化学反应方程式为:A(g)+B(g)![]() C(g)
C(g)
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动
C.T1<T2
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度和有催化剂条件下,恒容密闭容器中发生反应N2+3H2 2NH3,下列说法正确的是( )
t/min | 0 | 5 | 10 | 15 | 20 |
c(NH3)/(mol·L-1) | 0 | 1.00 | 1.60 | 1.80 | 1.80 |
A. 0~10min内,v(NH3)=0.16mol·L-1·min-1 B. 0~10min内,v(N2)=0.18mol·L-1·min-1
C. 0~10min内,v(N2)=0.16mol·L-1·min-1 D. 15~20min内,反应v(N2)正= v(N2)逆=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)检验气体中是否含有CO的实验操作:将该气体通入氯化钯(PdCl2)溶液中,观察是否有黑色的单质钯生成,写出对应的化学方程式:_______________。
(2)生产硫化钠大多采用无水芒硝(Na2SO4)—炭粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式:_________________。
(3)加入双氧水能提高软锰矿(主要成分是MnO2)的浸出率,锰转化成Mn2+。写出酸性条件下双氧水提高软锰矿浸出率的离子方程式:______________________________。
(4)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿(主要成分为CuFeS2)转化成硫酸盐,该过程反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由Cu、N、B等元素组成的新型材料有着广泛用途。
(1)基态 Cu+ 的核外电子排布式为____________。在高温下CuO 能分解生成Cu2O,试从原子结构角度解释其原因:_______________________________。
(2)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,它属于____晶体。
(3)化合物A (H3BNH3) 是一种潜在的储氢材料,它可由六元环状化合物 (HB=NH)3通过3CH4+ 2 (HB=NH)3+ 6H2O →3CO2 + 6H3BNH3 制得。
①与上述化学方程式有关的叙述不正确的是_________。(填标号)
A.反应前后碳原子的轨道杂化类型不变 |
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形 |
C.第一电离能:N>O>C>B |
D.化合物A中存在配位键 |
②1个 (HB=NH)3分子中有__个σ键。
(4)在硼酸盐中,阴离子有链状、环状等多种结构形式。图(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为________。图(b)是硼砂晶体中阴离子的环状结构,其中硼原子采取的杂化类型为_________。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烧杯A中盛放0.1mol/L的H2SO4溶液,烧杯B中盛放0.1mol/L的的CuCl2溶液(两种溶液均足量),组成的装置如图所示。下列说法不正确的是( )
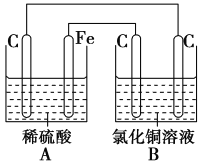
A.A为原电池,B为电解池
B.A为电解池,B为原电池
C.当A烧杯中产生0.1mol气体时,B烧杯中产生气体的物质的量也为0.1mol
D.经过一段时间,B烧杯中溶液的浓度减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com