
【题目】下列说法正确的是( )
A.已知X在一定条件下转化为Y,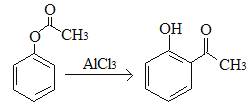 ,X与Y互为同分异构体,可用FeCl3溶液鉴别
,X与Y互为同分异构体,可用FeCl3溶液鉴别
B.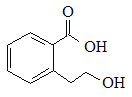 能发生的反应类型有:加成反应、取代反应、消去反应、水解反应
能发生的反应类型有:加成反应、取代反应、消去反应、水解反应
C.淀粉、蛋白质最终的水解产物都只有一种
D.香柠檬粉具有抗氧化功能,结构为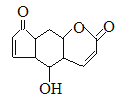 ,它与溴水发生反应,1mol最多消耗3molBr2,它与NaOH溶液反应,1mol最多消耗2molNaOH
,它与溴水发生反应,1mol最多消耗3molBr2,它与NaOH溶液反应,1mol最多消耗2molNaOH
【答案】A
【解析】
A.根据X、Y的分子的结构简式可知二者互为同分异构体,Y含有酚羟基,可用氯化铁溶液鉴别,A正确;
B. 含有苯环,因此可以发生加成反应;含有羧基、醇羟基,所以可以发生取代反应,由于羟基连接的碳原子的邻位碳原子上含有H原子,所以可以发生消去反应;但是该物质分子中无酯基、卤素原子,因此不能发生水解反应,B错误;
含有苯环,因此可以发生加成反应;含有羧基、醇羟基,所以可以发生取代反应,由于羟基连接的碳原子的邻位碳原子上含有H原子,所以可以发生消去反应;但是该物质分子中无酯基、卤素原子,因此不能发生水解反应,B错误;
C.淀粉可以不完全水解产生麦芽糖,完全水解产生葡萄糖;蛋白质水解产物是氨基酸,氨基酸的种类可能是一种,也可能是多种,C错误;
D.香柠檬粉具有抗氧化功能,结构为 ,它与溴水可发生加成反应,1mol最多消耗2molBr2,它含有酯基,酯基水解产生醇羟基和羧基,所以1mol该物质与NaOH溶液反应,1mol最多消耗1molNaOH,D错误。
,它与溴水可发生加成反应,1mol最多消耗2molBr2,它含有酯基,酯基水解产生醇羟基和羧基,所以1mol该物质与NaOH溶液反应,1mol最多消耗1molNaOH,D错误。
答案选A。


科目:高中化学 来源: 题型:
【题目】(1)根据A~E几种烃分子的结构填空。
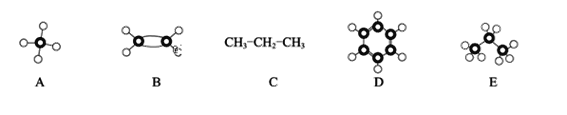
上述分子中属于C的同系物的是_____________(填字母序号)。
(2)随着工业的发展和社会的进步,人们日益关注环境问题。
①下列物质属于室内空气污染物的是__________________(填字母序号,下同);
A CO2 B 甲醛 C N2
②按照垃圾分类的方法,易拉罐瓶属于________________________;
A 可回收物 B 可堆肥垃圾
③工业废水需处理达标后才能排放。下列废水处理的方法合理的是__________。
A 用氯气除去废水中的悬浮物 B 用中和法除去废水中的酸
C 用明矾除去废水中的重金属离子
(3)化学是材料科学发展的基础,合理使用材料有利于人类的生产和生活。
①在一定条件下,将某种单体进行加聚反应得到一种如下图所示的导电性塑料:
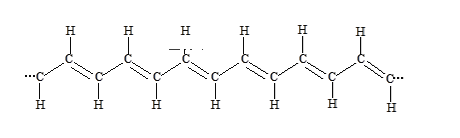
则合成该塑料的单体为___________ (填字母序号,下同);
A 乙炔 B 乙烯 C 乙烷 D 甲烷
②工业炼铁通常采用的方法是__________;
A 加热分解法 B 电解法 C 高温还原法
③某同学欲探究铁在NaCl溶液、蒸馏水和空气中锈蚀的快慢,设计了如下实验。
实验序号 | A | B | C |
实验 内容 |
|
|
|
一周后,试管中铁钉锈蚀程度最大的是__________;
④将质量相同的铁片、铜片用导线连接后浸入硫酸铜溶液中,构成原电池,工作一段时间后铜片质量与铁片质量相差12 g,则理论上导线中通过______mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素单质在碱性溶液中容易发生歧化反应,歧化的产物依反应温度的不同而不同。
Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
3Cl2+6OH-![]() 5Cl-+ClO3-+3H2O
5Cl-+ClO3-+3H2O
下图为制取氯气、氯酸钾、次氯酸钠和检验氯气性质的微型实验装置:

装置中盛装的药品如下:
①多用滴管中装有5 mL浓盐酸;②微型具支试管中装有1.5 g KMnO4;③微型具支试管中装有2~3 mL浓硫酸;④U形反应管中装有30% KOH溶液;⑤U形反应管中装有2 mol·L-1 NaOH溶液;⑥、⑦双U形反应管中分别装有0.1 mol·L-1 KI-淀粉溶液和KBr溶液;⑧尾气出口用浸有0.5 mol·L-1 Na2S2O3溶液的棉花轻轻覆盖住
(1)检查整套装置气密性的方法是________。
(2)为了使装置④⑤中的反应顺利完成,应该控制的反应条件分别为___________。
(3)装置⑥⑦中能够观察到的实验现象分别是_________。
(4)如果把装置⑥⑦中的试剂互换位置,则______(填“能”或“不能”)证明氧化性Cl2>I2,理由是_______。

(5)已知氯酸钾和氯化钾的溶解度曲线如图所示,反应结束后,从装置④所得溶液中提取氯酸钾晶体的实验操作是______________。
(6)尾气处理时Cl2发生反应的离子方程式为_________。
(7)选择微型实验装置的优点有___________(任答两点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10mL pH=4的盐酸中加水,稀释到100mL时,溶液pH为______;若加水稀释到1000mL时,溶液pH为________;若加水稀释到10000L时,溶液pH________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e是元素周期表中前四周期的元素,其原子序数依次增大,a为元素周期表中原子半径最小的元素,b的基态原子中占有电子的3个能级上的电子总数均相等,d与b同族,c与b同周期,且c的所有p轨道上的电子总数与所有s轨道上的电子总数相等,e的次外层电子数是其最外层电子的7倍。回答下列问题:
(1)c、d形成的化合物的晶体类型为___________;
(2)b、a c形成的三原子分子中,c原子的杂化方式为___________;
(3)b、c、d三种元素的电负性由小到大的顺序为___________;(用元素符号表示),d元素基态原子价层电子排布式为_________;
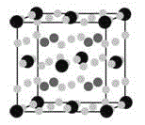
(4)金属Mg与a、e形成的化合物是目前人类已发现的体积储氢密度最高的储氢材料之一,其晶胞结构如图所示,其中黑球代表e,深灰色小球代表Mg,浅灰色小球代表a,其中浅灰色小球除在棱上、面上以外,在晶胞内部还有6个。试写出该化合物的化学式:__________________。
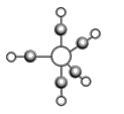
(5)b、c、e能形成如图所示三角双锥构型的配合物分子,三种元素的原子分别用大白球、小白球和灰色小球代表。该配合物形成配位键时提供空轨道的原子是___________(填元素符号),该配合物中大白球代表的元素的化合价为___________。
(6)①在水溶液中,水以多种微粒的形式与其他化合物形成水合物。试画出如下微粒的结构图式。H5O2+______________________
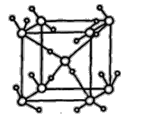
②如图为冰的一种骨架形式,依此为单位向空间延伸该冰中的每个水分子有___________个氢键;如果不考虑晶体和键的类型,哪一物质的空间连接方式与这种冰的连接类似_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】12.0g某液态有机化合物A完全燃烧后,生成14.4g H2O和26.4g CO2。测得有机化合物A的蒸气对H2的相对密度是30,求:
(1)有机物A的分子式_______________________。(写出计算过程)
(2)用如图所示装置测定有机物A的分子结构,实验数据如下(实验数据均已换算为标准状况):a mL(密度为ρ g/cm3)的有机物A与足量钠完全反应后,量筒液面读数为b mL,若1mol A分子中有x mol氢原子能跟金属钠反应,则x的计算式为____________(可以不化简,写出计算过程)。

(3)已知该有机物能够与金属钠或钾发生反应,并对有机物进行核磁共振操作,发现核磁共振氢谱图上有三组吸收峰,且峰面积之比为6:1:1,请写出该物质的结构简式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.碘化亚铁中通入过量氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
B.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓
C.1molL﹣1的NaAlO2溶液和2.5molL﹣1的HCl溶液等体积互相均匀混合:2AlO2﹣+5H+=Al3++Al(OH)3↓+H2O
D.用铜作电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7;p(Ni)=-lgc(Ni2+),p(B)=-lgc(S2-)或-lgc(CO32-)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是( )
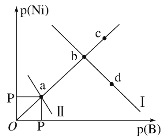
A.常温下NiCO3的溶解度大于NiS的溶解度
B.向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动
C.对于曲线Ⅰ,在b点加热,b点向c点移动
D.P为3.5且对应的阴离子是CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______(填序号,以下同),含有金属离子的物质是__,分子间可形成氢键的物质是________,属于离子晶体的是__,属于原子晶体的是__,①~⑤五种物质的熔点由高到低的顺序是__。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__。
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__;B.__;C.__D.____。
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com