
【题目】图中所示的装置图能够达到实验目的是
A.配制一定浓度的NaOH溶液
B.中和热的测定
C.加热熔融NaOH固体
D.测定高锰酸钾溶液的浓度
科目:高中化学 来源: 题型:
【题目】有一澄清透明的溶液,只可能含有大量的Fe3+、Fe2+、H+、AlO![]() 、Al3+、CO
、Al3+、CO![]() 、NO
、NO![]() 中的几种,向该溶液中逐滴加入一定量1 mol/L NaOH溶液,开始没有沉淀产生,而后才有沉淀产生。则下列判断正确的是( )
中的几种,向该溶液中逐滴加入一定量1 mol/L NaOH溶液,开始没有沉淀产生,而后才有沉淀产生。则下列判断正确的是( )
A.溶液中可能含有AlO![]()
B.溶液中可能含有NO![]()
C.溶液中一定不含Fe2+和Fe3+
D.溶液中可能含有Fe3+,但一定不含Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温,下列实验操作及现象与推论不相符的是( )
选项 | 操作及现象 | 推论 |
A | 用pH试纸测得0.1mol/LCH3COOH溶液pH约为3 | CH3COOH是弱电解质 |
B | 向某无色溶液中加入足量稀盐酸,产生无色无味气体;再将该气体通入澄清石灰水,产生白色浑浊 | 溶液中可能含有CO |
C | 用pH计测定相同浓度的CH3COONa溶液和NaClO溶液的pH,前者的pH小于后者的 | HClO的酸性弱于CH3COOH |
D | 向2mL1mol/LNaOH溶液中加入1mL0.1mol/LMgCl2溶液,产生白色沉淀;再加入1mL0.1mol/LFeCl3溶液,产生红褐色沉淀 | Mg(OH)2沉淀转化为Fe(OH)3沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯气相直接水合反应制备乙醇:C2H4(g)+H2O(g) ![]() C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如下(起始时,n(H2O)=n(C2H4)=1 mol,容器体积为1 L)。下列分析不正确的是( )
C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如下(起始时,n(H2O)=n(C2H4)=1 mol,容器体积为1 L)。下列分析不正确的是( )
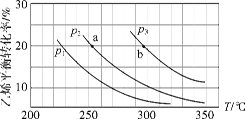
A.乙烯气相直接水合反应的H<0
B.图中压强的大小关系为:p1>p2>p3
C.图中a点对应的平衡常数K =![]()
D.达到平衡状态a、b所需要的时间:a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,加少量烧碱溶液可使溶液中
CH3COO-+H+,加少量烧碱溶液可使溶液中![]() 值增大
值增大
B.25 ℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O![]() H++OH-逆向移动,c(H+)降低
H++OH-逆向移动,c(H+)降低
C.取c(H+)=0.01 mol·L-1的盐酸和醋酸各100 mL,分别稀释2倍后,再分别加入0.3 g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3- )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20 mL NaOH溶液中逐滴加入0.1 mol/L醋酸溶液,滴定曲线如图所示。下列判断正确的是( )

A.在M点,两者恰好反应完全
B.滴定前,酸中c(H+) 等于碱中c(OH﹣)
C.NaOH溶液的物质的量浓度为0.1 mol/L
D.在N点,溶液中的c(CH3COO﹣)=c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定容积的密闭容器中,可发生以下反应:A(g)+B(g)![]() xC(g);H=?符合下图(a)所示的关系。w(c)为C的质量分数,由此推断关于图(b)的说法正确的是
xC(g);H=?符合下图(a)所示的关系。w(c)为C的质量分数,由此推断关于图(b)的说法正确的是

A.P3>P4,y轴表示A的转化率
B.P3<P4,y轴表示B的体积分数
C.P3<P4,y轴表示混合气体的平均相对分子质量
D.P3>P4,y轴表示混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俗称“一滴香”的物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )

A.该有机物的分子式为C8H8O3
B.1mo1该有机物最多能与2molH2发生加成反应
C.该有机物能发生取代、加成和氧化反应
D.该有机物能与碳酸氢钠反应生成CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素X、Y、Z、W,原子序数依次增大,X原子核外有6种不同运动状态的电子;Y原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;W位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
(1)X位于周期表的第__________________周期,第__________________族。
(2)元素的第一电离能:X__________________Y(填“>”或“<”,下同);原子半径:X__________________Y。
(3)Y的最高价氧化物对应水化物中酸根离子的空间构型__________________(用文字描述)。
(4)Z3+基态核外电子排布式为__________________,用硫氰化钾溶液检验Z3+的离子方程式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com