
【题目】Fe、Mg、Al分别跟稀盐酸充分反应得到相同质量的氢气,其原因是( )
①Fe、Mg、Al的物质的量相等,盐酸足量;
②Fe、Mg、Al的质量比是56∶24∶27,盐酸足量;
③Fe、Mg、Al的质量比是28∶12∶9,盐酸足量;
④Fe、Mg、Al均过量,所用盐酸的浓度和体积都相同。
A. ①② B. ①③ C. ②③ D. ③④
【答案】D
【解析】
Fe、Mg、Al三种金属分别跟稀盐酸反应的化学方程式为:Fe![]() 2HCl=FeCl2
2HCl=FeCl2![]() H2
H2![]() ,Mg
,Mg![]() 2HCl=MgCl2
2HCl=MgCl2![]() H2
H2![]() ,2Al
,2Al![]() 6HCl═2AlCl3
6HCl═2AlCl3![]() 3H2
3H2![]() ,由此可以知道,产生氢气的是盐酸中的氢离子,故要得到相同质量的氢气有两种情况:(1)参与反应的HCl的质量相等;(2)参与反应的Fe、Mg、Al的质量符合得到相同质量的氢气的条件。
,由此可以知道,产生氢气的是盐酸中的氢离子,故要得到相同质量的氢气有两种情况:(1)参与反应的HCl的质量相等;(2)参与反应的Fe、Mg、Al的质量符合得到相同质量的氢气的条件。
(1)因为产生氢气的是盐酸中的氢离子,故参与反应的HCl的质量相等,产生的氢气的质量就相等.故(4)符合;
(2)假设Fe、Mg、Al三种金属分别跟稀盐酸充分反应,得到氢气的质量都是2g,
设参与反应的Fe的质量为x,Mg的质量为y,Al的质量为z,
Fe![]() 2HCl=FeCl2
2HCl=FeCl2![]() H2
H2![]() ,
,
56 2
x 2g 解得x=56g;
Mg![]() 2HCl==MgCl2
2HCl==MgCl2![]() H2
H2![]()
24 2
y 2g 解得y=24g;
2Al![]() 6HCl==2AlCl3
6HCl==2AlCl3![]() 3H2
3H2![]()
54 6
z 2g 解得z=18g
故Fe、Mg、Al的质量比为:![]() 。故(3)符合;(1)(2)不符合;
。故(3)符合;(1)(2)不符合;
本题答案为D


科目:高中化学 来源: 题型:
【题目】取7.90gKMnO4,加热分解后剩余固体7.42g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以Mn2+存在。
请计算:
(1)KMnO4的分解率_______________。
(2)气体A的物质的量_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。
(1)“石灰干燥剂”的主要成分石灰是______________(填化学式),石灰所属的物质类型__________________(填序号)。
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂 ⑤纯净物 ⑥化合物 ⑦盐
(2)生石灰可做干燥剂的理由是________________________(用化学方程式表示)。
(3)你认为下列内容还必须在这种小纸袋上注明的是____________(填序号)。
①禁止食用 ②可以食用 ③禁止未成年人用手拿 ④生产日期
(4)小纸袋中的物质能否长期地作干燥剂?为什么?_______________________________。
(5)某同学将浓硫酸、氢氧化钠固体、生石灰等物质划分为一类。该同学的分类依据为____________(填字母)。
A. 酸类 B. 碱类 C. 氧化物 D. 干燥剂
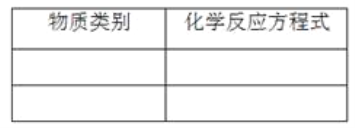
(6)生石灰还可以跟哪些类别的物质发生化学反应?请列举三例并填表。__________________、__________________、__________________、__________________、__________________、__________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐中常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为________(只填化学式)。
②分离操作①中所用到的玻璃仪器有____________。
③洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为________。
(2)用提纯的NaCl配制450 mL 4.00 mol·L-1NaCl溶液,所用仪器除药匙、烧杯、玻璃棒外还有________(填仪器名称)。
(3)在实验中多次用到玻璃棒,其作用有三个,分别是______________、______________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定Na2CO3和NaHCO3混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度盐酸30.0 mL,充分反应,产生CO2的体积(已折算成标准状况下的体积,不考虑CO2在水中的溶解)如下表:
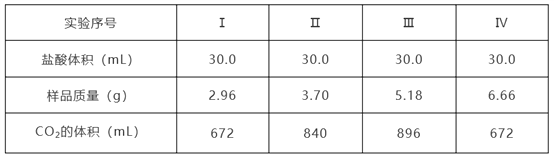
(1)样品中物质的量之比n(Na2CO3):n(NaHCO3)=_________。
(2)盐酸的物质的量浓度c(HCl)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不合理的是( )




![]()
A. 用a制备并收集氨气 B. 用b制备并检验乙炔
C. 用c蒸馏海水得到淡水 D. 用d分离Na2CO3溶液与植物油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用图甲装置制取氨气并探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用__(填序号)。
a.碱石灰 b.浓硫酸 c.五氧化二磷 d.氯化钙
(2)若探究氨气的溶解性,当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是__。不能在K2的导管末端连接图乙中的__装置(填序号)。
(3)若探究氨气的还原性,需关闭K1、K3,K2连接纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成的气体必须依次通过盛有__试剂和__试剂的洗气瓶。
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为__。
③尾气可用C装置处理,若尾气中含有少量Cl2,则C装置中应盛放__溶液(填化学式),反应的离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由钠、镁、铝、铁四种金属单质中的两种组成的合金共24g,跟足量的盐酸反应产生11.2L氢气(标准状况),那么此合金中一定含有的金属是
A. Na B. Mg C. Al D. Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如图.下列关于分枝酸的叙述正确的是( )

A. 分子中含有5种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且反应类型相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com