下列反应的离子方程式正确的是( )
A.向100mL0.1mol/LFeBr2溶液中通入0.025mol的Cl2,充分反应2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-
B.向Fe(NO3)3溶液中加入过量的HI溶液2NO3-+8H++6I-═3I2+2NO↑+4H2O
C.将碳与足量的浓硫酸共热反应后的气体混合物,通入过量氢氧化钠溶液中CO2+SO2+4OH-═SO32-+CO32-+2H2O
D.将等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合HCO-3+Ba2++OH-═BaCO3↓+H2O
【答案】
分析:A、FeBr
2的物质的量为0.01mol,Cl
2为0.025mol,发生的反应分别为:2Fe
2+Cl
2═2Fe
3++2Cl
-,2Br
-+Cl
2═2Cl
-+2Br
2,以此判断二者反应的程度并判断离子方程式的正误;
B、从Fe
3+离子的氧化性考虑,加入过量HI溶液,Fe
3+被还原为离子Fe
2+;
C、从将碳与浓硫酸共热反应后生成CO
2和SO
2气体的物质的量关系判断离子方程式的正误,反应方程式为:
C+2H
2SO
4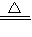
CO
2↑+2SO
2↑+2H
2O;
D、从加入物质的物质的量分析反应的情况,以此判断离子方程式的正误.
解答:解:A、FeBr
2的物质的量为0.01mol,Cl
2为0.025mol,根据发生的反应:2Fe
2+Cl
2═2Fe
3++2Cl
-,2Br
-+Cl
2═2Cl
-+2Br
2,可知氯气过量,故反应的离子方程式为:2Fe
2++4Br
-+3Cl
2═2Fe
3++2Br
2+6Cl
-,故A正确;
B、Fe
3+离子具有强氧化性,加入过量HI溶液,Fe
3+与HI发生氧化还原反应被还原为离子Fe
2+,本题不符合反应实际,故B错误;
C、将碳与浓硫酸共热反应方程式为:C+2H
2SO
4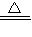
CO
2↑+2SO
2↑+2H
2O,生成CO
2和SO
2气体的物质的量之比为1:2,正确的离子方程式应为CO
2+2SO
2+6OH
-=2SO
2-3+CO
32-+3H
2O,故C错误;
D、等体积等物质的量浓度的NaHCO
3溶液与Ba(OH)
2溶液中,NaHCO
3和Ba(OH)
2物质的量相等,涉及反应有:
HCO
-3+OH
-=CO
32-↓+H
2O;CO
32-+Ba
2+=BaCO
3↓,总反应为:HCO
-3+Ba
2++OH
-=BaCO
3↓+H
2O,故D正确.
故选AD.
点评:本题考查离子方程式的正误判断,做题时注意物质的氧化性、还原性以及参加反应的物质的物质的量并以此判断反应的程度是做题的关键.本题难度中.

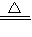 CO2↑+2SO2↑+2H2O;
CO2↑+2SO2↑+2H2O;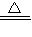 CO2↑+2SO2↑+2H2O,生成CO2和SO2气体的物质的量之比为1:2,正确的离子方程式应为CO2+2SO2+6OH-=2SO2-3+CO32-+3H2O,故C错误;
CO2↑+2SO2↑+2H2O,生成CO2和SO2气体的物质的量之比为1:2,正确的离子方程式应为CO2+2SO2+6OH-=2SO2-3+CO32-+3H2O,故C错误;

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案