


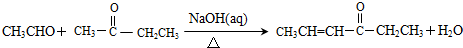
 ,其反应类型是加成反应.
,其反应类型是加成反应.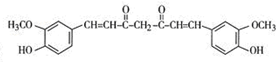 .
. .
.分析 乙烯和溴发生加成反应生成A为BrCH2CH2Br,由E的结构简式及D的分子式可知,D为OHC-COOH,结合C的分子式可知,C为OHC-CHO,根据转化关系可推得B为HOCH2CH2OH,A发生碱性水解得B,所以试剂X为NaOH水溶液,B发生氧化反应得C,C氧化得D,D发生加成反应得E,根据G的分子式可知,F发生反应生成G为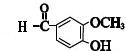 ,根据姜黄素的分子式可知,G发生成信息②中的反应得姜黄素为
,根据姜黄素的分子式可知,G发生成信息②中的反应得姜黄素为 ,据此解答.
,据此解答.
解答 解:乙烯和溴发生加成反应生成A为BrCH2CH2Br,由E的结构简式及D的分子式可知,D为OHC-COOH,结合C的分子式可知,C为OHC-CHO,根据转化关系可推得B为HOCH2CH2OH,A发生碱性水解得B,所以试剂X为NaOH水溶液,B发生氧化反应得C,C氧化得D,D发生加成反应得E,根据G的分子式可知,F发生反应生成G为 ,根据姜黄素的分子式可知,G发生成信息②中的反应得姜黄素为
,根据姜黄素的分子式可知,G发生成信息②中的反应得姜黄素为 ,
,
(1)A为BrCH2CH2Br,A的名称为1,2-二溴乙烷,试剂X名称为 NaOH水溶液,
故答案为:1,2-二溴乙烷;NaOH水溶液;
(2)D为OHC-COOH,D中含有的官能团名称 醛基、羧基,
故答案为:醛基、羧基;
(3)反应D→E的化学方程式为  ,其反应类型是 加成反应,
,其反应类型是 加成反应,
故答案为: ; 加成反应;
; 加成反应;
(4)G为 ,
,
a.G中没有羧基,不能与NaHCO3溶液反应,故a错误;
b.G中苯环上的氢能被溴取代,故b正确;
c.G中有酚羟基,能与FeCl3溶液发生显色反应,故c正确;
d.G中有一个醛羟基和一个苯环,1molG最多能与4molH2发生加成反应,故d错误,
故选ad;
(5)根据上面的分析可知,姜黄素的结构简式为 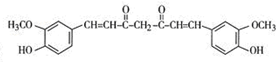 ,
,
故答案为: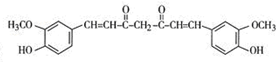 ;
;
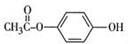
(6)G为 ,根据条件①苯环上的一取代物只有2种,即有两上取代基位于苯环的对位;②核磁共振氢谱中有4组吸收峰,即有四种位置的氢原子;③1mol该物质与烧碱溶液反应,最多消耗3molNaOH,说明有三个羧基或酚羟基,或水解产生羧基和酚羟基,则符合条件的G(C8H8O3)的同分异构体为
,根据条件①苯环上的一取代物只有2种,即有两上取代基位于苯环的对位;②核磁共振氢谱中有4组吸收峰,即有四种位置的氢原子;③1mol该物质与烧碱溶液反应,最多消耗3molNaOH,说明有三个羧基或酚羟基,或水解产生羧基和酚羟基,则符合条件的G(C8H8O3)的同分异构体为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断,涉及反应类型的判断、反应方程式的书写、同分异构体的判断等知识点,明确物质含有的官能团及断键和成键方式是解本题关键,注意结合题给信息进行推断,难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化石燃料属于可再生能源,不影响可持续发展 | |
| B. | 开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料 | |
| C. | 煤的气化技术在一定程度上实现了煤的高效、清洁利用 | |
| D. | 氢气燃烧热高,其燃烧产物是水,是一种理想的清洁燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
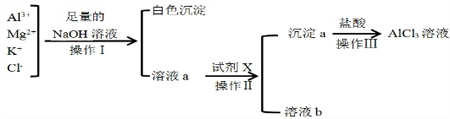 某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失
某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失查看答案和解析>>
科目:高中化学 来源: 题型:解答题
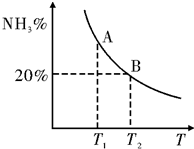 合成氨技术的发明使工业化人工固氮成为现实.
合成氨技术的发明使工业化人工固氮成为现实.| 温度/℃ CO2转化率% $\frac{n(N{H}_{3})}{n(C{O}_{2})}$ | 100 | 150 | 200 |
| 1 | 19.6 | 27.1 | 36.6 |
| 1.5 | a | b | c |
| 2 | d | e | f |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述三个反应都有单质生成,所以都是置换反应 | |
| B. | 氧化性由强到弱的顺序为KBrO3>KClO3>Cl2>Br2 | |
| C. | 反应②中氧化剂与还原剂的物质的量之比为1:6 | |
| D. | 反应③中1mol还原剂反应,则氧化剂得到电子的物质的量为2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在体积可变的密闭容器中发生可逆反应 A(g)+B(g)?C(g)+D(g),当混合气体的密度不再改变时,说明反应已达到化学平衡状态 | |
| B. | 对于反应 C(s)+CO2(g)?2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率可能减小 | |
| C. | 向 0.1 mol•L-1的氨水中加入氯化铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}0)}$增大 | |
| D. | 常温下,向 Mg(OH)2悬浊液中加入 MgCl2浓溶液后,溶液中$\frac{c(M{g}^{2+})•c(O{H}^{-})}{c({H}^{+})}$不变(一定温度下,Mg(OH)2悬浊液中 c(Mg2+)﹒c2(OH-)为定值) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+H2O═Na++OH-+O2↑ | |
| B. | 氯化铁溶液和氢氧化钠溶液反应:Fe3++3OH-═Fe(OH)3↓ | |
| C. | 氯化铝溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 碳酸钙与稀盐酸反应:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com