
| A、同体积、同密度的CO和CO2气体 |
| B、同温度、同体积的O2和O3气体 |
| C、同压强、同体积的N2O和CO2气体 |
| D、同质量、不同密度的O2和O3 气体 |
| m |
| M |
| m |
| M |


科目:高中化学 来源: 题型:
| A、Al2O3、Fe2O3都能和酸反应生成盐和水,故都是碱性氧化物 |
| B、CO、NO、SO2都是大气污染气体,在空气中都能稳定存在 |
| C、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液变红 |
| D、Na2O与Na2O2中,阴阳离子之比相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下将pH=2的醋酸和pH=12的NaOH溶液等体积混合,所得溶液显碱性 |
| B、已知同温时氢氟酸的电离常数大于亚硝酸的电离常数,则相同温度相同浓度的NaF溶液和NaNO2溶液的碱性:NaF溶液较强 |
| C、将等体积的盐酸和氨水混合,充分反应后所得溶液呈中性,则两溶液的物质的量浓度关系为:c(HCl)<c(NH3?H2O) |
| D、常温下,pH均为5的醋酸和硫酸铝溶液,由水电离出的氢离子浓度均为1×10-9 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知2H2(g)+O2(g)2H2O(g);△H=483.6kJ/mol,则氢气的燃烧热为241.8kJ |
| B、在测定中和热的实验中,盐酸物质的量一般要大于氢氧化钠物质的量,这样才能保证氢氧化钠中和完全 |
| C、已知碳的燃烧热为 y KJ/mol,当7.2 g 的碳在12.8 g 的氧气中燃烧,至反应物耗尽并放出x KJ 的热量,则可求出 1 mol 碳与氧气反应生成一氧化碳时△H=(0.5 y-2.5x)KJ/mol |
| D、己知2C(s)+2O2(g)=CO2(g);△H1 2C(s)+O2(g)=CO(g);△H2 则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
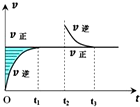 某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )
某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )| A、Z和W在该条件下一定不为气态 |
| B、t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C、若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等 |
| D、若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、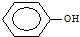 和 和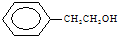 |
| B、最简式相同的有机物 |
| C、丙酸丙酯和高级脂肪甘油脂 |
| D、分子组成为CnH2n+2和CmH2m+2(m≠n)的两种烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化剂只有CuSO4 |
| B、Cu2S 既是氧化剂又是还原剂 |
| C、被氧化的硫与被还原的硫的质量比为3:7 |
| D、14mol CuSO4可氧化5mol FeS2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com