
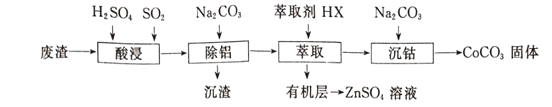
【题目】CoCO3可用作选矿剂、催化剂及家装涂料的颜料。以含钴废渣(主要成CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
下表是相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol/L计算):
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Co2+ | 7.6 | 9.4 |
Al3+ | 3.0 | 5.0 |
Zn2+ | 5.4 | 8.0 |
(1)写出“酸溶”时发生氧化还原反应的化学方程式____________________。
(2)“除铝”过程中需要调节溶液pH的范围为_______________ 。
(3)在实验室里,萃取操作用到的玻璃仪器主要有____;上述“萃取”过程可表示为ZnSO4(水层)+2HX(有机层) ![]() ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是______。
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是______。
(4)简述洗涤沉淀的操作____________________________________。
(5)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为 ____________________。
【答案】Co2O3+SO2+H2SO4=2CoSO4+H2O 5.0~5.4 分液漏斗、烧杯 向有机层中加入适量的硫酸溶液充分振荡,静置,分离出水层 向漏斗中加蒸馏水至没过沉淀,待水自然流完后,重复上述操作2-3次 Co3O4
【解析】
(1)从最终产物看,酸溶时,Co2O3被还原为Co2+,SO2被氧化为SO42-,
“酸溶”时发生氧化还原反应的化学方程式Co2O3+SO2+H2SO4=2CoSO4+H2O。
答案为:Co2O3+SO2+H2SO4=2CoSO4+H2O
(2)“除铝”过程中需要调节溶液pH的范围,目的是让Al3+全部转化为沉淀,而Zn2+不生成沉淀,所以pH的范围应为5.0~5.4。答案为:5.0~5.4
(3)在实验室里,萃取操作用到的玻璃仪器主要有分液漏斗、烧杯。
答案为:分液漏斗、烧杯
上述“萃取”过程可表示为ZnSO4(水层)+2HX(有机层) ![]() ZnX2(有机层)+H2SO4(水层),从反应中可以看出,此反应为可逆反应,所以加硫酸可实现让ZnSO4进入水层的目的。从而得出由有机层获取ZnSO4溶液的操作是向有机层中加入适量的硫酸溶液充分振荡,静置,分离出水层。
ZnX2(有机层)+H2SO4(水层),从反应中可以看出,此反应为可逆反应,所以加硫酸可实现让ZnSO4进入水层的目的。从而得出由有机层获取ZnSO4溶液的操作是向有机层中加入适量的硫酸溶液充分振荡,静置,分离出水层。
答案为:向有机层中加入适量的硫酸溶液充分振荡,静置,分离出水层
(4)洗涤沉淀的操作是:向漏斗中加蒸馏水至没过沉淀,待水自然流完后,重复上述操作2-3次。
答案为:向漏斗中加蒸馏水至没过沉淀,待水自然流完后,重复上述操作2-3次。
(5)从化学式CoCO3可以看出,n(Co)=n(C)=![]() ,
,
m(Co)=0.03mol×59g/mol=1.77g
m(O)=2.41g-1.77g=0.64g
n(O)=![]()
n(Co):n(O)= 0.03mol:0.04mol=3:4
则该钴氧化物的化学式为Co3O4。
答案为:Co3O4


科目:高中化学 来源: 题型:
【题目】在一定条件下,某些不饱和烃分子之间可以进行自身的加成反应,如:CH≡CH+CH≡CH→CH≡C-CH=CH2,现有有机物甲,其结构式为: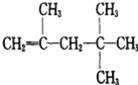 ,它是由不饱和烃乙的两个分子在一定条件下发生自身加成而得,在此反应中,除获得甲外,同时还获得了另一产物丙,丙是甲的同分异构体,则:乙的结构简式为________,丙的结构简式为_________。
,它是由不饱和烃乙的两个分子在一定条件下发生自身加成而得,在此反应中,除获得甲外,同时还获得了另一产物丙,丙是甲的同分异构体,则:乙的结构简式为________,丙的结构简式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某同学设计的用于鉴别苯和苯的同系物的几种方法或试剂,其中最适合的是( )
A. 液溴和铁粉B. 浓溴水
C. 酸性KMnO4溶液D. 在空气中点燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于烷烃的表述正确的是( )
A.乙烷的结构式为CH3CH3
B.C5H12分子的某种结构为CH3CH2(CH3)CH2CH3
C.CH3CH2CH(C2H5)CH2CH2CH3与CH3CH2CH2CH(C2H5)CH2CH3互为同分异构体
D.C4H10的一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。常用的自来水消毒剂有二氧化氯(ClO2)和高铁酸钾(K2FeO4)等。
(1)某研究小组用下图装置制备少量ClO2(夹持装置已略去)。
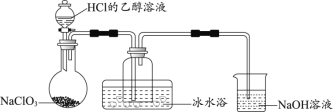
资料:ClO2常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,11℃时液化成红棕色液体。以NaClO3和HCl的乙醇溶液为原料制备ClO2的反应为2NaClO3 + 4HCl= 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O。
①冰水浴的作用是____________。
② NaOH溶液中发生的主要反应的离子方程式为________________。
(2)将ClO2水溶液滴加到KI溶液中,溶液变棕黄;再向其中加入适量CCl4,振荡、静置,观察到____,证明ClO2具有氧化性。
(3)ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO2-),需将其转化为Cl-除去。下列试剂中,可将ClO2-转化为Cl-的是_____________________(填字母序号)。
a. FeSO4 b. O3 c. KMnO4 d. SO2
(4)K2FeO4是一种新型、绿色的多功能净水剂,集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭等性能为一体。实验室制备K2FeO4的方法如下:在冰水浴中,向KClO和KOH的混合溶液中少量多次加入硝酸铁,并不断搅拌。
①上述制备K2FeO4反应的离子方程式为______________________。
②净水过程中,K2FeO4起到吸附、絮凝作用的原理是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间通过一步反应不能实砚如下图所示转化的是
选项 | X | Y | Z |
A | Na | NaOH | NaCl |
B | Si | SiO2 | Na2SiO3 |
C | Cl2 | HClO | NaClO |
D | NO | NO2 | HNO3 |

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所使用的装置(部分夹持装置略)、试剂和操作方法都正确的是 ( )
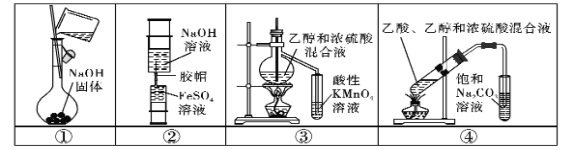
A.用装置①配制250 mL0.1 mol.L-1的NaOH溶液
B.用装置②制备少量Fe(OH)2固体
C.用装置③验证乙烯的生成
D.用装置④制取少量乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素硼对植物生长及人体健康有着十分重要的作用,也广泛应用于新型材料的制备。
(1)基态硼原子的价电子轨道表达式是________。与硼处于同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为______。
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的____。
(3)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
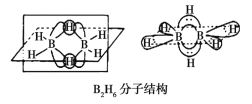
①B2H6分子结构如图,则B原子的杂化方式为__________
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是__________,写出一种与氨硼烷互为等电子体的分子_________(填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。BH4-的立体构型为__________________。
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。
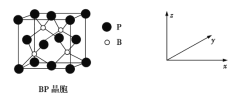
磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数的数值。下列说法正确的是
A.1 mol OH—含有的电子数为NA
B.将7.1 g Cl2通入水中,转移电子数为0.1NA
C.标准状况下,11.2 L O2、CO2混合气体含有的氧原子数为NA
D.1 L 0.1 mol·L-1 NH4Cl溶液中,含有的NH![]() 数为0.1NA
数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com