
【题目】将2 mol SO2和2 mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g) ![]() 2SO3(g),平衡时,SO3为n mol,相同温度下,分别按下列配比在相同容积的密闭容器中放入起始物质,平衡时,SO3的物质的量大于n mol的是( )
2SO3(g),平衡时,SO3为n mol,相同温度下,分别按下列配比在相同容积的密闭容器中放入起始物质,平衡时,SO3的物质的量大于n mol的是( )
A. 2 mol SO2和1 mol O2B. 4 mol SO2和1 mol O2
C. 2 mol SO2、1 mol O2和2 mol SO3D. 2 mol SO3
【答案】C
【解析】
2SO2(g)+O2(g) ![]() 2SO3(g)
2SO3(g)
初始:2mol 2mol
反应:2-n (2-n)/2 2-n
平衡:4-n (2-n)/2 n
A.起始量进行等效处理后和题目所给起始量相比,相当于减少2molSO2,减少反应物二氧化硫的量,平衡逆向进行,n(SO3)<n,A错误;
B.起始量进行等效处理后与题中给定起始量相同,平衡时完全相同,SO3物质的量为n mol,B错误;
C.起始量相当于加入4molSO2和2molO2,相当于在原平衡的基础上加入1molO2,平衡正向移动, n(SO3)>nmol, C正确;
D.起始充入2molSO3,相当于起始加入了2molSO2和1molO2,减少反应物二氧化硫的量,平衡逆向进行,消耗三氧化硫,平衡逆移,,n(SO3)<nmol,D错误;
答案为C


科目:高中化学 来源: 题型:
【题目】32g铜与150mL一定浓度的硝酸恰好完全反应,产生的NO2和NO混合气体在标准状况下的体积为11.2L.请回答:(不要求写计算过程)
(1)写出铜与稀硝酸反应的化学方程式________________。
(2)NO为_________ mol.标准状况V(NO):V(NO2)=________
(3)原硝酸溶液的浓度为__________ molL-1 。
(4)试描述实验过程中试管内产生气体现象___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积固定为a L的密闭容器中充入1 mol X气体和2 mol Y气体,发生反应X(g)+2Y(g) ![]() 2Z(g),此反应达到平衡状态的标志是( )
2Z(g),此反应达到平衡状态的标志是( )
A. 容器内气体密度不随时间变化 B. 容器内各物质的浓度不随时间变化
C. 容器内X、Y、Z的浓度之比为1∶2∶2 D. 单位时间内消耗0.1 mol X,同时生成0.2 mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列物质分类全部正确的是
①纯碱 ②食盐水 ③石灰水 ④氢氧化钠 ⑤液态氧 ⑥氯酸钾
A. 碱——①④ B. 纯净物——③④⑤
C. 盐——①⑥ D. 混合物——②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,体积不变的密闭容器中有可逆反应A(g)+ B(g) ![]() 2C(g)+D(s),可以判断反应达到平衡是( )
2C(g)+D(s),可以判断反应达到平衡是( )
A. 单位时间内反应nmol B同时生成2nmol C
B. 容器内气体的物质的量不再变化
C. A的生成速率与B的生成速率相等
D. 容器内气体的密度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组大小顺序不正确的是
A. 酸性:H2SiO3﹤H3PO4﹤H2SO4 B. 热稳定性:H2Se﹤H2S﹤H2O
C. 还原性:HI﹥HBr﹥HCl D. 金属的还原性:Na﹤Mg﹤Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2(g)+ O2(g) = 2H2O(g),H—H、O=O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则2mol H2完全燃烧放出的热量为
A. 480 kJ B. 916 kJ C. 960 kJ D. 190 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.用金属钠可区分乙醇和乙醚B.用高锰酸钾酸性可区分乙烷和3-己烯
C.用水可区分苯和溴苯D.用新制的银氨溶液可区甲酸甲酯和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.00 mL 0.1 mol·L-1 C6H5COOH(苯甲酸)溶液中滴加0.1 mol·L-1 NaOH溶液,溶液中离子浓度与pH关系如图所示。下列说法正确的是
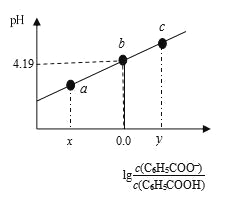
A. a点:溶液中c(Na+)>c(C6H5COO-)>c(H+)>c(OH-)
B. b点:对应的NaOH溶液体积为10 mL
C. 对b点溶液加热(不考虑挥发),实现曲线由b点向c点的变化
D. 298K时,C6H5COOH的电离常数为1×10-4.19
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com