
【题目】我国科学家构建了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐。下列说法正确的是

A.a为正极
B.左池电极反应式为C6H6O+11H2O-28e-=6CO2↑+28H+
C.若右池产生0.672L气体(标况下),则转移电子0.15mol
D.左池消耗的苯酚与右池消耗的NO3-的物质的量之比为28:5
【答案】B
【解析】
试题A、a端是苯酚转化为二氧化碳,C元素的化合价升高,发生氧化反应,所以a为负极,错误;B、左池为苯酚的氧化反应,失去电子生成二氧化碳和氢离子,正确;C、若右池产生0.672L气体(标况下),则生成氮气的物质的量是0.672L/22.4L/mol=0.03mol,N元素的化合价从+5价降低到0价,则转移电子的物质的量是0.03mol×2×5=0.3mol,错误;D、左池消耗1mol苯酚,则转移28mol电子,而右池转移28mol电子时,则消耗硝酸根离子的物质的量是28/5mol,则左池消耗的苯酚与右池消耗的NO3-的物质的量之比为1:28/5=5:28,错误,答案选B。


科目:高中化学 来源: 题型:
【题目】用系统命法写出下列物质名称或结构简式
(1) __________
__________
(2) ____________
____________
(3)![]() ___________
___________
(4)![]() ____________
____________
(5)2,6-二甲基-4-乙基辛烷_______
(6)2-甲基-1-戊烯____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池可净化废水,同时还能获得能源或有价值的化学产品,图为其工作原理和废水中Cr2O72-离子浓度与去除率的关系。下列说法正确的是
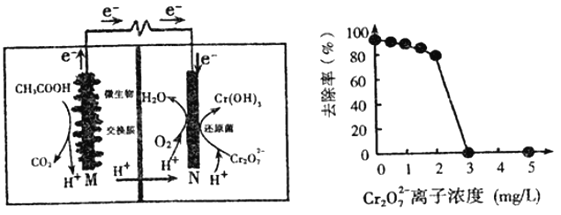
A. 反应一段时间后,N极附近的溶液pH下降
B. 外电路转移4mol电子时,M 极产生22.4LCO2
C. Cr2O72-离子浓度较大时,可能会造成还原菌失活
D. M为电池正极,CH3COOH被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某甲烷燃料电池构造示意图如下,关于该电池的说法不正确的是

A. 电解质溶液中Na+向b极移动
B. b极的电极反应是:O2+2H2O+4e-=4OH-
C. a极是负极,发生氧化反应
D. 电子通过外电路从b电极流向a电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s) ![]() 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表,下列说法错误的是
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表,下列说法错误的是
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度/10-3 mol·L-1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A. 当混合气体平均相对分子质量为26时说明该反应已达平衡
B. 达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增大
C. 根据表中数据,计算15.0 ℃时的分解平衡常数约为2.0×10-9
D. 因该反应熵变(ΔS)大于0,焓变(ΔH)大于0,所以在高温下自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.CO2溶于水得到的溶液能导电,则CO2属于电解质
B.电离需要通电才能进行
C.氯化氢的水溶液能导电,液态氯化氢不能导电
D.NaCl晶体不能导电,所以NaCl是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在水溶液中的电离方程式书写正确的是
A.KClO3=K++3O2—+Cl5+B.NaHSO4= Na++HSO4—
C.H2SO4=H++ SO42—D.Al2(SO4)3= 2Al3++3SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业生产甲醇的常用方法是CO(g)+2H2(g)===CH3OH(g) ΔH=-90.8 kJ·mol-1。已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1,H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1。
①H2的燃烧热ΔH=___________kJ·mol-1。
②CH3OH(g)+O2(g)=CO(g)+2H2O(g)的反应热ΔH=________________。
(2)工业上利用甲醇制备氢气常用方法之一是甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)=CO(g)+2H2(g),此反应能自发进行的原因是______________。
Ⅱ.铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):

(1)放电时:正极的电极反应式是________________;当外电路通过1 mol电子时,理论上正极板的质量增加___g。
(2)在完全放电耗尽PbO2和Pb时,若按图连接,电解一段时间后,则在A电极上生成___、B电极上生成____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。下列叙述中不正确的是:
A. 此时水的离子积Kw=1×10-14 B. 水电离出的c(H+)=1×10-10molL-1
C. 水的电离程度随温度升高而增大 D. c(Na+)=c(SO42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com