
【题目】碳、镁、镍在工业生产和科研领域有广泛用途。请回答下列问题:
(1)基态碳原子中,能量最高的电子所占用的能级符号为_________;该能级中原子轨道的电子云形状为______________________。
(2)从石墨中可剥离出由单层碳原子构成的石墨烯,石墨烯中碳原子和共价键的数目之比为________。
(3)Mg2+能形成多种配合物和配离子,如Na4[Mg(PO3)4]、Mg[EDTA]2- EDTA的结构简式为( )等。
)等。
①PO3-的立体构型为____________,其中心原子的杂化轨道类型为__________,其中杂化轨道的作用为__________________________。
② 是常用的分析试剂。其中位于同周期的三种基态原子第一电离能由小到大的顺序为________________(用元素符号表示);这三种元素形成的一种离子与CS2互为等电子体,该离子符号为_____________。
是常用的分析试剂。其中位于同周期的三种基态原子第一电离能由小到大的顺序为________________(用元素符号表示);这三种元素形成的一种离子与CS2互为等电子体,该离子符号为_____________。
(4)晶体镁的堆积模型为____________;其中镁原子的配位数为______________。
(5)碳、镁、镍形成的某晶体的晶胞结构如图所示。若晶体密度为ρg·cm-1,阿伏伽德罗常数的值为NA,则晶胞参数a=___________pm(用代数式表示)。

【答案】 2p 哑铃形(或纺锤形) 2:3 平面三角形 sp2 形成α键 C<O<N CNO- 六方最密堆积 12 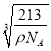
![]() 1010
1010
【解析】(1)基态碳原子核外有2个电子层,能量最高的电子所占用的能级符号为2p;该能级中原子轨道的电子云形状为纺锤形,故答案为:2p;纺锤形;
(2)石墨烯中每个碳原子与周围的3个碳原子通过共价键结合,每个碳原子含有![]() 个共价键,因此碳原子和共价键的数目之比为1:
个共价键,因此碳原子和共价键的数目之比为1: ![]() =
=![]() ,故答案为:
,故答案为: ![]() ;
;
(3)①PO3-中P原子的价层电子对数=3+![]() ×(5+1-2×3)=3,P原子采用sp2杂化,立体构型为平面三角形,其中杂化轨道形成σ键,故答案为:平面三角形; sp2;形成σ键;
×(5+1-2×3)=3,P原子采用sp2杂化,立体构型为平面三角形,其中杂化轨道形成σ键,故答案为:平面三角形; sp2;形成σ键;
② 是常用的分析试剂。其中位于同周期的三种基态原子为C、N、O,由于N原子的2p为半充满结构,较为稳定,第一电离能由小到大的顺序为C<O<N;这三种元素形成的一种离子与CS2互为等电子体,该离子为CNO-,故答案为:C<O<N ;CNO-;
是常用的分析试剂。其中位于同周期的三种基态原子为C、N、O,由于N原子的2p为半充满结构,较为稳定,第一电离能由小到大的顺序为C<O<N;这三种元素形成的一种离子与CS2互为等电子体,该离子为CNO-,故答案为:C<O<N ;CNO-;
(4)晶体镁的堆积模型为六方最密堆积;其中镁原子的配位数为12,故答案为:六方最密堆积;12;
(5)该晶胞中C原子个数=1,Mg原子个数=8×![]() =1,Ni原子个数=6×
=1,Ni原子个数=6×![]() =3,1mol晶胞的质量为12+24+59×3=213g,则ρg·cm-1=
=3,1mol晶胞的质量为12+24+59×3=213g,则ρg·cm-1=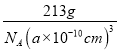 ,解得a=
,解得a=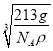 ×1010pm,故答案为:
×1010pm,故答案为: 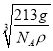 ×1010。
×1010。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列反应最终无沉淀产生的是
A. NaHCO3溶液中滴加Ba(OH)2溶液
B. Na2SiO3溶液中通入过量 CO2
C. 久置Na2SO3溶液滴加过量的盐酸酸化的BaC12溶液
D. NaAlO2溶液中滴加过量盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①干冰 ②Ba(OH)2 ③CCl4 ④NH4Cl固体 ⑤硫酸溶液 ⑥水 ⑦NH3 ⑧氯气 ⑨液态氯化氢⑩铝片
(1)上述为物质能导电的是_________________(填序号),属于电解质的是___________(填序号)。
(2)写出②与⑤反应的离子方程式____________________。
(3)写出①与过量②反应的离子方程式___________________。
(4)在标准状况下,含0.3molH的NH3的质量为__________g,体积为____________ L,与_____________molH2O所含电子数相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产生活中的许多现象或应用都与化学知识有关。下列现象或应用与胶体性质无关的是
A. 将盐卤或石膏加入豆浆中,制成豆腐
B. 冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷
C. 泡沫灭火器中将Al2(SO4)3与NaHCO3溶液混合后,喷出大量泡沫,起到灭火作用
D. 清晨,人们经常能看到阳光穿过茂密的树木枝叶所产生的美丽景象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题:
(1)某同学设计下图装置进行探究“铜和稀硝酸反应制取NO”的实验(夹持装置已略去),则制取NO的化学方程式为:____________;

利用该装置还可制取并收集少量其他气体,请完成下表:
制取气体 | 药品 |
O2 | __________ |
_______ | 某溶液_________________、Al |
(2)根据图1回答:
①打开K1,合上K2。则此时此装置为 ______;A电极可观察到的现象是____。
(3)根据图2回答:
将纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应式为_________________。
图2对应的实验完成后,铜电极增重6.4g,石墨电极产生标准状况下的气体体积_____L。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系正确的是
A. 沸点:戊烷>2,2-二甲基丙烷>2-甲基丁烷
B. 氢的质量分数:苯>乙烯> 甲烷
C. 密度:溴苯>H2O>苯
D. 等物质的量物质燃烧耗O2量:己烷>苯>C6H5COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、实验室中可以用高锰酸钾和浓盐酸反应制取氯气,化学反应如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)上述反应中的氧化剂是_________,还原剂与还原产物的物质的量之比为______。
(2)如果反应生成5mo1氯气,则过程中转移的电子数为________个。
II、按要求完成离子方程式。
(3)写出向明矾[KAl(SO4)2]溶液中加入氢氧化钡到Al3+完全沉淀的离子方程式:_________。
(4)完成以下氧化还原反应的离子方程式:__________________
( )MnO4 -+( )C2O42- +____ =( )Mn2++( )CO2↑+_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com