
【题目】下列各组物质的熔点均与所含化学键有关的是
A. CaO与CO2 B. NaCl与HCl C. CaCO3与SiO2 D. Cl2与I2
科目:高中化学 来源: 题型:
【题目】主族元素在元素周期表中的位置,取决于元素原子的( )
A.相对原子质量和核电荷数B.电子层数和中子数
C.电子层数和最外层电子数D.电子层数和核外电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在工农业生产中有重要的作用。
(1)已知:①C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol;
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-1651.0kJ/mol
CO还原Fe2O3的热化学方程式为__________________________________________。
(2)高炉炼铁产生的高炉气中含有CO、H2、CO2等气体,用CO和H2在催化剂作用下合成甲醇,是减少污染、节约能源的新举措,反应原理:CO(g)+2H2(g)![]() CH3OH(g) △H。在体积不同的两个恒容密闭容器中分别充入1molCO和2mol H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图。
CH3OH(g) △H。在体积不同的两个恒容密闭容器中分别充入1molCO和2mol H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图。
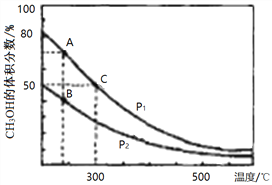
①在上图A、B、C三点中,选出对应下表物理量最小的点。
反应速率 | 平衡常数K | 平衡转化率α |
_________ | _________ | _________ |
②在300℃时,向C点平衡体系中再充入0. 5molCO、1.0molH2和0.5mol的CH3OH,该反应向_________方向进行(填“正反应”、‘逆反应”或“不移动”)。
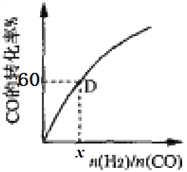
③一定温度下,CO的转化率与起始投料比[n(H2)/n(CO)]的变化关系图所示,测得D点氢气的转化率为40%,则x=_____________。
(3)三氯化铁是一种重要的化合物,可以用来腐蚀电路板。某腐蚀废液中含有0.5mol·L-1Fe3+和0.26mol·L-1的Cu2+,欲使Fe3+完全沉淀[c(Fe3+)≤4×l0-5]而Cu2+不沉淀,则需控制溶液pH的范围为_________。[KspCu(OH)2=2.6×l0-19;KspFe(OH)3=4×l0-38]
(4)莫尔盐,即六水合硫酸亚铁铵晶体,是一种重要的化工原料,在空气中缓慢风化及氧化,欲证明一瓶久置的莫尔盐已经部分氧化,需要进行实验操作是:取少量样品,加无氧水溶解,将溶液分成两份,______________________________________,则证明该样品已部分氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某蛋白质由三条肽链构成,其结构示意图如下,其中“—S—S—”为由两个“一SH”构成的二硫键,其作用是连接两相邻肽链。若该蛋白质分子共由A个氨基酸组成,则形成一个该蛋白质分子时减少的相对分子质量为:

A. 18(A-3)+4 B. 18(A-2)+4
C. 18m(A-3) D. 18(A-2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t ℃时,0.01 mol/L NaOH溶液pH=11,0.1 mol/LHA溶液中![]() =109。
=109。
(1)该温度下,水的离子积Kw=________,HA是________(填“强”或“弱”)酸。
(2)该温度下,将pH之和为13的NaOH溶液和HA溶液等体积混合后,所得溶液呈_____(填“酸”、“碱”或“中”)性,理由是____________________________________。
(3)在室温下,用蒸馏水稀释0.01 mol/L HA溶液时,下列呈减小趋势的是________。
A.![]() B.
B.![]() C.溶液中c(H+)和c(OH-)的乘积
C.溶液中c(H+)和c(OH-)的乘积
D.溶液中c(A-)·c(HA)的值 E.水的电离程度
(4)室温下,取pH=2的盐酸和HA溶液各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如下图所示:

①图中表示HA溶液pH变化曲线的是________(填“A”或“B”)。
②设盐酸中加入Zn的质量为m1,HA溶液中加入Zn的质量为m2,则m1________m2(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体A、B分别为0.6 mol和0.5 mol,在0.4 L密闭容器中发生反应:3A+B![]() aC+2D,经5 min后,此时C为0.2 mol,又知在此反应时间内,D的平均反应速率为0.1 mol·(L·min)-1,下列结论正确的是( )
aC+2D,经5 min后,此时C为0.2 mol,又知在此反应时间内,D的平均反应速率为0.1 mol·(L·min)-1,下列结论正确的是( )
A. 此时,反应混合物总的物质的量为1 mol B. B的转化率为50%
C. A的平均反应速率为0.1 mol·L-1·min-1 D. a值为2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,试管中盛有的水含几滴酚酞,气球a中盛有干燥的Na2O2颗粒,U形管中注有浅红色的水,将气球用橡皮筋紧缚在试管口。实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象预测错误的是 ( )

A. 气球a被吹大 B. 试管内溶液先变红后褪色
C. U形管内红色退去 D. U形管水位d>c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com