
【题目】某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞;
(B)用标准溶液润洗滴定管2-3次;
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液;
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm;
(E)调节液面至0或0刻度以下,记下读数;
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度。
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)______________________。
(2)实验中用左手控制_________(填仪器及部位),眼睛注视_______,直至滴定终点。判断到达终点的现象是___________。
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)_________________________。
(4)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对测定结果的影响是____________。
(5)滴定结束后如仰视观察滴定管中液面刻度,则对滴定结果的影响是______。
【答案】BDCEAF 碱式滴定管橡皮管玻璃珠处 锥形瓶中溶液的颜色变化 滴入最后一滴标准液,锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色 偏大 偏小 偏大
【解析】
(1)中和滴定按照检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等顺序操作,则正确的顺序为BDCEAF,故答案为:BDCEAF;
(2)滴定过程中,用左手控制碱式滴定管橡皮管玻璃珠处,右手摇动锥形瓶,两眼应该注视锥形瓶内溶液的颜色变化;滴定时,锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色,可说明达到滴定终点,故答案为:碱式滴定管橡皮管玻璃珠处;锥形瓶中溶液的颜色变化;滴入最后一滴标准液,锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色;
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,待测液的物质的量偏大,则消耗的标准液体积偏大,根据c(待测)=![]() 分析,可知c(待测)偏大,故答案为:偏大;
分析,可知c(待测)偏大,故答案为:偏大;
(4)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,等质量的NaOH或KOH固体中和酸时,NaOH消耗的盐酸多,所以会造成标准液的体积偏小,根据c(待测)= ![]() 分析,可知c(待测)偏小,故答案为:偏小;
分析,可知c(待测)偏小,故答案为:偏小;
(5)仰视观察滴定管中液面刻度,读数偏大,标准液的体积偏大,根据c(待测)=![]() 分析,可知c(待测)偏大,故答案为:偏大。
分析,可知c(待测)偏大,故答案为:偏大。


科目:高中化学 来源: 题型:
【题目】下列物质中,不能使酸性KMnO4溶液褪色的是
①![]() ②
②![]() ③
③![]() ④CH3CH2OH ⑤CH2=CH-COOH
④CH3CH2OH ⑤CH2=CH-COOH
A. ①③B. ①②③C. ③④⑤D. ②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月4日《光明日报》报道称,中科院大连化学物理研究所的研究团队利用多功能催化剂首次实现了CO2直接加氢制汽油的过程。其转化过程如图所示。
![]()
下列说法正确的是( )
A. 反应①的产物中含有水
B. 反应②为化合反应
C. 所制得汽油的主要成分是烃和烃的含氧衍生物
D. 这种人造汽油用作汽车的燃料时,汽车尾气不含氮氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:①H2(g)+1/2O2 (g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1 ,③C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ·mol-1,④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,回答下列问题:
(1)H2燃烧热的热化学方程式为___________ ;C燃烧热的热化学方程式为 ___________。(选数字)
(2)燃烧1gH2生成液态水,放出的热量为_________________。
(3)液态水的稳定性_______气态水的稳定性(填“大于”、“小于”、“等于”)。 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 化石燃料不一定在任何条件下都能充分燃烧
B. 化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体
C. 直接燃烧煤不如将煤进行深加工后再燃烧的效果好
D. 固体煤变为气体燃料后,燃烧效率将更低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性,下列说法正确的是
A. X、Y、Z、W的原子半径依次减小
B. W与X形成的化合物中只含离子键
C. W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D. 若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲中①②③④表示不同化学元素所组成的化合物,图乙表示由四个单体构成的化合物。以下说法不正确的是( )
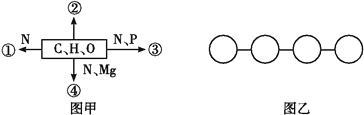
A. 若图甲中的②大量存在于皮下和内脏器官周围等部位,则②是脂肪
B. 若图甲中④能吸收、传递和转换光能,则④可用无水乙醇提取
C. 图乙中若单体是氨基酸,则该化合物彻底水解后的产物中氧原子数增加3个
D. 图乙中若单体是四种脱氧核苷酸,则该化合物彻底水解后的产物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料茉莉酮是一种人工合成的有机化合物,其结构简式为![]() ,下列关于茉莉酮的说法正确的是( )
,下列关于茉莉酮的说法正确的是( )
A. 该有机物的化学式是C10H14O
B. 1 mol该有机物与H2充分反应,消耗4 mol H2
C. 该有机物属于不饱和酮类物质,能发生银镜反应
D. 该有机物能发生加成反应,但不能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,其中正确的是
①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c (Na+) + c(H+)=c(OH-) + c(CH3COO-)
②对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
④常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;则有:Ka·Kh=Kw
⑤电解精炼铜时,电解质溶液中铜离子浓度不变 。
A.①④ B.①②④ C.①②④⑤ D.①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com