
【题目】短周期元素X、Y、Z、W原子序数依次增大。X氢化物的水溶性显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料,也是一种半导体材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中。请回答:
(1)Y在元素周期表中的位置是________。
(2)Y的最高氧化物相应水化物具有______(填“酸性”、“碱性”、“两性”)。并写出其电离方程式______。
(3)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈__性(填“酸”、“碱”或“中”),用离子方程式表示其原因是__。
(4)Z和W比较,非金属性较弱的是_______(填元素符号)。下列可以验证这一结论的是_______(填序号)。
a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.氢化物的水溶性
d.Z与W以共价键形成化合物时,Z或W显示的化合价
【答案】第三周期第IIIA族 两性 H++AlO2-+H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH- 酸 NH4++H2O
Al3++3OH- 酸 NH4++H2O![]() NH3H2O+H+ Si bd
NH3H2O+H+ Si bd
【解析】
短周期元素X、Y、Z、W原子序数依次增大,X氢化物的水溶液显碱性,则X是N元素;Y在元素周期表中所处的周期序数与族序数相等,且Y的原子序数大于X,所以Y是Al元素;Z单质是将太阳能转化为电能的常用材料,则Z是Si元素;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中,则W是Cl元素,结合元素周期律知识解答。
根据上述分析可知:X是N元素;Y是Al元素;Z是Si元素;W是Cl元素。
(1)Y是Al元素,核外电子排布是2、8、3,铝原子核外有3个电子层,最外层有3个电子,所以在元素周期表中位于第三周期第ⅢA族;
(2) Y是Al元素,其最高价氧化物相应的水化物是Al(OH)3,属于两性化合物,该物质既能与酸反应产生盐和水,也能与碱反应产生盐和水,这是由于Al(OH)3在水中存在两种方式的电离平衡,用电离方程式表示为:H++AlO2-+H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH-;
Al3++3OH-;
(3) X氢化物的水溶液氨水和盐酸恰好反应时生成氯化铵,氯化铵是强酸弱碱盐,在溶液中铵根离子发生水解NH4++H2O![]() NH3H2O+H+,破坏水的电离平衡,促进水的电离,当最终达到平衡时,溶液中c(H+)>c(OH-),使其水溶液呈酸性;
NH3H2O+H+,破坏水的电离平衡,促进水的电离,当最终达到平衡时,溶液中c(H+)>c(OH-),使其水溶液呈酸性;
(4)a.元素的非金属性强弱与其在地壳中的含量无关,a错误;
b.元素的非金属性越强,其最高价氧化物对应水化物的酸性就越强,因此可据此判断元素的非金属性强弱,b正确;
c.可根据氢化物的稳定性判断元素的非金属性,而不能根据氢化物水溶性判断,c错误;
d.元素的非金属性越强,其吸引电子的能力就越强,共用电子对就越偏小该元素,其化合价为负价,偏离的元素的化合价为正价,故可根据Z与W以共价键形成化合物时,Z或W显示的化合价判断元素的非金属性强弱,d正确;
合理选项是bd。


科目:高中化学 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:
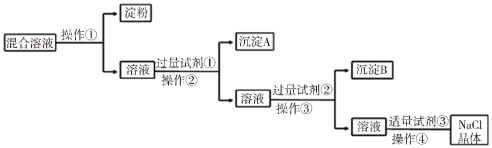
(1)操作①是利用半透膜进行分离提纯。
操作①的实验结果:淀粉___(填“能”或“不能”)透过半透膜;SO42-___(填“能”或“不能”)透过半透膜。
(2)写出实验过程中所用试剂(写化学式):
试剂①___;试剂③___。
(3)判断试剂①已过量的方法是:___。
(4)用离子方程式表示加入试剂②的作用:Ba2++CO32-=BaCO3↓、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 28g乙烯、丙烯的混合气体中所含原子数为6NA
B. 28g乙烯所含共用电子对数目为4NA
C. 标准状况下,11.2 L氯仿(CHCl3)所含分子数为0.5 NA
D. 78g苯中含有C—C键数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. ![]() 分子中的所有原子有可能共平面
分子中的所有原子有可能共平面
B. ![]() 中有8个碳原子可能在同一条直线上
中有8个碳原子可能在同一条直线上
C. 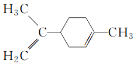 所有碳原子一定在同一平面上
所有碳原子一定在同一平面上
D. ![]() 至少有16个原子共平面
至少有16个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是 ________。
(2)根据上述反应,鉴别 NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________(填序号)。
(3)请配平以下化学方程式:
____Al+____NaNO3+____NaOH=____NaAlO2+____ N2↑+___H2O
(4)若反应过程中转移5 mol 电子,则生成标准状况下N2的体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)E元素形成的氧化物对应的水化物的化学式为_______________________________。
(2)元素C、D、E形成的简单离子半径大小关系是____________(用离子符号表示)。
(3)用电子式表示化合物D2C的形成过程:_________________。C、D还可形成化合物D2C2,D2C2中含有的化学键类型是_______________________________________________。
(4)由A、B、C三种元素形成的离子化合物的化学式为__________________,它与强碱溶液共热,发生反应的离子方程式是______________________。
(5)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为________________________(化学式用具体的元素符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为氢氧燃料电池装置示意图,下列有关说法正确的是( )
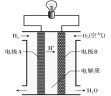
A. 电极A为正极
B. 产物为水,属于环境友好电池
C. 电子流向:电极B→导线→电极A
D. 该电池的化学能可以100%转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素单质可以参与很多化学反应, 如:NF3气体可由NH3和F2在Cu催化剂存在下反应直接得到;反应①:2NH3+3F2![]() NF3+ 3NH4F,Ta(钽)是一种过渡元素,利用“化学蒸气转移法”可以制备TaS2晶体;反应②:TaI4(g)+S2(g)
NF3+ 3NH4F,Ta(钽)是一种过渡元素,利用“化学蒸气转移法”可以制备TaS2晶体;反应②:TaI4(g)+S2(g)![]() TaS2(s)+2I2(g)+QkJ,Q>0
TaS2(s)+2I2(g)+QkJ,Q>0
(1)反应①中:非金属性最强的元素原子核外有____种不同运动状态的电子;该反应中的某元素的单质可作粮食保护气,则该元素最外层的电子有___种自旋方向。
(2)反应①中:物质所属的晶体类型有____;并写出所有原子符合8电子稳定结构的化合物的电子式____。
(3)反应②中:平衡常数表达式:K=___,若反应达到平衡后,保持其他条件不变,降低温度,重新达到平衡时____。
a.平衡常数K增大 b. S2的浓度减小 c. I2的质量减小 d. V(TaI4)逆 增大
(4)反应②在一定温度下进行,若反应容器的容积为2L,3min后达到平衡,测得蒸气的质量减少了2.45g,则I2的平均反应速率为___。
(5)某同学对反应②又进行研究,他查阅资料,发现硫单质有多种同素异形体,可表示Sx(x为偶数),且在一定条件下可以相互转化,他认为仅增大压强对平衡是有影响的,则TaI4的平衡转化率会____(填增大或减小),其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。某种综合处理含NH4+废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
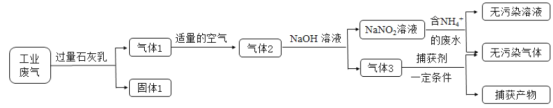
已知:NO+NO2+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)固体1的主要成分有Ca(OH)2、__________(填化学式)。
(2)若实验室需要配制3 mol·L-1NaOH溶液1L进行模拟测试,需称取NaOH固体质量为__________g。
(3)用NaNO2溶液处理含NH4+废水反应的离子方程式为__________。
(4)验证废水中NH4+已基本除净的方法是___________(写出操作、现象与结论)。
(5)气体1转化为气体2时空气不能过量的原因是__________。
(6)捕获剂捕获的气体主要是__________(填化学式)。
(7)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O;I2可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl。需选用的物质是__________(填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com