
【题目】下列说法正确的是
A.Fe3+的最外层电子排布式为![]()
B.基态原子的能量一定比激发态原子的能量高
C.基态碳原子价电子的轨道表示式:![]()
![]()
D.基态多电子原子中,P轨道电子能量一定比s轨道电子能量高
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】以NA代表阿伏加德罗常数,且已知C2H2(g)+ ![]() O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ/mol,则下列说法中正确的是( )
O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ/mol,则下列说法中正确的是( )
A.当有20NA个电子转移时,热化学方程式为2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-2600 kJ/mol
B.当有4NA个碳氧共用电子对生成时,放出1300 kJ的能量
C.若生成NA个水蒸气分子的焓变为ΔH',则ΔH'<ΔH
D.题给反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应可用于焊接钢轨,反应为:2Al + Fe2O3 ![]() 2Fe + Al2O3,下列关于该反应说法正确的是
2Fe + Al2O3,下列关于该反应说法正确的是
A. Al 是还原剂 B. Fe2O3 发生氧化反应
C. Fe 是氧化产物 D. 当生成 1 mol Fe 时,转移 6 mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应:M(g)+N(g)![]() P(g)+Q(g) ΔH>0,请回答下列问题:
P(g)+Q(g) ΔH>0,请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1 mol·L-1,c(N)=2.4 mol·L-1;5 min后反应达到平衡,M的转化率为60%,此时N的转化率为________;用M表示的反应速率为________;该温度下反应的平衡常数K=________。
(2)若反应温度升高,M的转化率________(填“增大”“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4 mol·L-1,c(N)=a mol·L-1;达到平衡后,c(P)=c(N)=2 mol·L-1,a=________。
(4)若反应温度不变,反应物的起始浓度为c(M)=c(N)=b mol·L-1,达到平衡后,M的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用下列化学反应在实验室中制备氯气,并进行有关氯气性质的研究。
![]()
(1)该小组同学欲用图所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
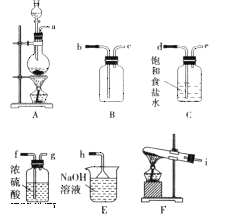
① 应该选择的仪器是__________(填字母)。
② 将各仪器按先后顺序连接起来,应该是a接__________,__________接__________,__________接__________,__________接h(用导管口处的字母表示)。
③ 浓盐酸与二氧化锰反应的离子方程式为__________。
(2)该小组同学设计分别利用图所示装置探究氯气的氧化性。
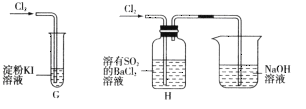
①G中的现象是__________,原因是__________(用化学方程式表示)。
②H中的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业烟气中去除氮氧化物的过程称为“脱硝”,某脱硝反应的平衡常数表达式为:K=![]() ,已知该反应的正反应为放热反应。
,已知该反应的正反应为放热反应。
(1)欲使该反应的K值增大,可采取的措施是___。
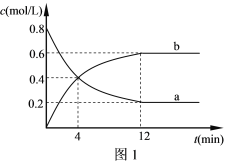
(2)400℃,在某恒容密闭容器中发生上述反应。测得部分物质浓度与时间的关系如图1所示。___分钟后,该反应的正逆反应速率相等;前4min内用O2表示的平均反应速率v(O2)=___。

(3)保持其他条件不变,探究![]() 的比值对NO转化率的影响,结果如图2所示,当
的比值对NO转化率的影响,结果如图2所示,当![]() <1时,NO转化率随着该比值的上升而上升,原因是___(用平衡移动原理解释);当
<1时,NO转化率随着该比值的上升而上升,原因是___(用平衡移动原理解释);当![]() >1后,由于氨气发生副反应导致烟气中NO浓度增大,使得转化率下降,这个副反应可以是___(用化学方程式表示)。
>1后,由于氨气发生副反应导致烟气中NO浓度增大,使得转化率下降,这个副反应可以是___(用化学方程式表示)。
(4)烟气脱硝的另一途径是电解NO:8NO+7H2O![]() 3NH4NO3+2HNO3。为得到纯净的NH4NO3,向上述所得溶液中通入适量NH3,浓度增大的离子有___;所得溶液稀释后可给庄稼施肥,稀释时
3NH4NO3+2HNO3。为得到纯净的NH4NO3,向上述所得溶液中通入适量NH3,浓度增大的离子有___;所得溶液稀释后可给庄稼施肥,稀释时![]() 将___(选填“增大”、“不变”或“减小”),理由是___。
将___(选填“增大”、“不变”或“减小”),理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所选装置或实验设计合理的是( )
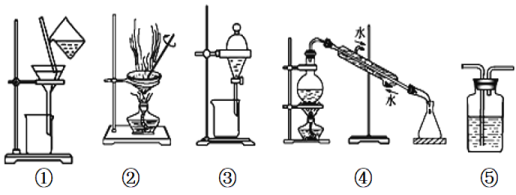
A.用图①和②所示装置可以除去NaCl中的CaCO3杂质,并获得NaCl固体
B.用乙醇提取溴水中的溴选择图③所示装置
C.用图④所示装置可以分离乙醇水溶液
D.图⑤所示装置中盛有饱和Na2CO3溶液除去CO2中含有的少量HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某样品中碳酸氢钠的质量分数(假设仅含杂质氯化钠),某学生设计了如下实验方案:

(1)称量所需要的仪器是_______________;
(2)样品放在_________(仪器名)中灼烧,在_________(仪器名)中冷却;
(3)实验中操作A的名称为_______________;
(4)灼烧后的样品若在空气中冷却,会造成实验结果_______(填“偏大”、“偏小”或“不变”);
(5)样品中碳酸氢钠的质量分数为_________(保留3位有效数字)。已知该样品碳酸氢钠的质量分数为0.800,则本次实验的相对误差为___________;
(6)将灼烧后的样品加足量稀硫酸溶解,生成的气体在标准状况下的体积为_____毫升(按碳酸氢钠质量分数0.800计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列行为不符合安全要求的是![]()
![]()
A.做实验剩余的金属钠放回原试剂瓶中
B.闻气体时用手轻轻扇动,使少量气体飘进鼻孔
C.金属钠着火时使用泡沫灭火器灭火
D.装氢氧化钠溶液的试剂瓶用橡胶塞
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com