
| A、0.1 mol?L-1NH3?H2O溶液中:c (NH4+)<c (OH-) |
| B、常温时,将等体积的盐酸和氨水混合后pH=7,则c(NH4+)=c(Cl-) |
| C、0.1 mol?L-1Na2CO3溶液中:c(HCO3-)+c(CO3-)+c(H2CO3)=0.1 mol?L-1 |
| D、浓度均为0.1 mol?L-1的NH4Cl、CH3COONH4、NH4HSO4溶液,c(NH4+)大小顺序:CH3COONH4>NH4Cl>NH4HSO4 |


科目:高中化学 来源: 题型:
| A、乙醇的结构简式为:C2H6O |
B、硫离子的结构示意图为: |
| C、NaHCO3电离:NaHCO3=Na++H++CO32- |
D、氮分子的结构式为: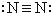 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀硫酸滴在铁片上:2Fe+6H+═2Fe3++3H2↑ |
| B、向AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
| C、硫酸铁溶液与铁粉混合:2Fe3++Fe=3Fe2+ |
| D、碳酸氢钠溶液与氢氧化钠混合:H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硝酸具有强氧化性,可用铁罐贮运浓硝酸 |
| B、明矾常作为净水剂,双氧水通常可用于作杀菌消毒 |
| C、合成氨工业中通过升高温度可以增大平衡常数K,来提高氨的产率 |
| D、催化剂可以改变反应速率,对平衡移动没有影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MFe2Ox是还原产物 |
| B、MFe2Ox 中+2价铁与+3价铁的物质的量之比为1:3 |
| C、x=3.5 |
| D、若反应中消耗H2(标准状况下)33.6 L,则转移电子3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、950mL,201.4g |
| B、1000mL,212g |
| C、任意规格,572g |
| D、500mL,106g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com