
【题目】“碘钟”实验中,3I-+![]() =
=![]() +
+![]() 的反应速率可以用
的反应速率可以用![]() 遇加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20 ℃进行实验,得到的数据如下表:
遇加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20 ℃进行实验,得到的数据如下表:
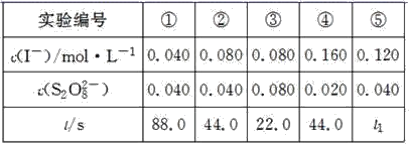
回答下列问题:
(1)该实验的目的是_______________。
(2)显色时间t1为________。
(3)通过分析比较上述数据,得到的结论是__________。
【答案】研究反应物I-与![]() )的浓度对反应速率的影响 29.3 化学反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比)
)的浓度对反应速率的影响 29.3 化学反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比)
【解析】
(1)根据图表已知物理量判断;
(2)根据浓度与时间的关系计算;
(3)根据图表中物理量的关系得出结论。
(1)图表中的物理量是反应物浓度与时间,通过分析知,反应物的浓度与时间成反比,浓度的变化量与时间的比值为速率,所以得出反应物浓度与反应速率的关系,故答案为:研究反应物I-与![]() 的浓度对反应速率的影响;
的浓度对反应速率的影响;
(2)由数据表容易发现:②④组所用时间相同,③组所用时间为它们的一半,①组所用时间为它们的2倍。进一步②④两组中c(I-)与c(![]() )的乘积相等,③组中此乘积为②④组的2倍,①组乘积为其一半。因此可得结论:当c(I-)·c(
)的乘积相等,③组中此乘积为②④组的2倍,①组乘积为其一半。因此可得结论:当c(I-)·c(![]() )相等时,显色时间相等,反应速率相等,显色时间与反应速率成反比,即t与c(I-)·c(
)相等时,显色时间相等,反应速率相等,显色时间与反应速率成反比,即t与c(I-)·c(![]() )成反比,
)成反比,![]() =
=![]() 得t1=
得t1=![]() ≈29.3s, 故答案为:29.3s;
≈29.3s, 故答案为:29.3s;
(3)通过分析知,反应物的浓度乘积与时间成反比,浓度的变化量与时间的比值为速率,故答案为:反应速率与反应物起始浓度乘积成正比或显色时间与反应物起始浓度乘积成反比。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 苯酚钠溶液中通入少量的二氧化碳,产物是苯酚和碳酸钠
B. 苯的同系物中,苯环和侧链相互影响,使得二者均易被氧化
C. ![]() 在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2
在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2
D. 苯甲醛、苯乙烯分子中的所有原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)![]() 4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
A. A的平均反应速率是0.010 molL﹣1s﹣1
B. 容器中含D物质的量至少为0.45 mol
C. 容器中A、B、C、D的物质的量的比一定是4∶5∶4∶6
D. 容器中A的物质的量一定增加了0.30 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:

A. 温度T下,该反应的平衡常数K=![]()
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两个体积相同的密闭容器A、B,在A中充入SO2和O2各1mol,在B中充入SO2和O2各2mol,加热到相同温度,有如下反应2SO2(g)+O2(g)![]() 2SO3(g),对此反应,下述不正确的是
2SO3(g),对此反应,下述不正确的是
A. 反应速率B>A B. SO2的转化率B>A
C. 平衡时各组分含量B=A D. 平衡时容器的压强B>A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+,进行以下实验,记录实验结果,并思考改变物质浓度对平衡移动的影响。
2CrO42-(黄色)+2H+,进行以下实验,记录实验结果,并思考改变物质浓度对平衡移动的影响。
实验1:向试管中加入4mL 0.1mol·L-1 K2Cr2O7溶液,再加数滴1mol·L-1 NaOH溶液,观察溶液颜色变化;
实验2:将上述溶液分成两份向其中一份中滴加1mol·L-1 HNO3,观察溶液颜色变化,并和另一份做对比_____。
实验现象 | 实验结论 | |
实验1 | ||
实验2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将H2(g)和I2(g)各1 mol的气态混合物充入2 L的密闭容器中,充分反应,5 min后达到平衡,测得c(HI)=0.2 mol/L。
(1)计算从反应开始至达到平衡,用H2(g)表示的反应速率。
(2)求该反应的平衡常数。
(3)保持温度不变,若向上述容器中充入H2(g)和I2(g)各2 mol,求达到平衡时I2(g)的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如图,下列说法不正确的是( )

A.在阴极室,发生的电极反应为:2H2O+2e-=2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+![]() Cr2O72-+H2O向右移动
Cr2O72-+H2O向右移动
C.该制备过程总反应的化学方程式为:4K2CrO4+4H2O![]() 2K2Cr2O7+4KOH+2H2↑+O2↑
2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为1-0.5d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂产生的烧渣(主要含![]() 、
、![]() 及少量
及少量![]() )可用于制备
)可用于制备![]() 和还原铁粉,其流程如图:
和还原铁粉,其流程如图:

(1)“酸溶”前需粉碎烧渣,其目的是_________、________。
(2)“滤渣”的主要成分是_________(填化学式)。
(3)“还原”时,![]() 被氧化为
被氧化为![]() 的离子方程式是_________。
的离子方程式是_________。
(4)“焙烧”时,烧渣、无烟煤、![]() 的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):

添加![]() 的目的是:①脱除
的目的是:①脱除![]() 等;②_________。
等;②_________。
(5)“焙烧”在半封闭装置中进行,投料层表面盖有适当厚度的煤层,“焙烧”时间控制在4~4.5小时(焙烧时间对还原铁粉产率的影响如图所示),超过5小时后还原铁粉产率降低的原因是_______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com