


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����¶Ȳ���ʱ��ˮ��Һ��c��H+����c��OH-������ͬʱ���� |
| B��pH=0����Һ��������ǿ����Һ |
| C��ǿ���ˮ��Һ�в�����OH- |
| D��ij�¶��£���ˮ��c��H+��=2��10-7mol?L-1��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2CO3 | B��Na2SO4 | C��NH4Cl | D��KAl (SO4) 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��һ���������� | B��ˮ�ĵ���ƽ�ⲻ��Ӱ�� |
| C��ˮ�������Ҫ�������� | D����Һ��pHһ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ѡ�� | �������ʵ | ���� |
| A | ���ȵ��ռ���Һϴȥ���� | Na2CO3��ֱ�Ӻ����۷�Ӧ |
| B | Ư���ڿ����о��ñ��� | Ư���е�CaCl2 ������е�CO2��Ӧ����CaCO3 |
| C | ʩ��ʱ����ľ��(��Ч�ɷ�ΪK2CO3)������NH4Cl���ʹ�� | K2CO3��NH4Cl��Ӧ���ɰ����ή�ͷ�Ч |
| D | FeCl3��Һ������ͭ��ӡˢ��·������ | FeCl3�ܴӺ���Cu2������Һ���û���ͭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
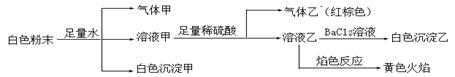
| A����ɫ��������Al(OH)3���������CO2�����Ի����һ����Al3����HCO3�� |
| B��������һ����NO��NO2�Ļ������ |
| C����ɫ��������BaSO4������ԭ�����һ������SO42�� |
| D����ɫ��ĩ��һ������Na�� ��Al3�� ��NO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c (Na+)=c(CH3COO��)+c(CH3COOH) |
| B��c(H+)=c(CH3COO��)+c(OHһ) |
| C��c (Na+) > c (CH3COO��)>c(OH��)>c(H+) |
| D��c (CH3COO��)>c(Na+)>c(H+)>c(OH��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��25��ʱ����0.1mol��L��1NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�c(Na��)��c(NH4+)��c(SO42��)��c(OH��)��c(H��) |
| B��25��ʱ��NaB��Һ��pH��8��c(Na��) + c(B��)��9.9��10��7mol��L��1 |
| C��0.1mol��L��1��NaHCO3��Һ�У�c(OH��)��c(CO32��)��c(H+)��c(H2CO3) |
| D��ͬ���£�pH��ͬʱ����Һ���ʵ���Ũ�ȣ�c(CH3COONa)<c(NaHCO3)<c(C6H5ONa)<c(Na2CO3) |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com