
| A、形成原电池后,原电池中的阳离子向正极移动 |
| B、原电池中电子流出的一极是正极,发生氧化反应 |
| C、原电池的两极发生的反应均为氧化还原反应 |
| D、原电池是把电能转化为化学能的装置 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
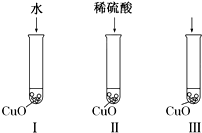 氧化铜是一种黑色固体,可溶于稀硫酸.某化学兴趣小组为探究稀硫酸中哪种粒子能使氧化铜溶解,该小组同学提出如下假设:
氧化铜是一种黑色固体,可溶于稀硫酸.某化学兴趣小组为探究稀硫酸中哪种粒子能使氧化铜溶解,该小组同学提出如下假设:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、b=2 |
| B、容器中一定没有残余的CO2和水蒸气 |
| C、a≥b |
| D、反应中转移的电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热时苏打较稳定,小苏打不稳定,易分解 |
| B、相同温度下,小苏打较苏打易溶于水 |
| C、苏打是发酵粉的主要成分之一,也用于治疗胃病 |
| D、小苏打常用作洗涤剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 空气 |
| △ |
| HNO3(稀) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 强电解质 | NaCl | H2SO4 | CaCO3 | HNO3 |
| 弱电解质 | HF | 氨水 | HClO | HI |
| 非电解质 | Cl2 | 蔗糖 | C2H5OH | SO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com