
【题目】一定温度下,在容积为2L的密闭容器中发生反应CO(g)+H2O(g)CO2(g)+H2(g),部分数据见表(表中t2>t1),说法错误的是( )
反应时间/min | n(CO)/mol | n(H2O)/mol | n(CO2)/mol | n(H2)/mol |
0 | 1.20 | 0.60 | 0 | 0 |
t1 | 0.80 | |||
t2 | 0.20 |
A.反应在t1min末的速率为v(H2)=0.2/t molL﹣1min﹣1
B.平衡时水蒸气的转化率为66.67%
C.该温度下反应的平衡常数为1
D.其他条件不变,若起始时,n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时水蒸气的转化率为33.33%
【答案】A
【解析】解:A.反应速率只能表示平均速率不能表示瞬时速率,反血在t1min内的平均速率为v(H2)= ![]() molL﹣1min﹣1 , 故A错误; B.由表中的数据可知t2时刻一定达到平衡状态,则水蒸气的平衡转化率为
molL﹣1min﹣1 , 故A错误; B.由表中的数据可知t2时刻一定达到平衡状态,则水蒸气的平衡转化率为 ![]() ×100%=66.67%,故B正确;
×100%=66.67%,故B正确;
C.根据方程式可知K= ![]() =
= ![]() =1,故C正确;
=1,故C正确;
D.温度不变,平衡常数不变,设水蒸气的转化率为x,则
CO(g)+ | H2O(g) | CO2(g)+ | H2(g) | ||
开始 | 0.6 | 1.2 | 0 | 0 | |
转化 | 1.2x | 1.2x | 1.2x | 1.2x | |
平衡 | 0.6﹣1.2x | 1.2﹣1.2x | 1.2x | 1.2x |
![]() =1,解得x=33.33%,故D正确;
=1,解得x=33.33%,故D正确;
故选A.
【考点精析】解答此题的关键在于理解化学平衡的计算的相关知识,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


科目:高中化学 来源: 题型:
【题目】室温下,单质A、B、C分别为固体、黄绿色气体与无色气体,在合适条件下,它们可以按下面的流程进行反应.又知E溶液是无色的.请回答: 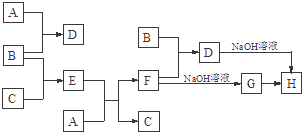
(1)写出E物质的化学式 .
(2)写出G→H的化学方程式 .
(3)写出B+F→D的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学查阅教材得知,普通锌锰电池筒内无机物质主要成分为MnO2、NH4Cl、ZnCl2等物质。他在探究废干电池内的黑色固体回收利用时,进行如图所示实验:下列有关实验的叙述中,不正确的是

A. 操作①中玻璃棒的作用是加快固体溶解速度
B. 操作②的操作名称是过滤
C. 操作③中盛放药品的仪器是坩埚
D. 操作④的目的是除去滤渣中杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解产物,某学生设计了如下实验方案: 
回答下列问题:
(1)试剂1是 , 作用是;
(2)试剂2是 , 作用是 , 发生的离子反应为:; 如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的 , 若不能,其原因是 .
(3)如何检验第①步实验已基本完成 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应X+2Y=X2++2Y-的叙述中正确的是
A. X被氧化,Y是氧化剂 B. Y被还原,X是氧化剂,
C. X是还原剂,Y被氧化 D. Y被还原,X2+是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在③~⑦元素中,原子半径最大的是 , 其离子的原子结构示意图为
(2)写出⑤和⑨最高价氧化物对应水化物间发生反应的离子方程式: .
(3)按要求写出下列两种物质的电子式:①的单质;⑨的过氧化物;
(4)在⑦与⑩的单质中,化学性质较活泼的是 , 可用什么化学反应说明该事实(写出反应的化学方程式): .
(5)请用电子式表示④和⑩组成的化合物的形成过程 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当光束通过下列物质时,不会出现丁达尔效应的是
①稀豆浆 ②蒸馏水 ③硫酸铜稀溶液 ④FeCl3稀溶液 ⑤云雾
A.②④⑤B.①③④C.②③④D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D,E,F六种化合物,其中A,B,C,D,E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为_______
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)下表为B与F实验的部分内容
①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色,且用激光笔照射有丁达尔效应。 |
写出B与稀H2SO4反应的离子方程式________
写出②中反应的化学方程式________
(3)现由6种粒子Mn2+、MnO 4-、H+、H2O、X2Y 82-(C中含有的阴离子)、XY 42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO 4- 需氧化剂的物质的量为________ mol
(4)化合物D和E相互转化D ![]() E,若有D和ExH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为________ g,ExH2O的化学式为________.
E,若有D和ExH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为________ g,ExH2O的化学式为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com