
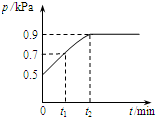
 在1.0L密闭容器中放入0.1mol X,在一定温度下发生反应:X(g)?Y(g)+Z(g)△H<0 容器内气体总压强p随反应时间t的变化关系如图所示.以下分析正确的是( )
在1.0L密闭容器中放入0.1mol X,在一定温度下发生反应:X(g)?Y(g)+Z(g)△H<0 容器内气体总压强p随反应时间t的变化关系如图所示.以下分析正确的是( )| A. | t1时n(X)=0.04 mol | |
| B. | t1到t2,混合气体的平均相对分子量增大 | |
| C. | 欲提高平衡体系中Y的含量,可升高体系温度或减少Z的量 | |
| D. | 其他条件不变,再充入0.1 mol 气体X,平衡正向移动,X的转化率减少 |
分析 A.利用压强之比等于物质的量之比计算t1时混合气体总物质的量,由方程式可知混合气体物质的量减少量等于参加反应X的物质的量;
B.t1到t2反应继续向正反应进行,混合气体总物质的量增大,而混合气体总质量不变;
C.升高温度平衡逆向移动,Y的含量降低;
D.其他条件不变,再充入0.1 mol 气体X,等效为在原平衡的基础上压强增大一倍,与原平衡相比逆向移动.
解答 解:A.由于恒温恒容下,压强之比等于物质的量之比,则t1时混合气体总物质的量为0.1mol×$\frac{0.7}{0.5}$=0.12mol,由方程式可知混合气体物质的量减少量等于参加反应X的物质的量,故转化的X为(0.12mol-0.1mol)=0.02mol,t1时n(X)=0.1mol-0.02mol=0.08 mol,故A错误;
B.t1到t2反应继续向正反应进行,混合气体总物质的量增大,而混合气体总质量不变,由M=$\frac{m}{n}$可知,t1到t2混合气体的平均相对分子量减小,故B错误;
C.减少Z的量,平衡正向移动,可以增大Y的含量,但正反应为放热反应,升高温度平衡逆向移动,Y的含量降低,故C错误
D.其他条件不变,再充入0.1 mol 气体X,平衡正向移动,所到达的平衡等效为在原平衡的基础上压强增大一倍,与原平衡相比逆向移动,X的转化率减小,故D正确,
故选:D.
点评 本题考查化学平衡计算与影响因素,侧重考查学生分析计算能力,D选项注意利用等效思想解答,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
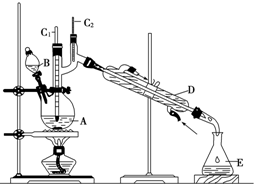 正丁醛是一种化工原料.某实验小组利用如右装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如右装置合成正丁醛.| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.810 9 | 微溶 |
| 正丁醛 | 75.7 | 0.801 7 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 高效利用CO2是“低碳经济”的有效途径,现有以下两种利用CO2的方法.
高效利用CO2是“低碳经济”的有效途径,现有以下两种利用CO2的方法.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(N2) | 0 | 0.20 | 0.35 | 0.40 | 0.40 |
| T2 | n(N2) | 0 | 0.25 | … | 0.30 | 0.30 |
| A. | T1温度下,CH4的平衡转化率为50% | |
| B. | T1<T2 | |
| C. | a<0 | |
| D. | T2时反应的平衡常数大于T1时反应的平衡常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com