
����Ŀ����1��������Ͽ�ѧ�ҷ������������ᾧˮ�ľ�����5K�³��ֳ����ԡ��þ���Ļ�ѧʽΪNa0.35CoO2��1.3H2O(�þ����Ħ������Ϊ122g��mol-1)������NA��ʾ�����ӵ���������12.2g�þ����к���ԭ����Ϊ___����ԭ�ӵ����ʵ���Ϊ___mol��
��2��FeCl3��Һ����������ˮ����100mL2mol��L-1��FeCl3��Һ��ˮʱ�����ɾ��о�ˮ���õ�����___(����ڡ������ڡ���С�ڡ�)0.2NA��
��3���ڱ�״���£�VLij����(Ħ������ΪMg/mol)�ܽ���1Lˮ(ˮ���ܶȽ���Ϊ1g/cm3)�У�����������ȫ�ܽ��Ҳ���ˮ������Ӧ��������Һ���ܶ�Ϊ��g/cm3����������Һ�����ʵ���Ũ��c=___mol/L(��������ĸ��ʾ���ұ��뻯��)��
��4����ҵ�����������ƺ�ϡ����Ϊԭ���Ʊ�ClO2��Ӧ��NaClO2��HCl��ClO2����NaCl+H2O��д����ƽ�Ļ�ѧ����ʽ____��
��5����100mL��FeBr2��Һ��ͨ���״����Cl23.36L(��֪��ԭ�ԣ�Fe2����Br��)����Ӧ�����Һ��Cl����Br�������ʵ���Ũ����ȣ���ԭFeBr2��Һ�����ʵ���Ũ��Ϊ____mol/L����Ӧ�����ӷ���ʽΪ____��
��6������ʢ��10mL1mol��L��1NH4Al(SO4)2��Һ���ձ��м�20mL1.2mol��L��1Ba(OH)2��Һ����ַ�Ӧ����Һ�в������������ʵ���Ϊ____mol��
���𰸡�0.33NA 0.26 С�� ![]() 5NaClO2��4HCl=4ClO2����5NaCl+2H2O 2 4Fe2����2Br-��3Cl2=4Fe3����Br2��3Cl- 0.022
5NaClO2��4HCl=4ClO2����5NaCl+2H2O 2 4Fe2����2Br-��3Cl2=4Fe3����Br2��3Cl- 0.022
��������
��1������![]() ���㾧������ʵ���������������ԭ�ӡ���ԭ�ӵ����ʵ�����
���㾧������ʵ���������������ԭ�ӡ���ԭ�ӵ����ʵ�����
��2��100mL2mol��L-1��FeCl3��Һ��FeCl3�����ʵ�����0.1L��2mol��L-1=0.2mol��
��3���������ʵ���Ũ�ȵļ��㹫ʽ![]() ���㣻
���㣻
��4�����ݵ�ʧ�����غ㡢Ԫ���غ���ƽ����ʽ��
��5����ԭ�ԣ�Fe2����Br����FeBr2��Һ��ͨ���״����Cl2������������Fe2����
��6��NH4Al(SO4)2��Ba(OH)2��Һ��ϣ�SO42-��Ba2+��Ӧ����BaSO4������OH-��Al3+��NH4+���η�����ӦAl3++3OH-=Al(OH)3����NH4++OH-=NH3H2O��Al(OH)3+OH-=AlO2-+2H2O��
��1������![]() ��12.2g�þ�������ʵ�����
��12.2g�þ�������ʵ�����![]() 0.1mol������ԭ����Ϊ0.1��3.3��NA=0.33NA����ԭ�ӵ����ʵ���Ϊ0.1mol��2.6=0.26mol��
0.1mol������ԭ����Ϊ0.1��3.3��NA=0.33NA����ԭ�ӵ����ʵ���Ϊ0.1mol��2.6=0.26mol��
��2��100mL2mol��L-1��FeCl3��Һ��FeCl3�����ʵ�����0.1L��2mol��L-1=0.2mol�����ɾ��о�ˮ���õ������������������������������������������ľۼ��壬��������С��0.2NA��
��3���ڱ�״���£�VLij��������ʵ�����![]() ��VLij�����������
��VLij�����������![]() ��������Һ��������
��������Һ��������![]() ����Һ�������
����Һ������� ���������ʵ���Ũ��Ϊ
���������ʵ���Ũ��Ϊ![]() ��
��![]() =
=![]() mol/L��
mol/L��
��4��NaClO2�в�����Ԫ�ػ��ϼ���+3����Ϊ+4��������Ԫ�ػ��ϼ���+3����Ϊ-1������NaClO2�������������ǻ�ԭ�������ݵ�ʧ�����غ㣬��������ԭ���ı�Ϊ1:4�����Է�Ӧ����ʽ��5NaClO2��4HCl=4ClO2����5NaCl+2H2O��
��5����ԭ�ԣ�Fe2����Br����FeBr2��Һ��ͨ��Cl2������������Fe2������״����3.36L Cl2�����ʵ�����![]() 0.15mol����FeBr2�����ʵ���Ϊxmol��������Fe2����Ӧ�����ӷ���ʽ��2Fe2��+Cl2=2Fe3��+2Cl-����Fe2���������������ʵ�����
0.15mol����FeBr2�����ʵ���Ϊxmol��������Fe2����Ӧ�����ӷ���ʽ��2Fe2��+Cl2=2Fe3��+2Cl-����Fe2���������������ʵ�����![]() mol����Br-��Ӧ���������ʵ�����0.15mol-
mol����Br-��Ӧ���������ʵ�����0.15mol-![]() mol��������Br-��Ӧ�����ӷ���ʽ��2Br-+Cl2=Br2+2Cl-��ʣ��Br-�����ʵ�����2x-0.3+x=(3x-0.3)mol��������Ԫ���غ㣬��Ӧ����Һ��Cl-�����ʵ�����0.3mol����Ӧ�����Һ��Cl����Br�������ʵ���Ũ����ȣ���3x-0.3=0.3��x=0.2mol��ԭFeBr2��Һ�����ʵ���Ũ��Ϊ0.2mol��0.1L=2mol/L����Br-��Ӧ���������ʵ�����0.15mol-
mol��������Br-��Ӧ�����ӷ���ʽ��2Br-+Cl2=Br2+2Cl-��ʣ��Br-�����ʵ�����2x-0.3+x=(3x-0.3)mol��������Ԫ���غ㣬��Ӧ����Һ��Cl-�����ʵ�����0.3mol����Ӧ�����Һ��Cl����Br�������ʵ���Ũ����ȣ���3x-0.3=0.3��x=0.2mol��ԭFeBr2��Һ�����ʵ���Ũ��Ϊ0.2mol��0.1L=2mol/L����Br-��Ӧ���������ʵ�����0.15mol-![]() mol=0.05mol����������Br-�����ʵ�����0.1mol����������Fe2����Br-�����ʵ�������2:1�����Է�Ӧ����ʽ��4Fe2����2Br-��3Cl2=4Fe3����Br2��3Cl-��
mol=0.05mol����������Br-�����ʵ�����0.1mol����������Fe2����Br-�����ʵ�������2:1�����Է�Ӧ����ʽ��4Fe2����2Br-��3Cl2=4Fe3����Br2��3Cl-��
��6��10mL 1molL-1NH4Al(SO4)2��Һ��Al3+���ʵ���Ϊ0.01mol��NH4+�����ʵ���Ϊ0.01mol��SO42-�����ʵ���Ϊ0.02mol��20mL 1.2 molL-1Ba(OH)2��Һ��Ba2+���ʵ���Ϊ0.024mol��OH-Ϊ0.048mol����SO42-+Ba2+=BaSO4������֪SO42-���㣬���Կ��Եõ�0.02mol BaSO4������Al3++3OH-=Al(OH)3����֪��Ӧʣ��OH-Ϊ0.048mol-0.03mol=0.018mol������H4++OH-=NH3H2O��֪��Ӧʣ��OH-Ϊ0.018mol-0.01mol=0.008mol������Al(OH)3+OH-=AlO2-+2H2O��֪�õ�Al(OH)3����Ϊ0.01mol-0.008mol=0.002mol�������յõ�����Ϊ0.02mol+0.002mol=0.022mol��


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵������ȷ����
A.4.0g��ˮ(D2O)������������Ϊ0.4NA
B.4.48L N2��CO�Ļ����������������Ϊ0.2NA
C.�����£�7.1g Cl2������NaOH��Һ��Ӧת�Ƶĵ�����ԼΪ0.1NA
D.0.2mol Na2O2�к�����������Ϊ0.8NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A. HCl��NaOH��Ӧ���к��ȡ�H����57.3kJ/mol����H2SO4��Ca(OH)2��Ӧ���к��� ��H��2��(��57.3)kJ/mol
B. CO(g)��ȼ������283.0kJ/mol����2CO2(g)��2CO(g)��O2(g)�ķ�Ӧ�ȡ�H����566.0kJ/mol
C. ��Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
D. ȼ������ָ1mol������ȫȼ��ʱ�ų�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
��CO(g)��1/2O2(g)===CO2(g)����H����283.0 kJ��mol��1
��H2(g)��1/2O2(g)===H2O(g)����H����241.8 kJ��mol��1
����˵����ȷ����(����)
A. ͨ��״���£�������ȼ����Ϊ241.8 kJ��mol��1
B. �ɢٿ�֪��1 mol CO(g)��1/2 mol O2(g)��Ӧ���� 1 mol CO2(g)���ų�283.0 kJ������
C. ������ͼ��ʾ2CO2(g)===2CO(g)��O2(g)��Ӧ�����е������仯��ϵ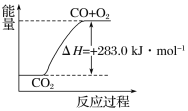
D. �ֽ�1 mol H2O(g)���䷴Ӧ��Ϊ��241.8 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��еĸ�������֮��ͨ��һ����Ӧ����ʵ����ͼ��ʾת�����ǣ� ��
��� | a | b | c | d |
|
�� | Na2O | Na2O2 | Na | NaOH | |
�� | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
�� | FeCl2 | FeCl3 | Fe | CuCl2 | |
�� | MgO | MgCl2 | Mg | Mg(OH)2 |
A.�٢ڢ�B.�٢ۢ�C.�٢ڢ�D.�ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ�����ǰѲ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܡ����ܵĴ�С�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H)����ѧ��Ӧ����H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ

�������Ȼ�ѧ����ʽ����ȷ����(����)
A. 1/2A2(g)��1/2B2(g)��AB(g) ��H����91.5kJ��mol��1
B. A2(g)��B2(g)��2AB(g)����H����183kJ��mol��1
C. 2AB(g)��A2(g)��B2(g) ��H����183kJ��mol��1
D. 1/2A2(g)��1/2B2��AB(g) ��H����91.5kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��CΪ��ѧ�������ʣ�����һ��Ϊ������ͨ�������AΪ���塢BΪ����ɫ���塢CΪ��ɫ���塣D��E��F��G��H��X��Ϊ���������X����������ɫ���壬��ˮ��Һ��һ������ǿ����Һ��EΪ��ɫ���壬H�ڳ�����ΪҺ�塣����֮���ת����ͼ��ʾ��ijЩ��Ӧ�����Ͳ��ַ�Ӧ��������ȥ����
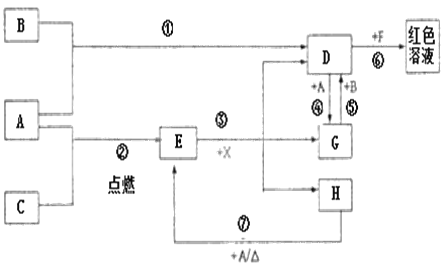
��1��д���������ʵĻ�ѧʽ��D___��X___��
��2���ڷ�Ӧ�١����У�������������ԭ��Ӧ����___�������ֱ�ţ���
��3����Ӧ�����ӷ���ʽΪ��___��
��4����Ӧ�ߵĻ�ѧ����ʽΪ___���÷�Ӧ��ÿ����0.3mol��A����ת�Ƶ���___mol��
��5����ȥD��Һ�л��е�����G�ķ����ǣ�___��
��6������G��Һ�������ӵķ����ǣ�___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����Ҫ��д������ʽ��
��HNO3(���뷽��ʽ) _____________��
��Fe2(SO4)3(���뷽��ʽ) ___________��
�������ƺ��Ȼ�����Һ��Ӧ(���ӷ���ʽ) ______________��
�ܶ�����̼ͨ����������������Һ(���ӷ���ʽ)_________________��
��2������Ϊ��ѧ��ѧ�г����ļ������ʣ��ٶ�����̼��������KCl����NaHSO4���塡��ͭ����ϡ���ᡡ����ʯ��ˮ���������ڵ���ʵ���_________�����ڷǵ���ʵ���________(�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Թ�ѧ��������Ϣ�����⼼����ҽ�ơ����������������ҪӦ�ü�ֵ���ҹ���ѧ������Ca2CO3�� XO2��X= Si��Ge����H3BO3�״κϳ������ΪCsXB3O7�ķ����Թ�ѧ���塣�ش��������⣺
(1)��̬��ԭ�ӵļ۵����Ų�ͼ��____________��������ͬ���ڵķǽ�������Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ________________��
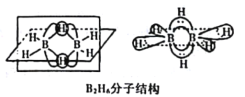
(2)B�ļ��⻯��BH3������������ڣ����������γɽ��ȶ���B2H6�����������ӽ�ϡ�
��B2H6���ӽṹ��ͼ����Bԭ�ӵ��ӻ���ʽΪ____________________��
�ڰ����飨NH3BH3������Ϊ�����DZ�������ʹ������֮һ�������д�����λ�����ṩ�µ��ӶԵijɼ�ԭ����______________��д��һ���백���黥Ϊ�ȵ�����ķ���_________�������ʽ����
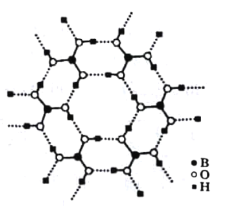
(3)��ͼΪH3BO3�����Ƭ��ṹ������B���ӻ���ʽΪ_______����������ˮ�б�����ˮ���ܽ�������������Ҫԭ����____________��
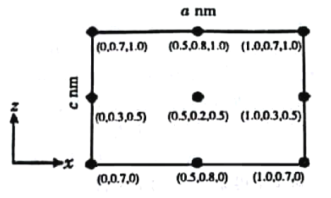
(4)�Ծ�������Ϊ��λ���Ƚ���������ϵ���Ա�ʾ�����и�ԭ�ӵ�λ�ã���Ϊԭ�ӷ������ꡣCsSiB3O7����������ϵ���������Σ�����������Ϊanm��bnm��cnm����ͼΪ��y��ͶӰ�ľ���������Csԭ�ӵķֲ�ͼ��ԭ�ӷ������ꡣ�ݴ��ƶϸþ�����Csԭ�ӵ���ĿΪ_________��CsSiB3O7��Ħ������ΪMg��mol��1����NAΪ�����ӵ�������ֵ����CsSiB3O7������ܶ�Ϊ_____g��cm��3���ú���ĸ�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com