

| 1mol |
| 1L |
| 0.75mol/L |
| 2min |
| ���� |
| ���� |
| 56KJ | ||
|



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��MgCl2 |
| B��H2SO4 |
| C��Fe2��SO4��3 |
| D��AgNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
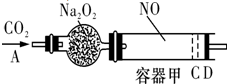 ��ͼװ���У��������ڳ���1mol NO���壬�������װ��һ����Na2O2����A������ͨ��CO2���壮�����£��������л���������D�����ƶ���������C��ʱ�����������С����С��Ϊԭ�����
��ͼװ���У��������ڳ���1mol NO���壬�������װ��һ����Na2O2����A������ͨ��CO2���壮�����£��������л���������D�����ƶ���������C��ʱ�����������С����С��Ϊԭ�����| 9 |
| 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ����۵� | ���ӷ���ʽ | |
| �� | ���е����ӷ���ʽ�����Ա�ʾһ�෴Ӧ | |
| �� | ��������кͷ�Ӧ���ɱ�ʾΪ��H++OH-�TH2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
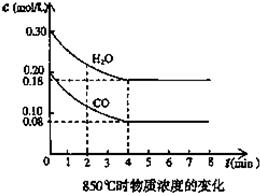 ��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��CO��g��ʮH2O��g��?CO2��g��ʮH2 ��g����H=Q KJ?mol-1 ��Q��0��CO��H2OŨ�ȱ仯��ͼ����0��4min��ƽ����Ӧ����v��CO��=
��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��CO��g��ʮH2O��g��?CO2��g��ʮH2 ��g����H=Q KJ?mol-1 ��Q��0��CO��H2OŨ�ȱ仯��ͼ����0��4min��ƽ����Ӧ����v��CO��=�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ʒ�� | ������ |
| ���� | �ʼ���������ۡ�����ֲ���͡�̼�����ơ������ء����ʻơ��������Ƶ� |
| ������ | 120�� |
| �������� | ���ڰ�װ������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com