
���� ��A�д̼�����ζ����մ��Ũ����IJ������ӽ�Aʱ������ɫ������˵��AΪNH3•H2O��
�ڽ�A�ֱ��������������Һ�У�ֻ��D��F���г��������������������Aʱ��D�г����ޱ仯������ΪAl��OH��3��Mg��OH��2��F�г�����ȫ�ܽ⣬��FΪAgNO3��D����ΪAl2��SO4��3��MgSO4��
�۽�B�ֱ����C��D��E��F�У�C��D��F�в���������E������ɫ����ζ�����ݳ���������ΪCO2��˵��EΪ����Һ���Ҵ�EΪ��ɫ��״Һ�壬˵��EΪH2SO4��
�ܽ�C�ֱ����D��E��F�У����г������ɣ��ټ���ϡHNO3�����������ܣ���ó�������ΪBaSO4��AgCl����CӦΪBaCl2��B����ΪNa2CO3��K2CO3������һ�ֳ�����ҽ�����зdz���Ҫ����;�����ܶȺܴ����ܹ���ֹX����ͨ����˵���������ᱵ�������Դ˽����⣮
��� �⣺��A�д̼�����ζ����մ��Ũ����IJ������ӽ�Aʱ������ɫ������˵��AΪNH3•H2O��
�ڽ�A�ֱ��������������Һ�У�ֻ��D��F���г��������������������Aʱ��D�г����ޱ仯������ΪAl��OH��3��Mg��OH��2��F�г�����ȫ�ܽ⣬��FΪAgNO3��D����ΪAl2��SO4��3��MgSO4��
�۽�B�ֱ����C��D��E��F�У�C��D��F�в���������E������ɫ����ζ�����ݳ���������ΪCO2��˵��EΪ����Һ���Ҵ�EΪ��ɫ��״Һ�壬˵��EΪH2SO4��
�ܽ�C�ֱ����D��E��F�У����г������ɣ��ټ���ϡHNO3�����������ܣ���ó�������ΪBaSO4��AgCl����CӦΪBaCl2��B����ΪNa2CO3��K2CO3������һ�ֳ�����ҽ�����зdz���Ҫ����;�����ܶȺܴ����ܹ���ֹX����ͨ����˵���������ᱵ������
��1�������Ϸ�����֪AΪNH3•H2O��CΪBaCl2���ʴ�Ϊ��NH3•H2O��BaCl2��
��2��FΪAgNO3�����ɵij���ΪAgOH���백ˮ������Ϸ�Ӧ������ʽΪAgOH+2NH3•H2O=Ag ��NH3��2++OH-+2H2O��
�ʴ�Ϊ��AgOH+2NH3•H2O=Ag ��NH3��2++OH-+2H2O��
��3��B����ΪNa2CO3��K2CO3�����е�������Ϊ��ȷ�������ӣ�������ɫ��Ӧ���飬�������ýྻ�IJ�˿պȡ����B����Һ���ھƾ��ƻ��������գ�����ɫ�ʻ�ɫ��BΪNa2CO3��Һ��������ɫ�ܲ����۲���ɫ����ɫ����BΪK2CO3��Һ��
�ʴ�Ϊ��CO32-���ýྻ�IJ�˿պȡ����B����Һ���ھƾ��ƻ��������գ�����ɫ�ʻ�ɫ��BΪNa2CO3��Һ��������ɫ�ܲ����۲���ɫ����ɫ����BΪK2CO3��Һ��
��4��D����ΪAl2��SO4��3��MgSO4��������ΪSO42-�����������ӣ���ȡ����D����Һ�������еμ�NaOH��Һ�г������ɣ������μӹ�����NaOH��Һ���������ܽ⣬��DΪAl2��SO4��3��Һ�����������ܽ⣬��DΪMgSO4��Һ��
�ʴ�Ϊ��SO42-��ȡ����D����Һ�������еμ�NaOH��Һ�г������ɣ������μӹ�����NaOH��Һ���������ܽ⣬��DΪAl2��SO4��3��Һ�����������ܽ⣬��DΪMgSO4��Һ��
���� ���⿼��������ƶϣ�Ϊ�߿��������ͣ���Ŀ�Ѷ��еȣ��漰�����ʼ��顢���ӷ���ʽ��д��֪ʶ��ע�����ճ������ʵļ��鷽�����ܹ����ݷ�Ӧ�����ж�δ֪��ɷ֣�����������ѧ���ķ���������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
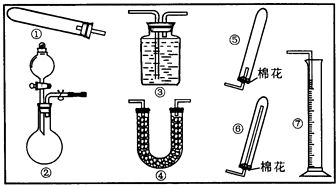
 ��Դ�Ŀ������������������Ŀɳ�����չϢϢ��أ�����������ú���Դ�ǰ���������ǰ���ش���⣮
��Դ�Ŀ������������������Ŀɳ�����չϢϢ��أ�����������ú���Դ�ǰ���������ǰ���ش���⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol����������Ӧ����Na2O��Na2O2ʱ��ʧ������Ŀ��ΪNA | |
| B�� | ������0.1molFeCl3�ı�����Һ�����ˮ�У�������������ĿΪ0.1NA | |
| C�� | 1molC7H16�к��й��ۼ�����ĿΪ23NA | |
| D�� | �����£�1L 0.1 mol•L-1��Na2CO3��Һ�к��е���������Ϊ0.3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �μӷ�Ӧ����������ʵ���Ϊ0.4mol | |
| B�� | ����Ͻ����������Ϊ9.6g | |
| C�� | ������ȫʱ����NaOH��Һ���Ϊ150mL | |
| D�� | �ܽ�Ͻ�ʱ����NO�������0.224L���Ա�״���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �Լ����/NH3�����mL�� | 6.0gCa��OH��2��s�������� | 6.0NaOH��s�������� | 6.0g CaO��s�������� |
| 5.4g NH4Cl��s�� | ��/1344 | ��/1568 | ��/1792 |
| 5.4��NH4��2SO4��s�� | ��1364 | ��1559 | ��/1753 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ������SO42- | B�� | һ������Ag+ | ||
| C�� | һ������Ag+��SO42- | D�� | ���ܺ���Ag+��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����SO3Ϊ2 mol | |
| B�� | ��Ӧ�ų�197 kJ ������ | |
| C�� | SO2��SO3���ʵ���֮��һ��Ϊ2mol | |
| D�� | SO2�����ʵ�����SO3���ʵ���һ����� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com