
【题目】下列事实能用勒夏特列原理解释的是( )
A.工业上N2与H2合成NH3,往往需要使用催化剂
B.密闭容器中2molCO与1molH2O(g)充分反应达平衡后,增大压强CO的反应速率加快
C.SO2与O2催化氧化成SO3是一个放热过程,450℃左右的温度比室温更有利于SO3生成
D.向1.50mol/L的硝酸铵溶液中加入少量氨水至中性,水的电离程度减小
【答案】D
【解析】
A. 催化剂只能改变反应速率,从而改变反应到达平衡的时间,但不能使平衡发生移动,A不合题意;
B. 密闭容器中2molCO与1molH2O(g)发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),达平衡后,增大压强CO的浓度增大,反应速率加快,但平衡不发生移动,B不合题意;
CO2(g)+H2(g),达平衡后,增大压强CO的浓度增大,反应速率加快,但平衡不发生移动,B不合题意;
C. SO2与O2催化氧化成SO3是一个放热过程,从平衡移动的角度考虑,应为降低温度有利于SO3生成,但从催化剂的活性考虑,450℃左右的温度比室温更有利于SO3生成,所以不能利用平衡移动原理解释,C不合题意;
D. 向1.50mol/L的硝酸铵溶液中加入少量氨水,将抑制铵根离子水解,从而使水的电离程度减小,D符合题意。
故选D。


科目:高中化学 来源: 题型:
【题目】“煤制油”的关键技术是煤的气化,目前煤的气化主要是煤中的碳和水蒸气反应: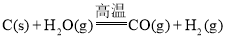 ,该反应是吸热反应,反应所需能量是由间歇进行的碳的燃烧(氧气用空气代替)来提供的:
,该反应是吸热反应,反应所需能量是由间歇进行的碳的燃烧(氧气用空气代替)来提供的: 。下列说法不正确的是( )
。下列说法不正确的是( )
A.煤的气化可以减少煤直接燃烧对环境造成的粉尘污染
B.第一个反应需要吸热,所以煤的气化从能量角度来看,得不偿失
C.煤气化后作为燃料,燃烧充分,热利用率高
D.上述两个反应,反应后的混合气体中除去![]() 、
、![]() 后主要是合成氨的两种原料气体
后主要是合成氨的两种原料气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
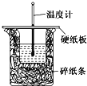
(1)从实验装置上看,图中尚缺少的一种玻璃用品是__________,烧杯间填满碎泡沫塑料的作用是________________________。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值__(填“偏大”、“偏小”或“无影响”)。
(3)实验中若改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量______(填“相等”或“不相等”),所求中和热的数值______(填“相等”或“不相等”),理由是_______________________________。
(4)三次平行操作测得的数据中,起始时盐酸与烧碱溶液温度相同,而终止温度与起始温度之差(t2-t1)分别为2.3 ℃、2.4 ℃、2.9 ℃,则最终代入计算式的温度差的平均值为_____℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放。
(1)用化学方程式表示NO形成硝酸型酸雨的反应______
(2)能作脱除剂的物质很多,下列说法正确的是______
a.用H2O作脱除剂,不利于吸收含氮烟气中的NO
b.用Na2SO3作脱除剂,O2会降低Na2SO3的利用率
c.用CO作脱除剂,会使烟气中NO2的浓度增加
(3)尿素[CO(NH2)2]在一定条件下能有效将NOx转化为N2
Ⅰ.已知可通过下列方法合成尿素:2NH3(g)+CO2(g)![]() H2NCOONH4(s)△H=-159.5kJ/mol
H2NCOONH4(s)△H=-159.5kJ/mol
H2NCOONH4(s)![]() CO(NH2)2(s)+H2O(l) △H=+28.5kJ/mol
CO(NH2)2(s)+H2O(l) △H=+28.5kJ/mol
①尿素释放出NH3的热化学方程式是______。
②写出有利于尿素释放NH3的条件并说明理由______。
ⅡCO(NH2)2与某种烟气![]() 主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线如图:
主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线如图:
①曲线a对应CO(NH2)2与NO的物质的量比值是______。
②曲线a、b、c中,800℃~900℃区间内发生主要反应的化学方程式是______。
③900℃~1200℃区间内脱除率下降,NO浓度上升,发生的主要反应是______。
④曲线a中,NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为______mg/(m3·s) 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来环境问题突出,大气污染更为严重。回答下面问题
(1)下列选项中属于重点城市空气质量日报首要污染物的是_____
A.CO2 B.SO2 C.可吸入颗粒物 D.H2S
(2)汽车尾气常含有CO、NO等有毒气体,汽车气缸中生成NO的化学方程式是___________
(3)汽车排气管装有的三元催化装置,可以消除CO、NO等的污染,反应机理如下(以Pt催化剂为例)
I:NO+Pt(S)=NO(S)(Pt(S)表示催化剂,NO(S)表示吸附态NO,下同)
II:CO+Pt(S)=CO(S)
III:NO(S)=N(S)+O(S)
IV:CO(S)+O(S)=CO2+2Pt(S)
V:N(S)+N(S)=N2+2Pt(S)
VI:NO(S)+N(S)=N2O+2Pt(S)
尾气中反应物及生成物浓度随温度的变化关系如下图。
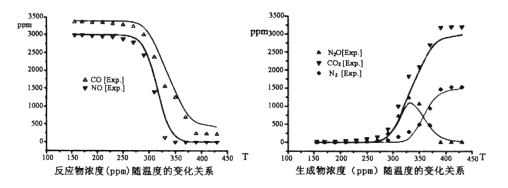
回答下面问题
①汽车尾气消污反应最适宜的反应温度是____
A. 250℃ B.300℃ C.330℃ D.400℃
②330℃以下的低温区发生的主要反应的化学方程式是___________
③低温区N2O选择性高于N2,由此可推断出:V反应的活化能____Ⅵ反应的活化能(填
“<”、“>”或“=”),理由是_______________
④结合反应机理和图像温度位于330℃—400℃时,升高温度,V反应的反应速率_____,(填“增大”、“减小”或“不变”,下同),Ⅳ反应的反应速率__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下表为![]() 时某些弱酸的电离平衡常数。依据所给信息判断,下列说法正确的是( )
时某些弱酸的电离平衡常数。依据所给信息判断,下列说法正确的是( )
| HClO |
|
|
|
|
A.向NaClO溶液中通入少量二氧化碳的离子方程式为:![]()
B.相同浓度的![]() 和NaClO的混合溶液中,
和NaClO的混合溶液中,![]()
C.向![]() 溶液中加入少量水,溶液中pH增大
溶液中加入少量水,溶液中pH增大
D.25℃时,![]() 溶液通入
溶液通入![]() 至溶液的
至溶液的![]() 时,溶液中:
时,溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯酸钾熔化,粒子间克服了________的作用力;二氧化硅熔化,粒子间克服了________的作用力;碘的升华,粒子间克服了________的作用力。
(2)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有________,由非极性键形成的非极性分子有________,能形成分子晶体的物质是________,含有氢键的晶体的化学式是________,属于离子晶体的是________,属于原子晶体的是________,五种物质的熔点由高到低的顺序是____________________________。
(3)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500℃
试推断它们的晶体类型:
A________;B________;C________;D________。
(4)如图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A________;B________;C________;D________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据化学原理的相关知识填空。
⑴常温时,![]() 的水溶液呈酸性,原因是
的水溶液呈酸性,原因是![]() 用离子方程式表示
用离子方程式表示![]() :___________,将
:___________,将![]() 溶液蒸干,灼烧,最后得到的固体产物主要是__________
溶液蒸干,灼烧,最后得到的固体产物主要是__________![]() 填化学式
填化学式![]() 。
。
⑵向![]() 溶液滴加石蕊溶液后变红,则
溶液滴加石蕊溶液后变红,则![]() 的电离程度______其水解程度
的电离程度______其水解程度![]() 填“
填“![]() ”或“
”或“![]() ”或“
”或“![]() ”
”![]() 。该物质能_______
。该物质能_______![]() 填“促进”或“抑制”
填“促进”或“抑制”![]() 水的电离。
水的电离。
⑶若想除去![]() 溶液中混有
溶液中混有![]() 杂质,则往往加入试剂 ________。
杂质,则往往加入试剂 ________。
![]()
![]()
![]()
![]()
⑷泡沫灭火器的灭火原理为___________![]() 用离子方程式解释
用离子方程式解释![]()
⑸在苏打溶液中存在的电荷守恒式为__________;质子守恒式为__________
⑹常温下,物质的量浓度相同的下列溶液:![]()
![]()
![]()
![]()
![]() 溶液中
溶液中![]() 从大到小排列顺序为________
从大到小排列顺序为________![]() 填序号
填序号![]() 。
。
⑺现有a.醋酸、b.盐酸、c.硫酸三种溶液,根据要求答题。
![]() 若它们物质的量浓度相等,它们的pH由大到小的关系为_______(用abc表示,下同)。
若它们物质的量浓度相等,它们的pH由大到小的关系为_______(用abc表示,下同)。
![]() 若它们的pH相等,它们物质的量浓度由大到小的关系为_____。
若它们的pH相等,它们物质的量浓度由大到小的关系为_____。
![]() 若它们的pH相等,均加水稀释100倍后,其pH由大到小的关系为________。
若它们的pH相等,均加水稀释100倍后,其pH由大到小的关系为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是________。
(2)烧杯间填满碎纸条的作用是________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________(填“偏大”、“偏小”或“无影响”)。
(4)该实验常用0.50 mol·L-1 HCl和0.55 mol·L-1 NaOH溶液各50 mL进行实验,其中NaOH溶液浓度大于盐酸浓度的作用是______,当室温低于10 ℃时进行实验,对实验结果会造成较大的误差,其原因是_____________。
(5)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求得的中和热________(填“相等”或“不相等”),简述理由: ______________。
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热ΔH将________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com