
| A. | 标准状况下,11.2L的水中含有0.5NA个水分子 | |
| B. | 含有1molHCl的盐酸中离子总数为NA个 | |
| C. | 1molO2和H2的混合气体中含有NA个分子 | |
| D. | 1mol大米中含有NA个大米粒子 |
分析 A.气体摩尔体积使用对象为气体;
B.氯化氢为强电解质完全电离出氯离子和氢离子;
C.依据N=nNA计算解答;
D.物质的量使用对象为微观粒子.
解答 解:A.标况下水是液体,不能使用气体摩尔体积,故A错误;
B.含有1molHCl的盐酸中,含有1mol氢离子和1mol氯离子,离子总数为2NA个,故B错误;
C.1molO2和H2的混合气体中含有分子数为:1mol×NA=NA,故C正确;
D.物质的量使用对象为微观粒子,不能用于宏观物质,大米为宏观物质,不能使用物质的量,故D错误;
故选:C.
点评 本题考查阿伏伽德罗常数及计算、应用,熟悉物质的量及阿伏伽德罗常数相关概念及计算公式是解题关键,注意物质的量使用对象只限于微观粒子,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
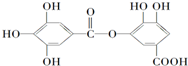
| A. | 在一定条件下,1 mol该物质最多能与6 mol NaOH完全反应 | |
| B. | 有弱酸性,1 mol该有机物与溴水反应,最多能消耗4 mol Br2 | |
| C. | 在Ni催化下,1 mol该物质可以和7 mol H2发生加成反应 | |
| D. | 它能发生水解反应,水解后只能生成两种产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳原子间以单键相连的链烃是烷烃 | B. | 所有糖类物质都有甜味 | ||
| C. | 糖类、油脂都能发生水解 | D. | 淀粉与纤维素互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
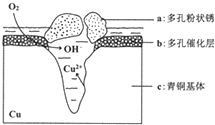 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所得溶液中氯化钠的浓度为1 mol/L | |
| B. | 向所得的溶液中通入二氧化碳,可使溶液具备漂白性 | |
| C. | 所得溶液中有大量的单质的氯元素存在 | |
| D. | 在反应中氯元素化合价降低,钠元素化合价升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,用NaOH溶液滴定20.00mL0.1mol•L-1CH3COOH溶液所得滴定曲线如图,下列说法正确的是( )
常温下,用NaOH溶液滴定20.00mL0.1mol•L-1CH3COOH溶液所得滴定曲线如图,下列说法正确的是( )| A. | 点①所示溶液中:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+) | |
| B. | 点②所示溶液中:c(Na+)═c(CH3COOH)+c(CH3COO-) | |
| C. | 点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定过程中不可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
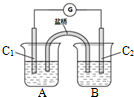 已知砷(As)元素的原子结构示意图为:
已知砷(As)元素的原子结构示意图为:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com