
【题目】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是___。
(2)属于电解质的是____。
(3)属于非电解质的是___。
(4)②在水溶液中的电离方程式为___,①与②在溶液中反应使溶液呈中性的离子方程式为____。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
I.还原产物是___。
II.用单线桥法标出反应中电子转移的方向和数目___。
【答案】④⑥⑨ ①②③⑦⑨⑩ ⑤⑧ KHSO4=K++H++SO42- Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O NO2 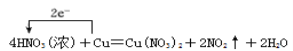
【解析】
(1)含有自由移动电子或离子的物质可以导电,溶于水或在熔融状态下能够导电的化合物是电解质,溶于水和在熔融状态下均不能导电的化合物是非电解质,则
①氢氧化钡固体中不存在自由移动的离子,不导电,溶于水或在熔融状态下能够导电,属于电解质;
②KHSO4中不存在自由移动的离子,不导电,溶于水或在熔融状态下能够导电,属于电解质;
③HNO3中不存在自由移动的离子,不导电,溶于水能够导电,属于电解质;
④稀硫酸中存在自由移动的离子,能导电,但属于混合物,既不属于电解质也不属于非电解质;
⑤二氧化碳气体中不存在自由移动的离子,不导电,CO2的水溶液虽然可以导电,但是溶液中的离子是由碳酸电离产生的,并非CO2自身电离产生的,因此CO2属于非电解质;
⑥铜是金属单质,可以导电,既不属于电解质也不属于非电解质;
⑦碳酸钠粉末中不存在自由移动的离子,不导电,溶于水或在熔融状态下能够导电,属于电解质;
⑧蔗糖晶体中不存在自由移动的离子,不导电,溶于水和熔融状态下都不导电,属于非电解质;
⑨熔融氯化钠中存在自由移动的电子,能导电,熔融NaCl溶于水和熔融状态下都能导电,属于电解质;
⑩CuSO4·5H2O晶体中不存在自由移动的离子,不导电,溶于水或在熔融状态下能够导电,属于电解质;
综上所述,上述状态下可导电的是④⑥⑨;故答案为:④⑥⑨;
(2)属于电解质的是①②③⑦⑨⑩;故答案为:①②③⑦⑨⑩;
(3)属于非电解质的是⑤⑧;故答案为:⑤⑧;
(4)硫酸氢钾是强酸的酸式盐,在水溶液中完全电离,电离方程式为KHSO4=K++H++SO42-;①与②在溶液中反应使溶液呈中性时生成硫酸钡、硫酸钾和水,反应的离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
故答案为:KHSO4=K++H++SO42-;Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
(5)已知③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,则
I.氮元素化合价降低,被还原,还原产物是NO2;
故答案为:NO2;
II.氮元素从+5价降低到+4价,只有2mol氮元素变价,铜元素化合价从0价升高到+2价,转移2mol电子,则根据得失电子守恒用单线桥法标出反应中电子转移的方向和数目可表示为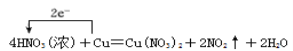 ;
;
故答案为: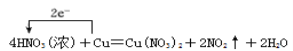 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】室温下向10 mL 0.1 mol·L-1 NaOH溶液中加入0.1 mol·L-1的一元
酸HA,溶液pH的变化曲线如图所示。下列说法正确的是

A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. b点所示溶液中c(A-)>c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列物质的化学性质,判断其应用错误的是
A. 酒精能使蛋白质变性,可用于杀菌消毒
B. CaO能与SO2反应,可作工业废气的脱硫剂
C. 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂
D. 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是

A. 原子半径:W<X
B. 常温常压下,Y单质为固态
C. 气态氢化物热稳定性:Z<W
D. X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
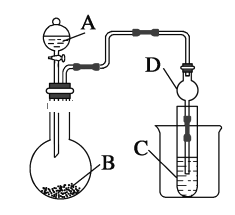
【题目】利用下图装置可以验证非金属性的变化规律。
(1)仪器A的名称为________,球形管D的作用是________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为____________________________________________________________。
(3)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加________,观察到C中溶液的现象为_____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是
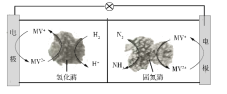
A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区,在氢化酶作用下发生反应H2+2MV2+![]() 2H++2MV+
2H++2MV+
C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D. 电池工作时质子通过交换膜由负极区向正极区移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
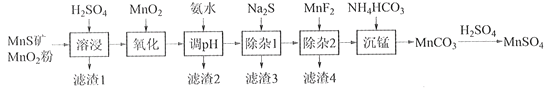
相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________。
(6)写出“沉锰”的离子方程式___________________________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnz2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___________。
时,z=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)合成氨工业对国民经济和社会发展具有重要意义,对于密闭容器中的反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0。写出该反应化学平衡常数表达式_______,升高温度,该反应化学反应速率_______,氢气的转化率_______ (以上均填“增大”、“减小”或“不变”)。实际生产中温度一般控制在500℃,原因是_______。
2NH3(g) ΔH<0。写出该反应化学平衡常数表达式_______,升高温度,该反应化学反应速率_______,氢气的转化率_______ (以上均填“增大”、“减小”或“不变”)。实际生产中温度一般控制在500℃,原因是_______。
(2)在500℃下合成甲醇的反应原理为:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),在1L的密闭容器中,充入1molCO2和3molH2,压强为p0,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),在1L的密闭容器中,充入1molCO2和3molH2,压强为p0,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
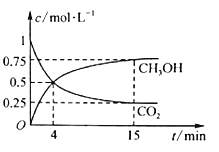
①反应进行到4 min时,v(正)________ (填“>”“<”或“=”)v(逆)。0~4 min,H2的平均反应速率v(H2)= _______。
②下列能说明该反应已达到平衡状态的是_______。
A v正(CH3OH)=3v逆(H2) B CO2、H2、CH3OH和H2O浓度之比为1:3:1:1
C 恒温恒压下,气体的体积不再变化 D 恒温恒容下,气体的密度不再变化
③500℃、在2个容积都是2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
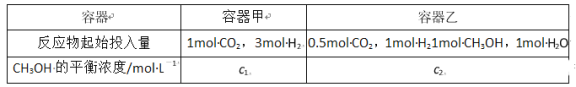
则乙容器中反应起始向_______方向进行;c1_______c2(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将Ⅰ阀关闭,Ⅱ阀打开,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色.甲瓶中所盛的试剂可能是
①浓硫酸 ②饱和氯化钠溶液 ③NaOH溶液 ④饱和碳酸钠溶液 ⑤水

A. ①③ B. ②⑤ C. ②③⑤ D. ①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com