
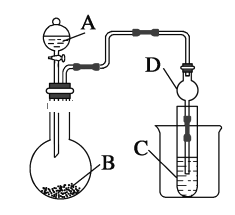
【题目】利用下图装置可以验证非金属性的变化规律。
(1)仪器A的名称为________,球形管D的作用是________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为____________________________________________________________。
(3)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加________,观察到C中溶液的现象为_____________________________
【答案】分液漏斗 防止倒吸 浓盐酸 KMnO4 Na2S溶液 S2-+Cl2===S↓+2Cl- 硫酸 Na2SiO3溶液 有白色胶状沉淀产生
【解析】
(1)仪器A的名称为分液漏斗,球形管D的作用是防止倒吸;
(2)通过证明Cl2氧化性大于S,验证氯的非金属性大于硫;
(3)通过证明碳酸酸性大于硅酸,来证明非金属性:C>Si。
(1)仪器A的名称为分液漏斗,球形管D的作用是防止倒吸;
(2)先利用浓盐酸和KMnO4来制取Cl2,再用Cl2与Na2S反应产生S验证氯的非金属性大于硫。故装置A、B、C中所装药品分别为浓盐酸、KMnO4、Na2S,装置C中的离子方程式为S2-+Cl2===S↓+2Cl-;
(3)要证明非金属性:C>Si,则A中加稀硫酸、B中加Na2CO3,产生二氧化碳气体,C中加Na2SiO3溶液,观察到C中溶液的现象为有白色胶状沉淀产生。


科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A.等物质的量的NaCl和MgCl2所含Cl-物质的量相等
B.1.7gH2O2中含有电子数为0.9NA
C.常温下,1L0.1mol·L-1的NH4NO3溶液中含氮原子数为0.2NA
D.常温常压下,32gSO2物质的量为0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过量SO2通入下列溶液中,能出现白色浑浊的是( )。
①Ca(OH)2 ②BaCl2 ③NaAlO2 ④Na2SiO3 ⑤Ba(NO3)2 ⑥苯酚钠 ⑦Na2CO3
A. ①②④⑦ B. ②③⑥⑦ C. ④⑤⑥⑦ D. ③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是
A. 3g 3He含有的中子数为1NA
B. 1 L 0.1 mol·L1磷酸钠溶液含有的![]() 数目为0.1NA
数目为0.1NA
C. 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D. 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式中,不能正确表达反应颜色变化的是
A. 向CuSO4溶液中加入足量Zn粉,溶液蓝色消失Zn+CuSO4![]() Cu+ZnSO4
Cu+ZnSO4
B. 澄清的石灰水久置后出现白色固体Ca(OH)2+CO2![]() CaCO3↓+H2O
CaCO3↓+H2O
C. Na2O2在空气中放置后由淡黄色变为白色2Na2O2![]() 2Na2O+O2↑
2Na2O+O2↑
D. 向Mg(OH)2悬浊液中滴加足量FeCl3溶液出现红褐色沉淀3Mg(OH)2+2FeCl3![]() 2Fe(OH)3+3MgCl2
2Fe(OH)3+3MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是___。
(2)属于电解质的是____。
(3)属于非电解质的是___。
(4)②在水溶液中的电离方程式为___,①与②在溶液中反应使溶液呈中性的离子方程式为____。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
I.还原产物是___。
II.用单线桥法标出反应中电子转移的方向和数目___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)![]() 1/2N2(g)+CO2(g)ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和CO的转化率,采取的正确措施是( )
1/2N2(g)+CO2(g)ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和CO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度
B. 升高温度同时充入N2
C.加催化剂同时增大压强
D.降低温度同时减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应A+2B![]() 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断下列结论错误的是( )
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断下列结论错误的是( )
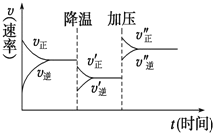
A.正反应是放热反应B.A、B一定都是气体
C.D一定不是气体D.C可能是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1.7g氨气在标准状况下的体积是_____________升,共含有_____________mol电子;0.1mol硫化氢共含有_____________个质子,同质量的氨气和硫化氢气体中分子个数比为_____________,含氢原子的个数比为_____________。在标准状况下硫化氢的密度为_____________。
(2)在标准状况下,18gCO和CO2的混合气体完全燃烧后得到11.2LCO2,则原混合气体的密度是_____________,原混合气体中,CO的质量是_____________,CO2的体积是_____________碳原子和氧原子的个数比为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com