
����Ŀ����ˮ��ɽ���ǽ�ɽ��ɽ���ҹ�������Ա��̽����ν��ʹ����е���������̼������ĺ������������˾��ף���ȡ���������ijɼ���
(1)���й��ڵ���������̼�������˵������ȷ����_____(����ĸ)��
A.CO2��NO2����������������
B.NO��CO���������ſ������ռ�
C.��ȥNO�л��е�NO2�ķ����ǽ��������ͨ����������������Һ��
D.��ȥCO�л��е�CO2�ķ����ǽ��������ͨ����������������Һ��
(2)��֪:N2(g)+O2(g)![]() 2NO(g)��H1=+180.5kJ/mol;
2NO(g)��H1=+180.5kJ/mol;
CO(g)![]() C(s)+1/2O2(g)��H2=+110.5kJ/mol;
C(s)+1/2O2(g)��H2=+110.5kJ/mol;
C(s)+O2(g)![]() CO2(g)��H3=-393.5kJ/mol��
CO2(g)��H3=-393.5kJ/mol��
��Ӧ2NO(g)+2CO(g)![]() N2(g)+2CO2(g)��H=__________
N2(g)+2CO2(g)��H=__________
(3)��Ӧ2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)�����ھ�������β������֪570Kʱ�÷�Ӧ�ķ�Ӧ���ʼ���,ƽ�ⳣ�������ɴ˿�֪�����β������Ч�ʵ����;����_________;��Ҫ��������β����ͬʱ��߸÷�Ӧ�ķ�Ӧ���ʺ�NO��ת����,��ֻ�ı�һ����Ӧ����,��Ӧ��ȡ�Ĵ�ʩ��_________��
2CO2(g)+N2(g)�����ھ�������β������֪570Kʱ�÷�Ӧ�ķ�Ӧ���ʼ���,ƽ�ⳣ�������ɴ˿�֪�����β������Ч�ʵ����;����_________;��Ҫ��������β����ͬʱ��߸÷�Ӧ�ķ�Ӧ���ʺ�NO��ת����,��ֻ�ı�һ����Ӧ����,��Ӧ��ȡ�Ĵ�ʩ��_________��
(4)ij����С����ݷ�Ӧ2NO(g)+2CO(g)![]() N2(g)+2CO2(g)��̽����ʼ��Ӧ���̼����[n(CO)/n(NO)]����Ⱦ��ȥ���ʵ�Ӱ�졣T��ʱ�������Ϊ1L�ĺ����ܱ������г��������ʵ���Ϊ4mol��NO��CO������壬������һ�����Ĺ���������з�Ӧ,ʵ����ƽ����ϵ��������ֵ�ת���ʺ���������������ı仯��ͼ��ʾ.
N2(g)+2CO2(g)��̽����ʼ��Ӧ���̼����[n(CO)/n(NO)]����Ⱦ��ȥ���ʵ�Ӱ�졣T��ʱ�������Ϊ1L�ĺ����ܱ������г��������ʵ���Ϊ4mol��NO��CO������壬������һ�����Ĺ���������з�Ӧ,ʵ����ƽ����ϵ��������ֵ�ת���ʺ���������������ı仯��ͼ��ʾ.

�ٸ���ͼ���Ʋ�����ת����1��ʾ����______ (�CO����NO��)��
��A��ʱ��n(CO)/n(NO)=_________,��ʱ��Ӧ��ƽ�ⳣ��K= __________(����д��ֵ�뵥λ)��
(5)ú̿��O2/CO2��������ȼ�ջ����CO,�������,������Ʒ�Ӧ2CO(g)=2C(s)+O2(g)������CO����Ⱦ��������_______(����С������С�), ������_______��
���𰸡� BD -746.5k]/mol ���Ƹ�Ч���� ����ѹǿ NO 1 80L/mol ������ �÷�Ӧ��H>0����S<0,��H-T��S>0,�÷�Ӧ���κ�����¶������Է�����
��������(1) A.CO2�������������NO2��ˮ��Ӧ���������һ�����������������������ѡ��A����B.NO����������Ӧ��CO�ܶ���������ܶȽӽ������������ſ������ռ���ѡ��B��ȷ��C. NO��NO2�����������ܷ�Ӧ����ȥNO�л��е�NO2�ķ����ǽ��������ͨ��ˮ�У�ѡ��C����D.��ȥCO�л��е�CO2�ķ����ǽ��������ͨ����������������Һ�У�������̼���������Ʒ�Ӧ��һ����̼����Ӧ��ѡ��D��ȷ����ѡBD��(2)��֪:��N2(g)+O2(g)![]() 2NO(g)��H1=+180.5kJ/mol����CO(g)
2NO(g)��H1=+180.5kJ/mol����CO(g)![]() C(s)+1/2O2(g)��H2=+110.5kJ/mol����C(s)+O2(g)
C(s)+1/2O2(g)��H2=+110.5kJ/mol����C(s)+O2(g)![]() CO2(g)��H3=-393.5kJ/mol�����ݸ�˹���ɣ���
CO2(g)��H3=-393.5kJ/mol�����ݸ�˹���ɣ���![]() ��+�۵÷�Ӧ2NO(g)+2CO(g)
��+�۵÷�Ӧ2NO(g)+2CO(g)![]() N2(g)+2CO2(g)��H=2��H2-��H1+��H3=2
N2(g)+2CO2(g)��H=2��H2-��H1+��H3=2![]() 110.5kJ/mol-180.5kJ/mol-393.5kJ/mol=-746.5k]/mol����3�����Ƹ�Ч��������߷�Ӧ���ʣ������Ӧ���������⣬������β����ת��������ѹǿ����ѧ��Ӧ���ʼӿ죬��ѧƽ�������������С�ķ����ƶ���������Ӧ����NO��ת����ת��������(4)����ʼ��Ӧ���̼����[n(CO)/n(NO)]Խ��һ��������ת����Խ����ͼ���Ʋ�����ת����1��ʾ����NO���ڷ�Ӧ2NO(g)+2CO(g)
110.5kJ/mol-180.5kJ/mol-393.5kJ/mol=-746.5k]/mol����3�����Ƹ�Ч��������߷�Ӧ���ʣ������Ӧ���������⣬������β����ת��������ѹǿ����ѧ��Ӧ���ʼӿ죬��ѧƽ�������������С�ķ����ƶ���������Ӧ����NO��ת����ת��������(4)����ʼ��Ӧ���̼����[n(CO)/n(NO)]Խ��һ��������ת����Խ����ͼ���Ʋ�����ת����1��ʾ����NO���ڷ�Ӧ2NO(g)+2CO(g)![]() N2(g)+2CO2(g)��NO��CO�Ļ�ѧ��������ȣ�A��ʱ�����ߵ�ת������ȣ���Ϊ80%����n(CO)/n(NO)=1,��ʱ�����ʵ�Ũ�ȷֱ�Ϊ0.4mol/L��0.4mol/L��0.8mol/L��1.6mol/L����Ӧ��ƽ�ⳣ��K=
N2(g)+2CO2(g)��NO��CO�Ļ�ѧ��������ȣ�A��ʱ�����ߵ�ת������ȣ���Ϊ80%����n(CO)/n(NO)=1,��ʱ�����ʵ�Ũ�ȷֱ�Ϊ0.4mol/L��0.4mol/L��0.8mol/L��1.6mol/L����Ӧ��ƽ�ⳣ��K=![]() ��(5)��Ʒ�Ӧ2CO(g)=2C(s)+O2(g)������CO����Ⱦ�����鲻����, �����Ǹ÷�Ӧ��H>0����S<0.��H-T��S>0,�÷�Ӧ���κ�����¶������Է����С�
��(5)��Ʒ�Ӧ2CO(g)=2C(s)+O2(g)������CO����Ⱦ�����鲻����, �����Ǹ÷�Ӧ��H>0����S<0.��H-T��S>0,�÷�Ӧ���κ�����¶������Է����С�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪: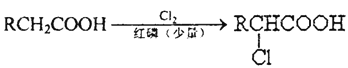
![]()
����ƽF�ǽ�Ѫ֬�������̴���ҩ�����һ���ϳ�·������:
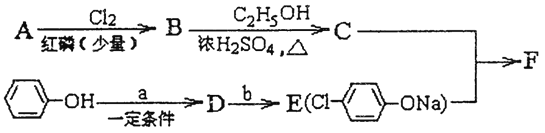
(1)AΪһԪ���ᣬ8.8gA������NaHCO3��Һ��Ӧ����2.24LCO2(��״��)��A�ķ���ʽΪ_________��
(2)д������A����ʽ�����м������Ľṹ��ʽ:____________��
(3)B���ȴ����ᣬ��˴Ź��������������壬д��B��C�ķ�Ӧ����ʽ:_______��
(4)C+E��F�ķ�Ӧ����Ϊ___________��
(5)д��A��F�Ľṹ��ʽ:A______��F_______
(6)D�ı������������⣬�����������ŵ�����Ϊ________��д��a��b���������Լ�:a. _______b. _______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H2(g)��Br2(g)===2HBr(g)����H����72 kJ/mol����������������±���
���� | H2(g) | Br2(g) | HBr(g) |
1 mol �����еĻ�ѧ���� ��ʱ��Ҫ���յ�����/kJ | 436 | a | 369 |
�����aΪ(����)
A.404B.260C.230D.200
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ������Ǻϳ��л������ĵ��壬��ϳɷ���֮һ���£�CH3OC��CH+CH3OH+A ![]() CH2=C(CH3)COOCH3������˵����ȷ����
CH2=C(CH3)COOCH3������˵����ȷ����
A. ��֪�÷�Ӧ��ԭ��������Ϊ100%����AΪCO2
B. CH3OH���ͻ�Ϊͬϵ��
C. CH3C��CH���ϩ���������ƣ�������ʿ��Է����ӳɡ�������Ӧ
D. ����NaHCO3��Ӧ��CH2=C(CH3)COOCH3��ͬ���칹����9��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ�����ı�־�ǣ� ��
A.ԭ��ѧ˵��1803�꣩
B.Ԫ�������ɣ�1869�꣩
C.��ѧԪ�صĸ��1661�꣩
D.����ѧ˵��1771�꣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ԭ��Ӧ����
A. CaO+H2O=Ca(OH)2 B. 2NaHCO3![]() Na2CO3+CO2��+H20
Na2CO3+CO2��+H20
C. 2KBr+Cl2=2KCl+Br2 D. HCl+NaOH=NaCl+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��Q��W��R��ԭ���������䳣�����ϼ۹�ϵ����ͼ��ʾ������˵����ȷ����
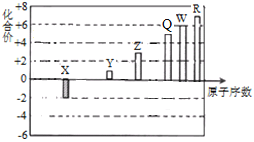
A. X��Y��R�γɵ�ij�ֻ������������Ư�ס�����
B. Q��W������������Ӧ��ˮ��������ǰ�ߴ��ں���
C. X��Y��Z��W��R�ļ����Ӱ뾶��С˳��ΪR��W��Z��Y��X
D. Y��Z��W��������������Ӧ��ˮ����䲻���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ij�л�����ӵļ������ģ�ͣ����л����к�C��H��O��N����Ԫ�ء����й��ڸ��л����˵���д������( )

A. ����ʽΪC3 H7O2N B. �ܷ���ȡ����Ӧ
C. ��ͨ���ۺϷ�Ӧ���ɸ߷��ӻ����� D. ���ܸ�NaOH��Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ����Ҫ���л�����ԭ�ϣ�C02��H2�ڴ���CZZA(��ͨͭ������)�����ºϳɼ״�����ط�Ӧ���£�
��Ӧ�� CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H1 = -49.2kJ��mol-1
CH3OH(g)+H2O(g) ��H1 = -49.2kJ��mol-1
��Ӧ�� CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H2
CO(g)+H2O(g) ��H2
��֪����CO��H2�ı�ȼ���ȷֱ�Ϊ-283.0kJ��mol-1��-285.8kJ��mol-1
��H2O(g)=H2O(l) ��H3 = -44.0kJ��mol-1
��ش�
��1����Ӧ��ġ�H2 =___________________kJ��mol-1��
��2���о�������������������ͬ������£�������CZZA�������ʹ���(CZZA/rGO)������������״���ѡ���ԣ����ù���̬���۽�����ԭ��___________________��
��3����CZZA/rGOΪ��������һ�������£������ʵ���֮��Ϊ1:3(����Ϊa mol)��C02��H2ͨ������ܱ������н��з�Ӧ��CO2��ƽ��ת���ʺͼ״���ѡ����(�״���ѡ���ʣ�ת����CO2�����ɼ״������ʵ�������)���¶ȵı仯��������ͼ��ʾ��
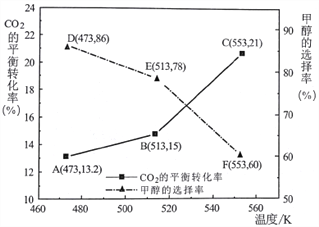
����553Kʱ����Ӧ��ϵ�ڼ״������ʵ���Ϊ___________________mol��
�������¶ȵ����ߣ�C02��ƽ��ת�������ӵ��״���ѡ���ʽ��ͣ��������ԭ��__________________��
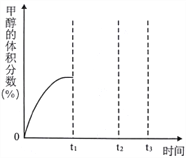
��4����CO2��H2�����ʵ���֮��Ϊ1:3ͨ����º����ܱ������У�����������ʹ���������Ӧ����У��õ��״������������ʱ��Ĺ�ϵ����ͼ2��ʾ�����������������䣬t1ʱ���������м���һ�������ʵ���֮��Ϊ1:3��CO2��H2�������t2ʱ�ٴδﵽƽ�⣬������ͼ�л���t1��t3ʱ���ڼ״����������ʱ��ı仯���ߡ�__________________
��5���ڴ��������£���NaOH��ҺΪ���Һ������������ͨ��ʯī���ϵ缫���������״���д��������Ӧ�ĵ缫��Ӧʽ___________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com