
【题目】甲醇是一种重要的有机化工原料,C02与H2在催化剂CZZA(普通铜基催化剂)作用下合成甲醇,相关反应如下:
反应Ⅰ CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1 = -49.2kJ·mol-1
CH3OH(g)+H2O(g) △H1 = -49.2kJ·mol-1
反应Ⅱ CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(g)=H2O(l) △H3 = -44.0kJ·mol-1
请回答:
(1)反应Ⅱ的△H2 =___________________kJ·mol-1。
(2)研究表明:在其他条件相同的情况下,将催化剂CZZA换成新型催化剂(CZZA/rGO),可以显著提高甲醇的选择性,试用过渡态理论解释其原因:___________________。
(3)以CZZA/rGO为催化剂,在一定条件下,将物质的量之比为1:3(总量为a mol)的C02与H2通入恒容密闭容器中进行反应,CO2的平衡转化率和甲醇的选择率(甲醇的选择率:转化的CO2中生成甲醇的物质的量分数)随温度的变化趋势如下图所示:
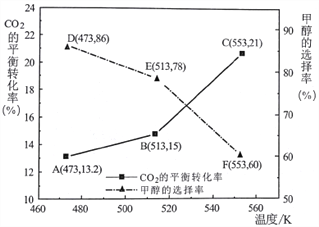
①在553K时,反应体系内甲醇的物质的量为___________________mol。
②随着温度的升高,C02的平衡转化率增加但甲醇的选择率降低,请分析其原因:__________________。
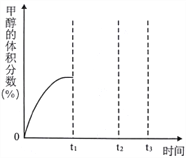
(4)将CO2与H2按物质的量之比为1:3通入恒温恒容密闭容器中,控制条件,使其仅仅按反应Ⅰ进行,得到甲醇的体积分数与时间的关系如上图2所示。保持其它条件不变,t1时再向容器中加入一定量物质的量之比为1:3的CO2与H2混合气,t2时再次达到平衡,请在下图中画出t1~t3时间内甲醇体积分数随时间的变化曲线。__________________
(5)在催化剂作用下,以NaOH溶液为电解液,将甲烷气体通入石墨复合电极,电解产生甲醇。写出阳极反应的电极反应式___________________。
【答案】 41.2 新型催化剂能将反应Ⅰ活化能降低更多,使反应物更容易生成甲醇 0.0315a 当温度升高时反应Ⅰ平衡逆向移动,而反应Ⅱ平衡正向移动且幅度更大,所以CO2的转化率增加,但甲醇的选择性却降低。 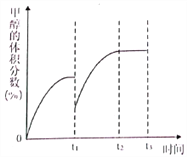 CH4 -2e- +2OH- =CH3OH+H2O
CH4 -2e- +2OH- =CH3OH+H2O
【解析】①CO(g)+![]() O2(g)=CO2(g) △H=-283.0kJmol-1、②H2(g)+
O2(g)=CO2(g) △H=-283.0kJmol-1、②H2(g)+![]() O2(g)=H2O(l) △H=-285.8kJmol-1,③H2O(g)=H2O(l) △H3 = -44.0kJ·mol-1,④反应Ⅰ CO2(g)+3H2(g)
O2(g)=H2O(l) △H=-285.8kJmol-1,③H2O(g)=H2O(l) △H3 = -44.0kJ·mol-1,④反应Ⅰ CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1 = -49.2kJ·mol-1,⑤反应Ⅱ CO2(g)+H2(g)
CH3OH(g)+H2O(g) △H1 = -49.2kJ·mol-1,⑤反应Ⅱ CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
(1)由盖斯定律,②-①-③反应Ⅱ的△H2 =-285.8kJmol-1-(-283.0kJmol-1)-( -44.0kJ·mol-1)=41.2 kJ·mol-1。(2)在其他条件相同的情况下,将催化剂CZZA换成新型催化剂(CZZA/rGO),可以显著提高甲醇的选择性,用过渡态理论解释其原因:新型催化剂能将反应Ⅰ活化能降低更多,使反应物更容易生成甲醇;
(3)CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g)
CH3OH(g) + H2O(g)
n始 0.25a 0.75a
n变 0.25a×0.21×60% 0.0315a
n平 0.0315a
①在553K时,反应体系内甲醇的物质的量为 0.25a×0.21×60%=0.0315a;②随着温度的升高,C02的平衡转化率增加但甲醇的选择率降低,其原因:当温度升高时反应Ⅰ平衡逆向移动,而反应Ⅱ平衡正向移动且幅度更大,所以CO2的转化率增加,但甲醇的选择性却降低。(4)保持其它条件不变,t1时再向容器中加入一定量物质的量之比为1:3的CO2与H2混合气,t2时再次达到平衡,t2时相当于对原平衡进行加压,平衡正向移动,甲醇的体积分数增大,如图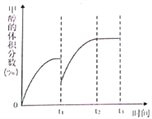 。(5)在催化剂作用下,以NaOH溶液为电解液,将甲烷气体通入石墨复合电极,电解产生甲醇。阳极甲烷氧化生成甲醇,阳极反应的电极反应式:CH4 -2e- +2OH- =CH3OH+H2O。
。(5)在催化剂作用下,以NaOH溶液为电解液,将甲烷气体通入石墨复合电极,电解产生甲醇。阳极甲烷氧化生成甲醇,阳极反应的电极反应式:CH4 -2e- +2OH- =CH3OH+H2O。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】绿水青山就是金山银山,我国科研人员在探究如何降低大气中氮氧化物与碳氧化物的含量方面做出了巨大贡献,并取得了显著的成绩。
(1)下列关于氮氧化物与碳氧化物的说法中正确的是_____(填字母)。
A.CO2、NO2均属于酸性氧化物
B.NO、CO均不能用排空气法收集
C.除去NO中混有的NO2的方法是将混合气体通入足量氢氧化钠溶液中
D.除去CO中混有的CO2的方法是将混合气体通入足量氢氧化钠溶液中
(2)已知:N2(g)+O2(g)![]() 2NO(g)ΔH1=+180.5kJ/mol;
2NO(g)ΔH1=+180.5kJ/mol;
CO(g)![]() C(s)+1/2O2(g)ΔH2=+110.5kJ/mol;
C(s)+1/2O2(g)ΔH2=+110.5kJ/mol;
C(s)+O2(g)![]() CO2(g)ΔH3=-393.5kJ/mol。
CO2(g)ΔH3=-393.5kJ/mol。
则反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)ΔH=__________
N2(g)+2CO2(g)ΔH=__________
(3)反应2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)可用于净化汽车尾气,已知570K时该反应的反应速率极慢,平衡常数极大。由此可知,提高尾气净化效率的最佳途径是_________;若要净化汽车尾气的同时提高该反应的反应速率和NO的转化率,且只改变一个反应条件,则应采取的措施是_________。
2CO2(g)+N2(g)可用于净化汽车尾气,已知570K时该反应的反应速率极慢,平衡常数极大。由此可知,提高尾气净化效率的最佳途径是_________;若要净化汽车尾气的同时提高该反应的反应速率和NO的转化率,且只改变一个反应条件,则应采取的措施是_________。
(4)某科研小组根据反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)来探究起始反应物的碳氨比[n(CO)/n(NO)]对污染物去除率的影响。T℃时,向体积为1L的恒容密闭容器中充入总物质的量为4mol的NO和CO混合气体,并加入一定量的固体催化剂进行反应,实验测得平衡体系中气体组分的转化率和氯气的体积分数的变化如图所示.
N2(g)+2CO2(g)来探究起始反应物的碳氨比[n(CO)/n(NO)]对污染物去除率的影响。T℃时,向体积为1L的恒容密闭容器中充入总物质的量为4mol的NO和CO混合气体,并加入一定量的固体催化剂进行反应,实验测得平衡体系中气体组分的转化率和氯气的体积分数的变化如图所示.

①根据图像推测曲线转化率1表示的是______ (填“CO”或“NO”)。
②A点时,n(CO)/n(NO)=_________,此时反应的平衡常数K= __________(请填写数值与单位)。
(5)煤炭在O2/CO2的气氛中燃烧会产生CO,有人提出,可以设计反应2CO(g)=2C(s)+O2(g)来消除CO的污染。该提议_______(填“可行”或“不可行”), 理由是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了防止番茄在长途运输中发生腐烂,常常运输尚未完全成熟的果实,运到目的地后再用一种植物生长调节剂将其催熟。这种植物生长调节剂是下列物质中的
A. 乙烷 B. 乙烯 C. 乙炔 D. 乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 聚合物![]() 可由单体CH3CH=CH2和CH2=CH2加聚制得
可由单体CH3CH=CH2和CH2=CH2加聚制得
B. 1 molCH3COOH与1mol CH3CH2OH在浓硫酸共热下生成的乙酸乙酯分子数为NA
C. 乙醇、苯酚、乙酸都有羟基,但是羟基上的H活泼性不同,主要是基团之间相互影响造成的
D. 等物质的量的乙炔和乙醛分别充分燃烧,所耗用氧气的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属的硝酸盐加热分解生成NO2和O2的分子数之比为4:1.在加热分解过程中,该金属元素( )
A.化合价升高
B.化合价降低
C.化合价不变
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢溴酸槟榔碱是驱除动物绦虫的有效药物,可由脂A(C4H6O2)经过如下合成路线获得:

已知:Ⅰ. 含碳碳双键的有机物与氨(NH3)或胺(RNH2)反应生成新的胺类化合物
如:R1CH=CH2 + RNH2![]() R1CH2CH2NHR
R1CH2CH2NHR
Ⅱ. R1COOR2 + R3CH2COOR4![]()
![]() + R2OH
+ R2OH
请回答:
(1)化合物E的结构简式___________________。
(2)下列说法不正确的是___________________。
A. 化合物A能发生还原反应,不能发生氧化反应
B. 化合物F能与FeCl3溶液发生显色反应
C. 化合物G具有碱性,可以生成内盐
D. 氢溴酸槟榔碱的分子式为C8H14O2NBr
(3)写出B+A→C的化学方程式___________________。
(4)写出化合物B可能的同分异构体的结构简式___________________,须同时符合:
① 分子结构中有一个六元环;
② 1H-NMR谱显示分子中有3种氢原子,IR谱显示有C-N键存在。
(5)设计酯A经路径二,通过两步反应转变为化合物E的合成路线(用流程图表示,所用试剂与路径一相同)___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,能在水溶液中大量共存的是
A. K+、SO42-、HCO3-、H+ B. NH4+、Cl-、OH-、Na+
C. CO32-、Na+、K+、OH- D. Na+、Ag+、H+、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用氯化铵与氢氧化钙的固体混合物加热制取氨气,下列是实验室提供的有关装置:
气体发生装置 |
a |
b |
c |
气体收集装置 |
A |
B |
C |
上述制备氨气的化学方程为_________________________________。从上图中选择实验室制取氨气的气体发生装置________(选填编号)、气体收集装置_________(选填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法正确的是 ( )
A. 2.4g金属镁所含电子数目为0.2NA B. 16g CH4所含原子数目为NA
C. 17gNH3所含质子数目为10 NA D. 18g水所含分子数目为18NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com